Explosif
Un explosif est défini par un mélange de corps qui, lors de leur transformation, sont susceptibles de dégager en un temps très court un grand volume de gaz porté à haute température, ce qui constitue une explosion. Une charge explosive (en anglais : explosive charge) est une quantité mesurée de matière explosive.
Histoire
Le premier composé explosif était très probablement la poudre noire, communément appelée la poudre à canon1. Sa première apparition date de 220 avant J.-C. lorsque des alchimistes chinois l'ont enflammée par accident. Cependant, la poudre noire n'a pas été introduite en Europe avant le XIIIe siècle. Elle est pour la première fois utilisée en génie civil afin de réaliser le dragage de la Rivière Niermen en Europe du Nord.
En 1846, le professeur italien Ascanio Sobrero découvre la nitroglycérine liquide2. Quelques années plus tard, un inventeur du nom de Immanuel Nobel va développer un procédé de fabrication de la nitroglycérine. Dans la même année, parallèlement à la préparation de la nitroglycérine, certains chercheurs se sont intéressés à la nitration de la cellulose afin d'obtenir de la nitrocellulose. La paternité de la nitrocellulose revient au chimiste inorganicien allemand Rudolf Christian Böttger3. Par sa grande instabilité, la nitrocellulose a provoqué de nombreux accidents dans les usines de production. En 1865, Sir Frederick Abel publie une solution en convertissant la nitrocellulose sous forme de pâte.
En 1875, Alfred Nobel, le fils d'Immanuel Nobel, découvrit que le mélange de nitrocellulose avec de la nitroglycérine donnait un gel. Ce gel a ensuite été développé afin de produire de la gélatine de dynamite4.
En 1895, le chimiste allemand Richard Wolffenstein découvrit le TATP5. Le TATP ( triperoxyde de triacétone) fait partie d’une famille de molécules instables constituées de peroxydes organiques cycliques.
Plus tard, vers la fin du XIXe siècle, l'acide picrique et le trinitrophénol sont apparus comme substitut de la poudre noire. L'acide picrique a été préparé en grande échelle en 1894 afin d'être utilisé comme explosif de base dans les utilisations militaires6.
Enfin, en 1863, le chimiste allemand Julius Adolph Wilbrand découvrit le trinitrotoluène (TNT)7. En 1914, il deviendra l'explosif standard des armées durant la Première Guerre mondiale.
Classification
Par comportement physique
De l'explosion résulte la création d'un front d'onde de pression. La vitesse de ce front d'onde détermine la classification des explosifs. Il existe trois grands groupes d'explosifs :
- les explosifs soufflants (régime de déflagration) ;
- les explosifs brisants (régime de détonation) ;
- les explosifs progressifs se situent entre les soufflants et les brisants.
La différence entre les régimes de déflagration et de détonation n'est pas toujours simple. Selon les conditions d'utilisation, un explosif normalement déflagrant peut détoner, et un explosif normalement détonant peut déflagrer.
- Les explosifs soufflants sont conçus pour un régime de déflagration, c’est-à-dire une auto-combustion subsonique (la réaction chimique se propage à la vitesse de 10 à 400 m/s dans l'explosif lui-même).
- Les explosifs progressifs suivent le régime de détonation supersonique (de 2 000 à 3 500 m/s).
- Les explosifs brisants détonent également (de 4 000 à 9 000 m/s).
Les explosifs peuvent aussi être utilisés pour la propulsion de projectiles ou fusées sous forme de poudre ou propergol. Le régime est alors la combustion qui doit être très bien maîtrisée (exemple, les deux propulseurs d'appoint à poudre de chaque côté de la fusée Ariane).
Explosif soufflant
Un explosif soufflant est un explosif qui provoque lors de son explosion une pression dans les directions de moindre résistance. Si on place une petite charge d'explosif soufflant sur un mur, lors de l'explosion la pression va s'appliquer à l'opposé du mur, le mur restera intact. Au contraire, si on avait placé une charge d'explosif brisant, le mur aurait été endommagé ou perforé.
On peut citer à titre d'exemple les explosifs soufflants suivants :
- la poudre noire, surtout utilisée pour les canons d'autrefois, les feux d'artifice et les pétards ;
- la poudre blanche (nitrocellulose), utilisée aussi dans certains propulseurs à réaction ;
- les mélanges « faciles à réaliser » : mélanges à base de produits courants comme le fioul, engrais ou lessive, permettant de réaliser des explosifs artisanaux. Ils peuvent être utilisés au combat en l’absence de matériel plus sophistiqué (guérilla, guerre asymétrique, guerre civile, etc.), ou pour des activités terroristes.
Explosif brisant
Un explosif brisant est un explosif qui applique, lors de son explosion, une pression sur la zone la plus résistante. Un exemple simple : si on place une petite charge d'explosif brisant sur un mur, lors de l'explosion la pression va s'appliquer sur le mur et provoquer la perforation du mur. Au contraire, si on avait placé une charge d'explosif soufflant, le mur n'aurait pas été perforé, mais il y aurait eu un fort effet de souffle dans la direction opposée au mur.
Les explosifs brisants ont une vitesse de détonation qui dépasse 6 050 m/s. Le plus puissant connu (l'octanitrocubane) atteint la vitesse de détonation de 10 100 m/s. On peut citer parmi eux les groupes -nitros et nitrates, les peroxydes organiques, les chlorates et les perchlorates, les halogénures d'azote, les azotures et les fulminates.
Ils sont généralement utilisés dans le domaine militaire ou dans le bâtiment. Pour la pyrotechnie, on préférera les explosifs déflagrants, car les brisants sont trop complexes à manipuler. De plus, ils sont souvent très toxiques et même parfois cancérigènes.
En génie civil, la nitroglycérine, trop instable, est inutilisable sous sa forme liquide courante ; elle a son utilisation la plus répandue en médecine, car c'est un puissant vaso-dilatateur. Les ingénieurs civils lui préfèrent le plus souvent la dynamite, qui est de la nitroglycérine stabilisée par ajout d'un stabilisant (le plus souvent de la cellulose). Au XXIe siècle, les explosifs dits plastiques, composés d'explosif et de gélatinisant (afin de « flegmatiser » la matière active), sont les plus utilisés.
En génie militaire, plusieurs explosifs sont utilisés :
- la mélinite pure (connue sous le nom d'acide picrique ou bien encore de 2,4,6-trinitrophénol) n'est plus utilisée de nos jours, mais sert d'étalon pour donner le coefficient d'utilisation pratique (CUP) d'un explosif, mesurant sa puissance ;
- le TNT ou trinitrotoluène a été largement utilisé pendant la Seconde Guerre mondiale ;
- l'hexolite ou RDX, dont la composition C-4 est un dérivé ;
- l'octolite (usage militaire exclusif) est dans les années 1980 l’explosif le plus puissant ;
- la donarite (nom commercial, de l'allemand Donner, « tonnerre ») est un explosif contenant 70 à 80 % de nitrate d'ammonium, 15 à 25 % trinitrotoluène, et 5 % de nitroglycérine1. Sa vitesse de détonation est de 4 100 m/s. Utilisé par le génie militaire de la Wehrmacht, il est toujours employé dans l'exploitation minière ;
- le tétrytol.
De la poudre d'aluminium est parfois ajoutée au TNT pour augmenter la puissance du souffle (ex. : ammonal).
Par sensibilité
Explosif primaire
En pyrotechnie, un explosif primaire ou initiateur est un produit chimique explosif, celui qui le premier amorce la chaîne pyrotechnique conduisant à l'explosion d'une charge d'explosif.
On les trouve par exemple dans les détonateurs ou les amorces. Ce sont généralement des produits toxiques et dangereux, source de nombreux accidents depuis leur découverte.
Fonctions
Sa vocation peut être d'amorcer la réaction à lui seul, ou de mettre à feu un booster explosif servant de pont entre un explosif de faible énergie et un autre qui possède une grande énergie, mais une réactivité faible.
Toxicologie
Ces produits sont souvent toxiques et toujours dangereux. Ils participent aux séquelles de guerre, y compris séquelles de pollution.
Exemples
Explosif secondaire
Un explosif secondaire est un explosif capable de fournir une très grande quantité d'énergie. C'est le cas par exemple du C3 et du C4.
- Trinitrotoluène (TNT)
- Nitroglycérine…
Cependant un explosif de ce genre est fabriqué de manière à être puissant mais stable dans la mesure du possible. Il a donc besoin d'une énergie d'activation pour exploser. Il est toujours placé après l'explosif primaire qui joue le rôle de détonateur.
L'explosion de cette charge primaire fournit peu d'énergie comparée à la charge secondaire mais suffisamment de chaleur et une onde de choc pour activer cette seconde charge.
Booster explosif
Un booster explosif, ou explosif secondaire, sert de pont entre un explosif de faible énergie et un autre qui possède une grande énergie, mais une réactivité faible.
Il concentre l'énergie d'un explosif primaire de façon à amorcer la réaction du deuxième explosif. Les boosters sont créés en mélangeant des composants de grande réactivité et de grande énergie en proportions variables.
Par exemple, un initiateur (tel un tube explosif) ne possède pas l'énergie d'activation nécessaire pour déclencher la réaction d'une grande quantité d'explosif puissant (tel le PETN, le TNT et l'ANFO), le booster amène l'énergie d'activation nécessaire pour démarrer la réaction chimique.
Le tétryl était populaire au XXe siècle comme booster, particulièrement durant la Seconde Guerre mondiale, mais n'est plus beaucoup utilisé au XXIe siècle, remplacé par des mélanges répondant mieux aux exigences des explosifs modernes.
Ces produits sont souvent toxiques.
Formation et réglementation
Pour des raisons de sécurité des utilisateurs et de lutte contre le terrorisme, la mise en œuvre d'explosifs nécessite de suivre une formation et de respecter la réglementation en vigueur dans le pays8,9,2.
Il faut disposer d'autorisations et être titulaire d'un permis ou d'un certificat. Ces diplômes se préparent lors d'une formation par un organisme agréé. Ils sont obtenus après réussite à un examen.
Il est en général interdit de fabriquer des explosifs. On peut se procurer ces derniers auprès de fabricants qui ne commercialisent que des produits ayant reçu un agrément technique10,11.
L'utilisateur devra aussi respecter les règles concernant le transport et le stockage des explosifs.
Par ailleurs, le code pénal français sanctionne à une peine de trois ans d'emprisonnement et 45 000 € d'amende pour diffusion à un public non professionnel de modes de fabrication d'engins explosifs. La peine peut aller jusqu'à cinq ans d'emprisonnement et 75 000 €, lorsque la diffusion de cette information circule sur un média de type Internet12.
Risques et dangers pour l'environnement ou la santé
Les explosifs agréés sont des produits sûrs, mais peuvent présenter des dangers si des consignes de sécurité ne sont pas respectées lors de leur utilisation :
- activation accidentelle d'éléments sensibles comme les détonateurs à la suite d'un choc, d'une perturbation électromagnétique ;
- certains composants de certains explosifs sont toxiques, et peuvent être source d'intoxication due aux gaz dégagés par l'explosif dans un milieu mal ventilé ;
- intoxication par contact avec la peau en manipulant les produits ;
- périmètre de sécurité non respecté ;
- projection ou déstabilisation de roches et autres matériaux ;
- incident lors d'un tir nécessitant une intervention de l'artificier sur un dispositif endommagé ;
- effet cancérigène ou de perturbateur endocrinien, pour certains explosifs (perchlorates par exemple) ;
- eutrophisation, ou dystrophisation induite par les explosifs riches en azote quand ils sont solubilisés dans l'eau (y compris pour des explosifs modernes très stables dans l'air et réputés peu agressifs envers l'environnement car photodégradables), ou partiellement biodégradables, tels que le dinitramide de guanylurée (Fox-12) ; ce dernier libère dans l'eau une grande quantité d'azote, dont sous forme d'ion nitrate (NO–
3)13,14.
Remarque : les explosifs primaires comme les poudres sont tellement sensibles qu'ils peuvent réagir avec la seule électricité statique générée par le corps humain ou par frottements.
Dangers spécifiques des explosifs faits maison
Les feux d'artifice, explosifs faits maison, ou engin explosif improvisé (EEI), peuvent présenter des dangers pour l'utilisateur lors de leur fabrication, leur transport ou leur utilisation. Certains mélanges sont instables, ils détonent ou s'enflamment spontanément à des températures basses (40 °C), ou lors d'un faible choc, ou après un certain laps de temps. L'opérateur peut être blessé (main arrachée, brûlures, œil crevé, perte de l'audition, intoxication, éviscération partielle) ou tué. Ces engins ou mélanges peuvent provoquer des blessures à d'autres personnes et causer des dégâts matériels importants (parois et vitres soufflées, incendie).
Détection
Des détecteurs électroniques sont peu à peu mis au point, mais on a beaucoup utilisé et on utilise encore le flair de certains animaux comme les chiens, capables de détecter des soupçons de certains produits sous forme d'explosif préparé ou même sous forme de composant primaire (mercure, baryum, chlorates, etc.), non sans risque parfois pour leur santé15.
Plusieurs méthodes (dont par analyse chimique et/ou signature isotopique) permettent de détecter la provenance de certains explosifs ou de leurs composants, dans le cadre d'enquêtes par exemple16.
Notes et références
- U.S. Bureau of Mines, Dictionary of Mining, Mineral, and Related Terms, , CD-ROM.
- Au Canada : Loi sur les explosifs (L.R., 1985, ch. E-17) [archive]
- (en-US) Tom Sharp, « 1846: Guncotton - The book of science » [archive], sur sharpgiving.com (consulté le )
- (en) « Alfred Nobel | Biography, Inventions, & Facts | Britannica » [archive], sur www.britannica.com (consulté le )
- Richard Wolffenstein, « Ueber die Einwirkung von Wasserstoffsuperoxyd auf Aceton und Mesityloxyd », Berichte der deutschen chemischen Gesellschaft, vol. 28, no 2, , p. 2265–2269 (ISSN 0365-9496, DOI 10.1002/cber.189502802208, lire en ligne [archive], consulté le )
- (en-US) « Encyclopedia of Arkansas » [archive], sur Encyclopedia of Arkansas (consulté le )
- (en) Simon Cotton2010-08-18T00:00:00+01:00, « TNT » [archive], sur Chemistry World (consulté le )
- En Suisse : Loi fédérale sur les substances explosibles 941.41 [archive]
- En France : Décret relatif au marquage, à l'acquisition, à la livraison, à la détention, au transport et à l'emploi des produits explosifs [archive]
- Emploi des explosifs, guide pratique (décret du 27 mars 1987), janvier 1995, p. 12.
- En France : Loi Perben II Art. 322-6-1
- « Mort d'un étudiant qui avait fabriqué un engin explosif grâce à Internet » - Société [archive], Le Monde.fr
- Perreault N, Halasz A, Thiboutot S, Ampleman G et Hawari J. (2013), A joint Photo-Microbial Process for the Degradation of the Insensitive Munition FOX-12 (N-guanylurea-dinitramide), Environ. Sci. Technol., 2013-04-17, résumé [archive]
- H Östmark, U Bemm, H Bergman et A Langlet (2002), N-guanylurea-dinitramide: a new energetic material with low sensitivity for propellants and explosives applications, Energetic Materials, Thermochimica Acta, vol. 384, no 1–2, 25 février 2002, p. 253–259, Energetic Materials Department, Swedish Defence Research Agency, FOI, SE-172 90 Stockholm, Suède, DOI:10.1016/S0040-6031(01)00800-0
- Patti Gahagan et Tina Wismer, Toxicology of Explosives and Fireworks in Small Animals, DOI:10.1016/j.cvsm.2011.12.011.
- David Widory, Jean-Jacques Minet et Martine Barbe-Leborgne, Sourcing explosives: A multi-isotope approach, Special Issue: Forensic application of isotope ratio mass spectrometry (IRMS), Science & Justice, vol. 49, no 2, juin 2009, p. 62–72
- Cet article est partiellement ou en totalité issu de l'article intitulé « Explosif primaire » (voir la liste des auteurs).
- Cet article est partiellement ou en totalité issu de l'article intitulé « Explosif secondaire » (voir la liste des auteurs).
- Cet article est partiellement ou en totalité issu de l'article intitulé « Booster explosif » (voir la liste des auteurs).
Articles connexes
- Explosion
- Déflagration
- Détonation
- Séquelle de guerre
- Munition
- Toxicité des munitions
- Risque pyrotechnique
- Fire in the hole
- Engin explosif improvisé
- TM 31-210 Improvised Munitions Handbook
Trinitrotoluène
TNT
Pour les articles homonymes, voir TNT.
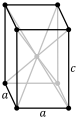
| Trinitrotoluène | |
 |
|
| Structure du trinitrotoluène | |
| Identification | |
|---|---|
| Nom UICPA | 1-méthyl-2,4,6-trinitrobenzène |
| No CAS | |
| No ECHA | 100.003.900 |
| No CE | 204-289-6 |
| Apparence | cristaux incolores à jaunes1 |
| Propriétés chimiques | |
| Formule | C7H5N3O6 [Isomères] |
| Masse molaire2 | 227,131 1 ± 0,008 4 g/mol C 37,02 %, H 2,22 %, N 18,5 %, O 42,26 %, |
| Propriétés physiques | |
| T° fusion | 80,1 °C1 |
| T° ébullition | (décomposition) : 240 °C1 |
| Solubilité | dans l'eau à 20 °C : 0,19 g L−11, soluble dans l'éther, l'acétone, le benzène |
| Masse volumique | 1,65 g cm−31 |
| Pression de vapeur saturante | 0,057 hPa (81 °C) |
| Thermochimie | |
| Cp | |
| Précautions | |
| SGH6 | |
| H201, H301, H311, H331, H373 et H411 | |
| SIMDUT7 | |
  D2B, F, |
|
| Transport | |
| Classification du CIRC | |
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme5 | |
| Écotoxicologie | |
| LogP | 1,601 |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le trinitrotoluène (TNT) est un explosif, utilisé dans plusieurs mélanges, notamment en proportion égale avec le nitrate d'ammonium pour former l’amatol.
Historique
Le TNT a été découvert en 1863 par le chimiste allemand Julius Wilbrand. Son potentiel explosif n'a pu être observé que plusieurs années plus tard, en raison de la difficulté à mettre au point un détonateur efficace, du fait de sa faible sensibilité et de sa puissance modeste en comparaison d'autres explosifs.
Cependant, plusieurs de ses propriétés lui permettent d'être intégré au sein des torpilles et ainsi d'avoir un pouvoir destructeur plus important que les autres explosifs alors utilisés, comme l'acide picrique. L'armée allemande l'adopte en 1902, tandis que les Britanniques l'intègrent progressivement à leur arsenal à partir de 1907.
C'est ainsi que, durant la Première Guerre mondiale, le pouvoir destructeur des torpilles de la marine impériale allemande est plus important que celui des britanniques car elles explosent après avoir perforé la coque, tandis que les torpilles britanniques explosent à son contact et donc dissipent à l'extérieur du bateau une partie de l'énergie dégagée par l'explosion.
Chimie
Le TNT est un composé chimique de type aromatique cristallin.
Il est préparé par nitration du toluène (C7H8). Toute la difficulté de sa synthèse vient du fait que la température nécessaire à son obtention est proche de la température d'explosion du composé binitré (dinitrotoluène) formé intermédiairement. Sa formule est C6H2(NO2)3CH3.
Il existe trois autres isomères trinitrotoluène du TNT (2,4,6-trinitrotoluène) : le 2,3,4-, le 2,3,5- et le 2,3,6-trinitrotoluène.
Explosif
Lors de l'explosion, le TNT peut se décomposer selon différentes réactions :[réf. nécessaire]
- 2 C7H5N3O6 → 3 N2 + 5 H2O + 7 CO + 7 C
et surtout :
- 2 C7H5N3O6 → 3 N2 + 5 H2 + 12 CO + 2 C
ou encore :
- 2 C7H5N3O6 → 3 N2 + H2 + 4 H2C2 + 6 CO2
- C7H5N3O6 → 3 HCN + H2O + 3 CO + CO2
- C7H5N3O6 → HCN + (CN)2 + 2 H2O + 4 CO
- 2 C7H5N3O6 → 6 NO + 5 H2C2 + 2 CO + 2 CO2
- 2 C7H5N3O6 → 6 HCNO + 2 H2C2 + 2 CO + 2 CO2
Un mélange de ces équations est plus probable.[réf. nécessaire]
Sous sa forme raffinée, le trinitrotoluène est relativement stable et moins sensible que la nitroglycérine aux chocs et au transport. Son action explosive doit être amorcée par un détonateur. Il n'interagit pas avec les métaux et n'absorbe pas l'eau, ce qui lui assure une stabilité pour des stockages assez longs, contrairement à la dynamite, mais il peut former des composés instables au contact de métaux alcalins.
L'énergie spécifique de combustion du TNT est de 14,5 MJ/kg, la combustion nécessitant que des atomes de carbone du TNT réagissent avec l'oxygène de l'air. L'énergie de détonation est de 4,184 MJ/kg. Le facteur d'efficacité relative, une mesure de puissance d'un explosif destiné à des démolitions militaires, est utilisé pour comparer l'efficacité massique d'un explosif par rapport au TNT.
On peut remarquer que les explosifs (non-nucléaires) produisent moins d’énergie par kilogramme que des produits alimentaires comme les matières grasses (38 MJ/kg) ou le sucre (17 MJ/kg). De même, la tonne d'équivalent pétrole vaut 41,868 GJ à comparer à une tonne de TNT qui équivaut à 4,184 GJ. On peut noter trois différences essentielles entre ces chiffres :
- les énergies spécifiques de combustion des combustibles ordinaires sont calculées sans tenir compte de la masse d'oxygène nécessaire à la combustion : si l'on en tient compte, il faut diviser le chiffre par plus de quatre pour les matières grasses, et environ deux pour les sucres ;
- la combustion des explosifs nitrés se faisant sans apport d'oxygène atmosphérique, elle est loin d'être complète : la quantité d'oxygène disponible n'est pour le TNT qu'un tiers environ de ce qui serait nécessaire pour une combustion complète ;
- cependant, les explosifs ont des effets bien plus destructeurs, car ils libèrent leur énergie presque instantanément, n'ayant pas besoin d’oxygène externe pour leur combustion.
Unité de puissance explosive
La puissance des bombes, en particulier des bombes atomiques, est souvent désignée par un équivalent en TNT. On utilise alors la « kilotonne » (1 kt de TNT, souvent abrégée simplement par 1 kT, vaut 1 000 t de TNT, soit 4,184 · 1012 J = 4,184 TJ) ou la « mégatonne » (1 Mt TNT, ou 1 MT, vaut 1 000 000 t de TNT, soit 4,184 · 1015 J = 4,184 PJ).
La bombe larguée sur Hiroshima en 1945 avait une puissance d'environ 15 kt, soit 15 000 t de TNT (un cube de TNT de 21 m de côté), ou 62,76 TJ. La bombe H la plus puissante jamais testée — la Tsar Bomba soviétique, le — était équivalente à 57 Mt (un cube de TNT de 325 m de côté), soit 238,488 PJ.
Production
Le complexe militaro-industriel allemand a produit 5 590 t de trinitrotoluène par mois en moyenne en 1939, 7 250 t/mois en moyenne en 1940, 10 560 t/mois en moyenne en 1941, 11 000 t/mois en moyenne en 1942, 16 180 t/mois en moyenne en 1943, 17 280 t/mois en moyenne en 1944, avec un fort déclin à partir de mi-juin dû aux bombardements stratégiques alliés, puis s'effondre début 19458.
La production de ce produit par le complexe militaro-industriel des États-Unis avait cessé en 19869 et a repris en 2005 à la Radford Army Ammunition Plant (en) dans le comté de Pulaski (Virginie)10 de façon plus écologique11. La capacité de production de cette usine, qui est la seule produisant actuellement[Quand ?] du TNT aux États-Unis, est de quinze millions de livres par an (environ 6 800 t).
Toxicité
Beaucoup de terrains militaires sont contaminés par le TNT. Une exposition à de fortes doses peut provoquer des anémies et des maladies du foie. On a également observé des hypertrophies de la rate et des effets négatifs pour le système immunitaire chez des animaux qui avaient ingéré et respiré du trinitrotoluène, ainsi que des irritations cutanées. Les autres effets délétères sont une baisse de la fertilité masculine et un risque cancérigène (c'est un dérivé d'un hydrocarbure aromatique, dont beaucoup de propriétés sont communes avec le benzène, de nature cancérigène). La consommation de TNT noircit l’urine12.
Durant la Seconde Guerre mondiale, la production de TNT pour les besoins de la Wehrmacht fut souvent confiée à des ouvriers étrangers du Service du travail obligatoire, des prisonniers de guerre et des Arbeitsmaid du Kriegshilfdienst dont des malgré-elles. L'un des gros ateliers de production fut l'usine Werk Tanne de Clausthal-Zellerfeld en Basse-Saxe, qui produisait, en 1943-44, 28 000 tonnes de TNT. Les conditions sanitaires y étaient déplorables. Du fait de sa dangerosité, le produit était manipulé manuellement et pénétrait dans l'organisme par la peau ou par les voies respiratoires. Les premiers signes d'empoisonnement étaient la « galle de la poudre » (Pulverkrätze), très douloureuse, suivie par une décoloration en jaune ou roux des cheveux, puis une pigmentation orange de la peau, suivie d'une anémie et d'une leucémie mortelle. Les ouvriers en contact direct avec le TNT étaient surnommés « Canaris », signe qu'ils étaient contaminés par le produit13. Les soins donnés aux malades étaient alors rudimentaires. Les médecins des camps de travail leur servaient du lait comme contre-poison et on badigeonnait quotidiennement le malade d'huile de Mitigal14.
Notes et références
- 2, 4, 6 - TRINITROTOLUENE [archive], Fiches internationales de sécurité chimique .
- Masse molaire calculée d’après « Atomic weights of the elements 2007 » [archive], sur www.chem.qmul.ac.uk.
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C5 to C7, vol. 2, Huston, Texas, Gulf Pub. Co., , 400 p. (ISBN 0-88415-858-6).
- « 2,4,6-trinitrotoluène » [archive], sur ESIS (consulté le ).
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Évaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » [archive], sur monographs.iarc.fr, CIRC, (consulté le ).
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE no 1272/2008 [archive] [PDF], .
- « Trinitro-2,4,6 toluène [archive] » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- (en) Appendix D. Strategic Air Attack on the Powder and Explosives Industries [archive].
- (en) Charles Webb, III, The munitions industrial base: what can we do about it? The Air Force must change its contracting strategy - Agile Combat Support - Industry Overview [archive], Air Force Journal of Logistics, été 2003.
- (en) Radford Army Ammunition Plant [archive], Alliant Techsystems.
- (en) Deborah Elliott, Toxic Red Water Eliminated from TNT Production at Radford [archive], U.S. Army Environmental Command.
- « 🔎 Ammonal - Risque et conseils de prudence » [archive], sur Techno-Science.net (consulté le )
- « http://www.geschichtsatlas.de/~gb31/Die%20Sprengstofffabrik%20Werk%20tann%20in%20claus.htm »(Archive.org • Wikiwix • Archive.is • http://www.geschichtsatlas.de/~gb31/Die%20Sprengstofffabrik%20Werk%20tann%20in%20claus.htm" rel="nofollow" class="external text">Google • Que faire ?).
- Nina Barbier, Malgré-elles : les Alsaciennes et Mosellanes incorporées de force dans la machine de guerre nazie, Paris, Éditions Talandier, , 347 p. (ISBN 979-10-210-3322-1), p. 131-140.
Voir aussi
Articles connexes
- Toluène, benzène avec un groupe méthyle
- Nitrotoluène, toluène substitué par un groupe nitro
- Dinitrotoluène, toluène substitué par deux groupes nitro
- Trinitrobenzène
- Dynamite
- Liste de composés explosifs
Composition C-4
Pour les articles homonymes, voir C4.
Le C-4, composition C-4 ou C-45010A, est une variété d'explosif de la famille des plastics. Elle est utilisée principalement par l'armée et par des entreprises de démolition. Elle fait partie de la famille d'explosifs dits de composition C.
Description
Le C-4 est composé d'un explosif, d'un liant plastique, d'un plastifiant, d'un produit pétrolier et, depuis 2006, d'un marqueur chimique pour faciliter sa détection et identifier le fabricant. Comme plusieurs explosifs de la famille des plastics, l'explosif est principalement composé de RDX, qui constitue environ 91 % de la masse du C-4. L'agent plastifiant est de l'adipate ou le sébaçate de bis-2-éthylhexyle (5,3 %) et le liant est du polyisobutylène (2,1 %). Un autre agent liant possible est l'adipate de dioctyle (DOA). Une petite quantité de pétrole (1,6 % d'huile moteur SAE 10 sans détergent) est aussi ajoutée.
Le C-4 est fabriqué en combinant le RDX sous forme colloïdale au liant. Ce mélange est dissous dans un solvant, qui est évaporé par la suite. Le résultat est alors séché et filtré. Sous sa forme finale, le C-4 est de couleur blanc cassé et a une texture qui rappelle l'argile à modeler.
L'avantage principal du C-4 est qu'il peut prendre n'importe quelle forme. Il est facile à presser à l'intérieur d'un vide, que ce soit une lézarde dans un immeuble, un récipient d'une machine-outil ou un objet à emporter. Il est aussi reconnu pour sa durabilité et sa stabilité. Il n'explosera pas s'il est percé, coupé, frappé par une balle ou lancé dans un feu. La seule façon certaine de le faire détoner est d'utiliser un détonateur ou un explosif primaire (c'est-à-dire un explosif peu puissant, mais très sensible, qui amorce la détonation). S'il est pressé et chauffé, le C4 n'explose pas1.
Les Britanniques ont produit un explosif semblable qu'ils désignent par le terme de PE4. La seule différence connue est le type et la quantité de plastifiant utilisé.
Le C-4 appartient à la famille des explosifs dont les membres s'appellent C, C-2 et C-3, chacun contenant une quantité différente de RDX. Sa puissance équivaut à 118% celle du TNT.
Historique
Le C-4 a été créé en 1956, il s'agit d'une amélioration du Nobel 808 développé initialement par les Britanniques lors de la Seconde Guerre mondiale. Le Nobel 808 contenait du RDX, de l'huile minérale et de la lécithine.
Anecdotes
- Pendant la guerre du Viêt Nam, des soldats allumaient de petites quantités de C-4 pour réchauffer leurs rations lors de longues patrouilles. En effet, soumis à une forte température, le C4 brûle lentement au lieu d'exploser (mais les fumées sont très toxiques).
Notes et références
Voir aussi
Article connexe
Lien externe
- (en) Description [archive]
Dynamite
Pour les articles homonymes, voir Dynamite (homonymie).
A. Sciure (ou tout autre type de matériau absorbant) trempée dans de la nitroglycérine ;
B. Revêtement de protection entourant la matière explosive ;
C. Détonateur ;
D. Câble électrique connecté au détonateur.
La dynamite est un explosif fabriqué avec de la nitroglycérine. Elle est 1,25 fois plus puissante que le trinitrotoluène (TNT)1. Découverte par Alfred Nobel en 1866, la dynamite a été très utilisée, notamment dans l'industrie minière, jusqu'à son remplacement par des explosifs plus puissants et plus faciles à manipuler, comme ceux de la famille des plastics.
Étymologie
Le nom de la dynamite vient du mot grec δύναμις (dunamis ou dynamis), qui signifie « puissance », « pouvoir », auquel a été ajouté le suffixe suédois -it.
Histoire
La nitroglycérine est d'abord fabriquée et vendue par la société d'Alfred Nobel sous sa forme liquide. Mais elle est tellement instable et dangereuse (Emil Oskar Nobel (en), le frère d'Alfred, et d'autres personnes meurent d'une explosion durant la préparation de la nitroglycérine en 18642) qu'elle est rapidement interdite en Europe. La production artisanale de nitroglycérine se fait dans les mines, cependant comme toute fabrication artisanale d'explosifs, les accidents sont fréquents (réactions réalisées à température ambiante et non à 0 °C).
Alfred Nobel résout le problème par sérendipité en la mélangeant à des kieselguhrs (poudre fossile de diatomées), puis en la moulant sous forme de bâtonnets enveloppés de papier, c'est ainsi qu'est créée la dynamite en 1866. Elle fait l'objet d'un brevet d'invention du en Angleterre et du en Suède3. Il s'agit du premier explosif puissant, peu coûteux à produire et stable (c'est-à-dire ne présentant que peu de risques d'explosion accidentelle lors du transport).
La nitroglycérine peut également être mélangée à d'autres composants neutres, comme la silice, ou à des composés actifs (soufre, nitrate de sodium, cellulose, etc.).
L'exploitation de son brevet rapporte à Alfred Nobel une fortune considérable, qui est plus tard dévolue aux Prix Nobel. Il contrôle strictement ses droits et réussit à les faire valoir face à des marchands américains qui tentent de plagier son invention en utilisant une formule légèrement différente.
Bâton de dynamite
Un bâton de dynamite a classiquement les dimensions suivantes : 25 cm de longueur sur 3 cm de diamètre, mais la grande majorité de la dynamite est utilisée sous forme de cartouches de diamètre supérieur à 5 cm et d'un poids supérieur à 1 kg.
À l'origine, le bâton de dynamite est composé de 75 % de nitroglycérine (corps très instable) et de 25 % de kieselguhr (micro-algues) qui stabilise la nitroglycérine et fait de la dynamite un explosif plus sûr.
La dynamite est d'utilisation beaucoup moins risquée que la nitroglycérine ou même que la poudre à canon. Elle est moins sensible aux chocs, et un bâton placé dans un feu brûlera (théoriquement) sans exploser. De fait, elle nécessite un détonateur pour être utilisée.
Avec le temps (ou à une température supérieure à 32 °C), les bâtons de dynamite suintent de la nitroglycérine liquide, ce qui peut les rendre dangereux et pose un problème de sécurité sur les chantiers. C'est pourquoi elle est moins utilisée de nos jours.
Les dynamites actuelles, dont le principe est là encore basé sur une invention de Nobel, contiennent un peu de coton azotique (nitrocellulose) qui gélifie la nitroglycérine et supprime les suintements. La nitroglycérine est remplacée jusque 50 % par du nitroglycol, ce qui abaisse le point de congélation du mélange et le rend plus sûr, car une dynamite gelée est très sensible aux chocs. Le kieselguhr est remplacé par un mélange de farine de bois ou similaire, et de nitrate d'ammonium, qui augmente la puissance du produit.
Usages
Les principaux domaines d'utilisation de la dynamite ont été la construction, l'exploitation minière et la destruction. De plus, elle a eu des applications dans la guerre et le terrorisme. Durant l'industrialisation, il y eut un important besoin de puissants explosifs pour l'industrie minière ou la construction de tunnels. Cependant, de nouveaux explosifs et de nouvelles techniques ont peu à peu remplacé la dynamite. Cela fait des décennies qu'elle n'a plus été commercialisée.
Terrorisme
L'invention de la dynamite a mis entre les mains des terroristes une source d'énergie presque inimaginable dans ses dimensions. Un périodique espagnol populaire de 1908 captura cette image lorsqu'elle décrivait les attributs et le pouvoir de la dynamite : « Sa force irrésistible, sa formidable puissance. Il semble que l’esprit de Shiva, le dieu de la destruction, destructeur éternel de la vie, réside dans les profondeurs de sa composition étrange. Tous les grands phénomènes de la nature lui ressemblent par leurs effets : […] il crée et détruit, anéantit et donne vie; il est enchaîné Prométhée et Jupiter en colère; il illumine et assombrit. De nécessité de la civilisation, il devient son châtier […] il est devenu un anathème social, dans l’arme terroriste des sectes dissidentes. »4
Anarchistes
La dynamite était une arme très associée aux anarchistes de la fin du XIXe siècle. Le schisme entre le mouvement marxiste et anarchiste en 1872 après le cinquième congrès de la Première Internationale coïncide avec la popularisation de la dynamite. Elle représentait une technologie moderne et puissante qui pouvait être utilisée afin d'atteindre leurs buts. Johann Most, un anarchiste, a affirmé que la dynamite contenait le pouvoir de détruire le régime capitaliste tout comme la poudre à canon et le fusil contenant le pouvoir de supprimer le féodalisme de la surface de la Terre5.
La dynamite est l’outil idéal pour implémenter la propagande par le fait, qui cherchait à être le plus visible possible et à démontrer la révolution par des actes violents. L’intention est donc de causer plus de peur que de mal, ainsi la dynamite est préférée aux armes blanches et aux armes à feu6. Un exemple est le cas d’Auguste Vaillant qui, en 1893, a lancé une bombe dans la Chambre des députés afin de protester contre les conditions misérables dans lesquelles il vivait en tant qu'ouvrier pauvre. L’acte ne visait pas à tuer et seules quelques personnes furent blessées. Le , il fut exécuté et fut décrit comme « la première personne de la France du XIXe siècle à être exécutée, même s'il n'a tué personne. »7
Ainsi, par son efficacité à mettre en actes la propagande par le fait, la dynamite devient une signature idéologique; tout attentat à la dynamite est rattaché aux mouvements anarchistes sans qu’aucune revendication ne soit faite6.
L'aspect de la destruction non ciblée de la dynamite convenait également aux anarchistes. L’objectif de frapper contre le régime bourgeois « corrompu et criminel », vise une classe entière de personnes et ainsi tout membre de cette classe est une cible possible. « Il n’y a pas d’innocents », a déclaré l’anarchiste français Émile Henry à la cour qui l’interrogeait à propos de la bombe lancée le dans un café8.
Entre février et mai 1885, une enquête sur les activités anarchistes est menée par les autorités judiciaires suisses. La cause étant une série de lettres anonymes, finalement dévoilées comme incorrectes, prétendant qu’un groupe d’anarchistes complotait pour faire exploser la Palais fédéral à la dynamite. Aussi, l’Allemagne et l’Italie mettaient pression sur la Confédération suisse pour mettre fin aux activités dites terroristes des anarchistes séjournant en Suisse. En effet, par sa position géographique et sa réputation de terre d’asile, la Suisse était la destination choisie par de nombreux réfugiés politiques, la Confédération comptait des représentants de presque tous les mouvements révolutionnaires de l'Europe. La responsabilité de mener les enquêtes est placée sur les autorités cantonales qui manquaient de ressources, que ce soit monétaire ou d’agents suffisamment formés, et qui ne travaillaient qu’à l’échelle cantonale sans regarder la situation générale de la Confédération. De plus, le public et les autorités avaient une grande réticence à l’idée de la surveillance politique qui est opposée aux principes de démocratie et liberté qui étaient fortement liés au sentiment national. Par cette démarche, des fautes ont été commises, par exemple, la poursuite d'un train que l'on soupçonne de transporter de la dynamite alors qu'il s'agissait de tabac. Une fois l’affaire close, la formation d'un bureau central chargé de réunir des informations sur les étrangers subversifs fut mandaté. Cet événement fut ainsi un tournant dans la professionnalisation de la surveillance politique, même s’il n’a mené qu’à l’expulsion de quelques anarchistes9,10.
La dynamite comme arme d’assassinat contre Alexandre II
A la fin du XIXe siècle en Russie, la dynamite a été utilisé par divers groupes révolutionnaires cherchant à renverser le système autocratique et à arrêter les réformes gouvernementales du Tsar Alexandre II de Russie. Par exemple, un groupe révolutionnaire socialiste/nihiliste Narodnaya Volya (Volonté du Peuple), formé en 1879 sont devenus le premier groupe terroriste anarchiste à utiliser largement la dynamite.
En septembre de la même année, les révolutionnaires Véra Figner, Nikolaï Kibaltchitch et Mikhail Frolenko sont venus à Odessa avec des explosifs passés en contrebande depuis la Suisse11, afin de faire exploser le train impérial en novembre 1880, alors qu'il transportait le Tsar de Livadia à Saint-Pétersbourg. Ils ont fabriqué les fusibles, séché la pyroxyline et testé le mécanisme explosif. La dynamite était extrêmement sensible et explosait souvent d'elle-même, tuant les « dynamiteurs ». Le nom « dynamiteur », un nouveau mot pour l'époque, était donné aux personnes utilisant des explosifs contre l’état11. Une fois l’attentat planifié et les bombes fabriquées, de la dynamite a été placée sur les rails. Normalement, le train du Tsar voyageait 30 minutes derrière le train qui transportait le personnel mais dans ce cas, le train du Tsar devançait celui-ci car il avait eu une défaillance mécanique. Les bombes n’ont donc affecté que le train du personnel et le Tsar s’en sortit indemne11.
Une autre tentative du même groupe a été faite au Palais d'Hiver avec l'aide de Stepan Khalturin. En 1880, il a obtenu un emploi de charpentier au Palais d'Hiver lui permettant de dormir sur place ; ceci lui a permis d'apporter des paquets de dynamite chaque jour, les cachant dans sa literie. Il a ainsi placé un total de près de trois cents livres de dynamite sous la salle à manger12. Il était prévu de faire exploser la bombe le soir du [O.S. 5 février] 1880, afin d’assassiner la famille impériale. Mais un invité arrivant de Berlin avait du retard, et pour la première fois depuis des années, le dîner a dû être retardé12. Alors que la famille quittait le salon pour aller vers la salle à manger, la bombe a explosé. La salle à manger a été complètement démolie et onze membres de la garde finlandaise qui se trouvaient dans la salle des gardes juste en dessous furent tués ainsi que trente autres blessés13.
Le 13 mars 1881, la Volonté du Peuple a fait une autre tentative d’assassinat à l’aide de la dynamite, attaquant alors que le Tsar parcourait une route qu’il fréquentait régulièrement les dimanches. La première lancée de dynamite n'a endommagé que le chariot et quelques piétons. Le Tsar n'a pas été blessé, mais il quitta son chariot pour aider les blessés, ignorant qu'il y avait trois autres terroristes sur place. Ignati Grinevitsky, a attendu le passage d'Alexandre et a jeté une bombe à ses pieds. L'explosion l'a tué et a laissé Alexandre II mortellement blessé. Grinevitsky est donc considéré comme le premier auteur d’un attentat suicide14,15. Alexander II fut alors transporté jusqu'à son bureau au Palais d'Hiver, où il est décédé une heure plus tard.
La Volonté du Peuple a utilisé de la dynamite à la gélatine pour toutes ses tentatives d'assassinat, même si le pistolet conventionnel était meilleur marché et plus facilement disponible, et avait probablement plus de chances de succès. Ces révolutionnaires pensaient que la dynamite avait un bien plus grand impact psychologique : il exemplifiait « une nouvelle étape dans le mouvement révolutionnaire » plutôt que d'être « interprété comme un meurtre ordinaire. »4
La dynamite comme arme d’assassinat contre Guillaume Ier
Une tentative d'assassinat a eu lieu à Niederwald contre le kaiser allemand en septembre 1883, tentant de faire exploser non seulement Guillaume Ier et le prince héritier Frédéric, futur Frédéric III, mais aussi de nombreux généraux et aristocrates du gouvernement. Toutes ces personnalités devaient assister à l'inauguration d'un grand monument symbolisant la Germanie surplombant le Rhin. Mais un fusible mouillé qui n'a pas réussi à allumer seize livres de dynamite placé dans un tuyau de drainage a déjoué la tentative des anarchistes4. Dans un effort ultérieur, ils ont fait sauter une salle de concert presque vide dans la ville voisine de Rudesheim en supposant à tort que l'empereur allemand avait prévu cet endroit pour une visite.
L'échec de la tentative de Niederwald a illustré certains des problèmes pratiques liés à l'utilisation de la dynamite. Bien que la dynamite ait conservé pendant cinquante ans sa réputation parmi les anarchistes, les révolutionnaires et le public en tant qu'arme miracle de destruction, un fossé existait entre le puissant symbole et la réalité mondaine. La dynamite était beaucoup plus puissante que les explosifs précédents, mais en pratique, elle s'est souvent révélée moins meurtrière et plus lourde que prévu. La plupart des manuels sur les explosifs étaient inexacts et les tentatives des amateurs de concocter des bombes à dynamite se soldaient souvent par des explosions prématurées. Même lorsque les terroristes ont volé ou acheté de la dynamite produite commercialement (ce que la plupart recommandaient par rapport à ces recettes maison), des quantités énormes étaient souvent nécessaires pour garantir le succès4.
Tunnel ferroviaire du Saint-Gothard
Un autre exemple concret de l’utilité de la dynamite est lors de la construction du tunnel ferroviaire du Saint-Gothard en Suisse. Construit entre 1872 et 1881, long de 15 km, le tunnel posait de nombreux défis aux ingénieurs qui l’ont conçu. La poudre noire était insuffisante pour sa construction à cause de la grandeur du projet16, mais la dynamite, qui avait été inventée seulement six ans auparavant, le rendit possible : au lieu de devoir percer 80 trous dans la montagne pour ensuite les remplir avec de la poudre à canon pour créer un bout de tunnel, il suffit d’en creuser 24 lorsqu’on utilise la dynamite, ce qui permettait de faire le même travail en un tiers du temps16. Pour satisfaire les demandes énormes en dynamite, deux usines ont été créées, une à Isleten au nord du Gothard et une autre à Ascona, au sud. Celles-ci étaient les deux premières usines de dynamite en Suisse.
À Isleten, la population était incommodée par la construction de l’usine. Lors des réunions communales le 2 juin et le , ils ont porté plainte contre la démarche, citant des raisons de sécurités16. Le public était assuré que les dangers étaient gérables, et le , les fondateurs — entre autres Alfred Nobel — ont commencé formellement la construction de la « Schweizerische Dynamit- & Chemische Producten-Fabrik » (Usine de Dynamite & Produits Chimiques Suisse)16. Afin de garantir la sécurité, diverses précautions sont prises : l’usine est située loin des habitations et de nombreuses protections contre des explosions accidentelles sont installées16. Par exemple, le mélange de la nitroglycérine et du kieselguhr se fait dans des cabanes en bois, situées dans un trou de trois mètres de profondeur et entourées d’un mur de terre faisant six à sept mètres de haut mesuré depuis le fond ou se trouve la cabane. Malgré tout, un accident d’explosif a tué trois ouvriers le 16.
L’usine a produit 200 tonnes de dynamite par année pendant la construction du tunnel ferroviaire, représentant alors une partie important de l’économie du canton d’Uri16.
Autres usages
La dynamite a aussi été utilisée dans des conflits armés, notamment dans la guerre franco-allemande de 1870.
Il est arrivé que des criminels intéressés par l'ouverture de coffres-forts aient délibérément extrait de la nitroglycérine de bâtons de dynamite en les faisant bouillir.[réf. souhaitée]
Les spéléologues ont longtemps utilisé de la dynamite pour pratiquer la désobstruction des conduits et chatières non-pénétrables par l'Homme. Petit à petit, la pratique s'est orientée vers des explosifs plus intéressants d'un point de vue rapport puissance/volume.
La pêche à la dynamite est une méthode de pêche, de nos jours illégale, consistant à bombarder une zone de mer avec de la dynamite. L'onde de choc provoquée par la détonation provoque la mort des poissons aux alentours qui remontent à la surface et le pêcheur n'a plus qu'à les ramasser.
Notes et références
- « Les explosifs non-nucléaires les plus puissants » [archive], sur records-du-monde.com (consulté le ).
- (en) « Alfred Nobel - Timeline » [archive], sur Nobelprize.org (consulté le ).
- (de) Phokion Naoúm, Nitroglycerin und Nitroglycerinsprengstoffe, Springer-Verlag, , p. 8.
- (en) Jensen, R., Daggers, Rifles, and Dynamite: Anarchist Terrorism in Nineteenth Century Europe, Northwestern State University Press, , p. 129-130.
- Hunter R. (1916), Violence and the Labour Movement, Macmillan, p. 66-68.
- Ivianski Z. (1977), Individual Terror: Concept and Typology, Journal of Contemporary History, vol. 12, p. 43-63.
- Merriman J.M. (2016), The Dynamite Club. How a Bombing in Fin-de-Siècle Paris Ignited the Age of Modern Terror, Yale University Press.
- Piarotas M. (2000), Regards populaires sur la violence, Publications de l’Université de Saint-Étienne, p. 127-142.
- Ferretti F. et Minder P. (2015), Pas de la dynamite, mais du tabac. L'enquête de 1885 contre les anarchistes en Suisse romande, Éditions du Monde Libertaire.
- Association pour l'étude de l'histoire du mouvement ouvrier (1992), Cent ans de police politique en suisse, 1889-1989, Éditions d’En-bas, p. 33-38.
- Edvard Radzinsky (1993/2005), Alexander II The Last Great Tsar, New York, Free Press, p. 315-319.
- Edvard Radzinsky (1993/2005), Alexander II The Last Great Tsar, New York, Free Press, p. 329-335.
- Virginia Cowles (1971), The Romanovs, Harper and Row.
- Pomper, P. (2008), Aleksandr Ul'ianov: Darwinian Terrorist, Russian History, 35 (1/2), 139–156.
- Bennett, Brian T. (2007), Understanding, Assessing, and Responding to Terrorism: Protecting Critical Infrastructure and Personnel, Wiley-Interscience.
- Burkhardt Hansjakob (2012), Dynamit Am Gotthard - Sprengstoff in der Schweiz. Eine Geschichte der Sprengstoffindustrie in der Schweiz am Beispiel von Isleten am Urnersee. hier + jetzt, Verlag für Kultur und Geschichte. p. 24-56.
Voir aussi
Articles connexes
- Trinitrotoluène (TNT)
- Titadine
- Dynamiterie de Paulilles
- Paul Barbe, premier fabricant associé à Nobel
Poudre noire
Ne doit pas être confondu avec Gunpowder.
La poudre noire, parfois dénommée poudre à canon ou poudre à fusil, est le plus ancien explosif chimique connu. De couleur noire, elle est constituée d'un mélange déflagrant de soufre, de nitrate de potassium (salpêtre) et de charbon de bois.
Inventée en Chine probablement vers le IXe siècle, la poudre noire s'est progressivement diffusée en Europe et en Asie jusqu'au XIIIe siècle. Utilisée pour les canons et les fusils, c'était le seul explosif chimique connu jusqu'au XIXe siècle. La poudre noire n'est plus utilisée de nos jours pour les armes modernes et pour les applications industrielles, en raison de sa faible efficacité comparée à celle des explosifs plus récents. Son usage est aujourd'hui limité à des armes anciennes de chasse et de tir sportif (armes authentiques ou répliques), aux pétards et aux feux d'artifice.
Historique
Certaines sources situent l'invention de la poudre noire durant la dynastie Han (206 av. J.-C. à 220 ap. J.-C), mais la plupart des historiens pensent que la poudre à canon fut inventée en Chine vers le VIIe siècle, durant la Dynastie Tang (618-907). En chinois, la poudre à canon est désignée par le terme Huoyao (chinois : 火药 ; pinyin : ; litt. « substance à feu ») et est d'abord utilisée pour ses propriétés médicinales.
Au milieu de la dynastie Xixia, vers 1044, il est conseillé d'éviter ce type de mélange qui risque d'exploser. Le Wujing Zongyao (武经总要, « Principes généraux du classique de la guerre ») donne une méthode de fabrication de grenades à poudre noire, dont l'effet principal semble encore être le bruit. Au Xe siècle, apparaissent les premières lances de feu, au départ de simples tubes de bambou contenant de la poudre noire et un projectile, dispositif fixé sur une lance chinoise (Qiang). Il semble qu'aux alentours de 1130, des tubes de bambou remplis de poudre noire servirent de lance-flammes.
Les techniques de fabrication de la poudre auraient été transmises au monde arabo-perse entre le VIIIe siècle et le IXe siècle, car des échanges de techniques d'alchimie existaient déjà entre le monde musulman et le monde chinois1. Cependant l'usage « connu » de la poudre semble plutôt dater du XIIIe siècle, avec des mentions écrites de composition à base de salpêtre, lors des guerres entre la dynastie Yuan et les pays musulmans d'Asie centrale. On a longtemps dit que la poudre noire était arrivée en Europe au milieu du XIIIe siècle par l'intermédiaire de la civilisation islamique (et parfois, au mépris des attestations historiques, que Marco Polo l'avait rapportée de son voyage en Extrême-Orient[réf. nécessaire]) ; en fait, il semble que les Mongols aient joué un rôle déterminant.
À partir du XIVe siècle, la poudre noire est utilisée pour animer les spectacles équestres du Maghreb organisés par les tribus marocaines.
Roger Bacon et Albert le Grand en mentionnent la recette, en s'inspirant de celle donnée par Marcus Graecus dans son manuscrit Liber ignium ad comburandos hostes (1230)2, mais le but en reste incendiaire. Selon d'autres sources, le moine allemand Berthold Schwarz est considéré comme celui qui redécouvrit ses secrets en Occident. Ibn Khaldoun mentionne un usage de la poudre pour l'artillerie en 1273 au siège de Sidjilmesa. Les premières armes à feu utilisables apparaissent environ cinquante ans plus tard.
C'est en 1617 qu'est attestée la première utilisation de la poudre noire en Europe pour l'extraction de minerais dans une mine de cuivre du Thillot3 grâce aux travaux archéologiques menés par la Société d'étude et de sauvegarde des anciennes mines (SESAM) depuis 1987 dans ces mines.
En 1829, Samuel Colt est le premier à faire déflagrer une charge de poudre sous l'action d'un courant électrique.
En 1886 est inventée la poudre pyroxylée, qui dégage beaucoup moins de fumée et peu de résidus lors de sa combustion. Cette poudre est aujourd'hui utilisée dans toutes les armes contemporaines, car la quasi absence de résidus ne les encrasse pas.
Aspects chimiques
Aux XIVe siècle et XVe siècle, la composition était (en masses) : 6 parties de salpêtre (75 %) pour une partie de soufre (12,5 %) et une partie de carbone sous forme de charbon de bois (12,5 %). Mais ultérieurement, on trouve des compositions variables selon les usages.
Par exemple (pourcentages massiques) :
- 30 % de charbon, 30 % de soufre, 40 % de salpêtre pour la poudre de mine (lente) ;
- ou bien 12 % de charbon, 10 % de soufre, 78 % de salpêtre pour la poudre de chasse et les poudres françaises PNF destinées au tir sportif ;
- ou encore 15 % de charbon, 10 % de soufre, 75 % de salpêtre pour la poudre dite de guerre f3 ;
- ou alors 12 % de charbon, 12 % de soufre, 76 % de salpêtre pour les poudres suisses destinées au tir sportif.
Dans les pièces d'artifices, on trouve généralement la composition (charbon 15 %, soufre 10 %, salpêtre 75 %). Cette poudre est un mélange de deux éléments très combustibles (le soufre et le charbon), avec un corps très oxydant : le salpêtre. La qualité de la poudre est due en grande partie au charbon utilisé. Il provient du bois d'arbres des plantes telles que Rhamnus Frangula, Solanum Mauritianum, Prunus domestica, Salix Caprea ou Fraxinus americana ; par pyrolyse à 500 °C, on obtient du charbon noir (poudre de guerre), tandis que la pyrolyse à 300 °C donne du charbon roux (poudre de chasse).
Pour que la combustion se déroule efficacement, le soufre et le charbon doivent être broyés en poudres fines (moins de 80 nanomètres), avant de le mélanger avec un moulin à billes. Par la suite, un mélange de nitrate de potassium et d'alcool est ajouté et le tout est mélangé dans un mélangeur pour obtenir un mélange très homogène. Enfin, le mélange est séché à basse température et doucement réduit en poudre à l'aide d'un pilon. On obtient une poudre noire qui brûle comme un flash.
La poudre noire craint beaucoup l'humidité, contrairement à ses descendantes modernes (poudres pyroxylées).
La poudre noire, contenant du salpêtre, a un goût salé en raison de ce constituant (nitrate de potassium KNO3). Pendant les différents conflits européens de la fin du XVIIIe et du début du XIXe siècle, les soldats utilisaient de la poudre noire pour assaisonner et conserver leurs aliments lorsque le sel venait à manquer. Le salpêtre est encore utilisé de nos jours comme conservateur (on en trouve dans la charcuterie par exemple).
L'équation de la combustion de la poudre à canon (charbon 15 %, soufre 10 %, salpêtre 75 %) est la suivante :
- 10 KNO3 + 4 S + 2 C7H3O → 5 K2O + 3 H2O + 4 SO2 + 12 CO + 2 CO2 + 5 N2
Les résidus solides sont appelés « calamine ».
Aspects physiques
Parmi les avantages de la poudre noire, notons qu'elle est peu onéreuse, stable et qu'une faible quantité d'énergie en provoque la combustion. Ainsi, peut-on l'enflammer à l'aide d'une flamme, d'une friction, d'une étincelle, ou même d'un laser. Il en résulte que sa manipulation est dangereuse.
Elle produit :
- d'abondants résidus solides, surtout composés de sulfure de potassium, abusivement nommée calamine, qui encrassent les armes. C'est l'une des raisons pour lesquelles une arme à feu ancienne présente un fort calibre qui augmente la tolérance donc réduit la fréquence des nettoyages nécessaires ;
- de la fumée, gênant la visée lors des tirs répétés si le vent ne la chasse pas.
Pour ces raisons, on lui préfère aujourd'hui la poudre sans fumée.
Au cours du XIXe siècle, les chimistes mirent au point un procédé permettant d'obtenir de la poudre noire en grains, dont la taille peut être modulée selon l'usage prévu : plus les grains sont petits, plus la poudre obtenue est dite « vive », c'est-à-dire qu'elle présente une vitesse de combustion élevée. Ce conditionnement permet également de mieux conserver et de mieux doser la poudre noire.
Aspects thermodynamiques
La poudre noire contient à la fois un combustible et un comburant. Le comburant est le salpêtre qui libère de l'oxygène au cours de la réaction, venant oxyder les combustibles (soufre et carbone).
Stable à température ambiante, un petit apport d'énergie localisé suffit à amorcer la réaction.
Du fait de sa vitesse de combustion à l'air libre, on dit que la poudre noire « déflagre », ce qui signifie que l'onde de combustion (front de flamme) se déplace moins vite que les gaz générés, ne produisant donc pas d'onde de choc. Placée dans un endroit confiné qui permet une élévation de la pression des gaz, elle détone (génération d'une onde de choc) et produit un effet de souffle assez important en raison du volume de gaz produit.
Considérée comme un explosif à effet de souffle, par opposition aux explosifs à effet brisant, elle a longtemps été utilisée à cette fin.
La température de la réaction est assez élevée (plus de 2 000 K) mais reste nettement inférieure à celle obtenue avec des explosifs modernes (TNT, dynamite, poudres pyroxylées), limitant les risques de brûlures. L'ajout de certains composés chimiques ou de corps simples (particules métalliques, oxydes, etc.) permet de modifier la couleur de la flamme obtenue pour les feux d'artifice par exemple. La fumée dégagée par la réaction chimique est blanche, assez dense, en raison de nombreuses particules issues de la combustion.
Étapes de fabrication
Lors de son élaboration, la poudre noire suit un protocole précis, pratiquement identique dans les différents pays de production. En France, et plus particulièrement à la poudrerie de Vonges (21), le protocole est le suivant :
Les éléments entrants dans la fabrication de la poudre noire sont stockés séparément. Le charbon de bois issu de la bourdaine produit en Europe, arrive en vrac. Il est stocké dans des poches en tissu (coton) dans un hangar chauffé l’hiver et ventilé l’été pour obtenir le meilleur séchage possible. Le soufre et le salpêtre importés très souvent du Mexique et du Chili, sont livrés en sacs (papier ou polyester) de 25 kg. Dans la composition de certaines variétés de poudres noires, il y est ajouté quelquefois du lignite importé régulièrement d’Allemagne, en quantité précise.
Tonnes binaires
Dans un premier atelier nommé « tonnes binaires » (tonneaux en acier de 2 m de Ø et 2 m de hauteur équipés d’une porte d’accès, placés horizontalement sur un axe rotatif contenant un poids précis de billes en bronze pur d’environ 2 cm de Ø, entraînés par des courroies), le charbon de bois et le soufre sont malaxés ensemble. L’atelier est équipé d’un nombre variable de « tonnes », généralement une dizaine.
Après plusieurs heures de pulvérisation des composants, les tonnes sont vidées sur un tamis très fin et leur contenu stocké dans des étouffoirs (tonneaux en matière plastique).
Remarque importante : à partir de l’étape de fabrication suivante, tous les ateliers dans lesquels les préparations seront traitées ou entreposées seront soumis à des règles de sécurité drastiques afin d’éviter tous risques de surchauffe, d’étincelle, etc. (port de sabots en caoutchouc, sols en asphalte le plus souvent maintenus mouillés, utilisation d’outils en bronze, en bois ou en aluminium, interdiction formelle de fumer ou d’utiliser une flamme nue, etc.). La sécurité des employés est primordiale.
Préparations
Dans cette deuxième phase, le produit arrivant des tonnes binaires est mélangé au salpêtre, en respectant des poids très précis suivant la variété de poudre à fabriquer. Une certaine humidité est observée à ce mélange en y ajoutant un peu d’eau. Tout en restant compact, le mélange est entreposé dans des bacs plastiques individuels de 15 à 25 kg.
Ces bacs sont entreposés dans un hangar fermé attenant aux ateliers des préparations.
Meules
Le mélange provenant de l’atelier des ateliers des préparations entre dans sa troisième phase de fabrication. Entre 120 et 200 kg de matière, sont déposés sur une piste en fonte sur laquelle tournent autour d’un axe entraîné par courroies, deux meules en fonte également, d’environ 1,50 m de Ø, pesant plusieurs tonnes (voir photo ci-contre).
Le mélange, malaxé 30 à 50 min par les meules, est sorti en plusieurs morceaux de poids variables (galettes). Ces morceaux (galettes) sont répartis dans les bacs provenant des ateliers des préparations et entreposés dans un autre hangar dédié, fermé, attenant aux ateliers des meules.
Grenoirs
Les galettes provenant des ateliers des meules entrent dans la quatrième phase de fabrication. Environ 100 kg de galettes sont déposés dans une tonne grenoir (sorte de tonneau fait de deux disques en bois cerclé de bronze, de 1,5 m de Ø dont un est équipé d’une porte d’accès à son centre, placés horizontalement sur un axe rotatif à 1 m d’écart, équipés sur leurs circonférences d’un grillage quadrillé en inox les reliant entre eux, entraînés par des courroies). Un poids précis de boules de bois (gaïac) d’environ 10 cm de Ø, sont placées dans ce tonneau. Sous l’effet des boules bondissantes lors de la rotation, les galettes sont cassées en de nombreuses particules qui passent au travers d’une toile tamis (en nylon) de différentes grosseurs selon la variété de poudre fabriquée. Ces grains sont récupérés à l’extrémité du tamis et entreposés dans des sacs de toile (coton).
Lorsque la tonne grenoir est vidée de son contenu, elle est de nouveau approvisionnée de galettes. Cette phase dure de 40 min à plus d’une heure.
Les grains fabriqués avec les galettes provenant des ateliers des meules, sont entreposés en sacs dans un autre hangar dédié, fermé, attenant aux ateliers des grenoirs.
Lissoir
La poudre constituée des grains fabriqués dans les ateliers grenoirs, arrive dans sa cinquième phase de fabrication. Plusieurs centaines de kilos de poudre sont déposés dans une tonne lissoir (sorte de tonneau en bois cerclé de bronze, de 1,5 m de Ø, équipé d’une porte d’accès, placé horizontalement sur un axe rotatif, entraîné par des courroies). On ajoute à ces grains avant de refermer la porte quelques centaines de grammes de poudre de graphite. Ce graphite augmente la fluidité des grains et les protège de l'humidité.
Les grains provenant des ateliers grenoirs, mélangés plusieurs heures (4 à 5 heures), sont déversés sur un tamis de la grosseur du grain voulu, puis entreposés en sacs dans un autre hangar dédié, fermé, attenant aux ateliers des grenoirs. Ce tamis élimine les poussières restantes et les plus gros grains.
Séchoir
La poudre de l’atelier lissoir arrive dans sa sixième phase de fabrication. Plusieurs centaines de kilos de poudre sont déposés sur un grand châssis de bois (environ 15 m²) recouvert d’une toile de coton, sur une épaisseur d’une dizaine de centimètres. Cette poudre est séchée par de l’air chauffé à 45 °C, arrivant sous la toile en coton durant vingt-quatre heures.
La poudre noire provenant de sa dernière phase de fabrication, est entreposée en sacs dans un autre hangar dédié, fermé, attenant au séchoir.
Il existe quelques variantes dans la fabrication de la poudre noire, elle ne subit pas forcément toutes les différentes phases décrites ci-dessus. Par exemple, le pulvérin ou le MCHA destinés à la fabrication des artifices ou utilisé dans les carrières d’extraction de pierres, ne subissent pas de phase de séchage.
La poudre noire ainsi obtenue après avoir subi toutes ces phases de fabrication, est destinée à l’emballage, l’emboîtage, ou à la fabrication de pastilles ou de cartouches. Au cours des dernières phases de finition, des échantillons de poudre noires sont prélevés pour être analysés en laboratoire pour déterminer toutes ses caractéristiques techniques ainsi que son taux d’humidité.
Il convient de noter qu’avant l'utilisation de l'électricité, les différents ateliers de fabrication de la poudre noire étaient tous alimentés par la force hydraulique. Lorsque les ateliers ont été modernisés, les axes de transmissions qui étaient entraînés par des courroies, l'ont été par des moteurs électriques. Il convient de noter que pour leur sécurité, tous les ouvriers de fabrication de la poudre noire, qui conduisent les ateliers (excepté les tonnes binaires et les préparations), se trouvent, durant le fonctionnement des ateliers, derrière des murs forts de plus d'un mètre d'épaisseur. Ils doivent tenir, hiver comme été, les sols humides de leurs ateliers en les aspergeant régulièrement à l'eau.
Granulation
Les principales différences entre les différents types de poudres noires que l’on peut trouver sur le marché, résident dans leurs granulométries, ce qui confère à chacune sa vivacité propre. Plus les grains sont petits, plus la poudre est dite « vive », plus elle brûlera vite, plus la montée en pression sera rapide et inversement.
Aparté à destination des tireurs sportifs
Plus la différence entre les tailles de grains est faible, plus la poudre est homogène, plus la montée en pression et la vitesse des balles seront reproduites à l'identique d'un tir à l'autre et donc, plus la précision sera accrue.
En effet, une poudre hétérogène, comme la SNPE Poudre Noire Chasse, contient des grains qui vont de FFFFFg (pulvérin) à FFg (poudre lente).
Comme les grains de granulométries différentes ne sont jamais parfaitement mélangés dans un bidon ou dans une doseuse, il y aura forcément des charges plus vives que d'autres, ce qui engendrera des pressions et des vitesses de balles différentes.
Le tableau supra permet de visualiser la granulométrie de chaque poudre noire et leur classement en conséquence. Il concerne les poudres noires disponibles actuellement, sur le marché français. Les poudres françaises sont représentées en gris et les poudres suisses en noir. Elles sont classées dans l'ordre décroissant, selon leur granulométrie moyenne. En fond, un code de couleurs symbolise l'échelle américaine de granulométrie, de Fg à FFFFg. Les poudres pourront donc être comparées avec cette échelle et donc, avec les poudres américaines.
Ceci est particulièrement intéressant pour transposer en France, avec les PN suisses et françaises, les recommandations américaines, qui sont faites avec leurs PN.
Risques et dangers
La fabrication, le stockage, le transport et la manipulation de poudre à canon ont été source de nombreux accidents.
En outre, la poudre à canon sous forme agglomérée assure de mauvais groupements et engendre des risques supplémentaires lors de l'utilisation.
Législation
En Europe
En Allemagne la poudre noire est vendue exclusivement en armurerie pour les particuliers. Les quantités admises à la vente sont limitées et c'est la SNPE qui fournit le marché allemand[réf. nécessaire]. Vendue dans des bidons contenant 500 g ou 1 kg de poudre, son utilisation est très réglementée. La loi n'autorise pas de posséder plus de 2 kg chez soi.
En France
En France, les lois sont similaires : la poudre noire est vendue en bidons généralement en plastique (antistatique), les quantités sont similaires à l'Allemagne.
Catégories
Les tireurs utilisant la poudre noire en Allemagne utilisent deux types de poudre : l'« allemande » et la « suisse ». La poudre noire allemande (PNA) est réputée moins intéressante pour le tir que la poudre noire suisse « Poudrerie d'Aubonne (Vaud) », mieux dosée et plus régulière.
En France, les tireurs utilisent également deux types de poudre : la « française » et la « suisse ». Les poudres noires françaises (PNF1, PNF2 et PNF4P) sont différentes des poudres noires suisses, en dosage et en granulométrie, à l'usage. La poudre suisse « Poudrerie d'Aubonne (Vaud) » est moins salissante (moins de résidu) et légèrement plus puissante [moins de salpêtre (76 %), plus de charbon de pin (12 %) et de soufre (12 %)].[réf. souhaitée]
Notes et références
- (en) James Riddick Partington, A History of Greek Fire and Gunpowder, The Johns Hopkins University Press,
- Journal des sciences militaires des armées de terre et de mer sur Google Livres
- « Dossier de presse » [archive] [PDF], sur le-thillot.fr (consulté le )
Voir aussi
Bibliographie
- Jean Pierre Paul Tortel, « De l'origine de la poudre à canon et de son premier emploi dans les armes à feu », Le spectateur militaire, , p. 497-531 (lire en ligne [archive]), 1er septembre 1841, p. 617-654, (lire en ligne) [archive]
- Léon Lacabane, « De la poudre à canon et de son introduction en France », Bibliothèque de l'École des chartes, t. 6, , p. 28-57 (lire en ligne [archive])
- Anne Robert Jacques Turgot, Œuvres, t. 2, Bibliothèque nationale de France (BNF Gallica), (BNF 31505417).
- Michel Rival, Grandes Inventions de l'humanité, Paris, Larousse, .
Articles connexes
- Histoire de la poudre à canon
- Poudre pyroxylée
- Explosif
- Munition
- Poudrerie
- Poudrière
- Société nationale des poudres et explosifs
- Loi de Piobert
- Lexique des armes à feu
Liens externes
-
Notices dans des dictionnaires ou encyclopédies généralistes
- « On a enfin inventé la poudre ! » [archive], Eurêka ! , France Culture, 5 juillet 2021.
- La ferme des poudres et salpêtres création et approvisionnement en poudre en France (1664 – 1765) [archive], sur Stratisc.org
- Extrait de l'arrêt du Conseil d'État, qui convertit en une régie, pour le compte du roi, le bail des poudres passé à Alexis Demont le 16 juin 1772 [archive], mai 1775, p. 418
- Extrait du résultat du Conseil du roi, contenant règlement pour l'exploitation de la régie des poudres et salpêtres [archive], mai 1775, p. 419
5G
Article
Discussion
Lire
Modifier
Modifier le code
Voir l’historique
Antennes 5G en Allemagne.
La 5G (cinquième génération) est une norme de réseau de téléphonie mobile. Elle succède à la quatrième génération, appelée 4G1, en proposant des débits plus importants et une latence fortement réduite, tout en évitant le risque de saturation des réseaux lié à l'augmentation des usages numériques (smartphones, tablettes, objets connectés). Son déploiement fait l'objet de contestations concernant en particulier l'effet sanitaire des ondes électromagnétiques et l'impact environnemental de cette technologie.
Caractéristiques
La technologie 5G donne accès à des débits dépassant largement ceux de la 4G, avec des temps de latence très courts2 et une haute fiabilité, tout en augmentant le nombre de connexions simultanées par surface couverte3. Elle vise à supporter jusqu'à un million de mobiles au kilomètre carré (dix fois plus que la 4G)4. Une fois déployée, elle doit permettre des débits de télécommunications mobiles de plusieurs gigabits de données par seconde, soit jusqu'à 1 000 fois plus que les réseaux mobiles employés en 20105 et jusqu'à 100 fois plus rapides que la 4G initiale6.
Pour le ministère de l'Économie français, c'est une « technologie clé »7 car ses débits potentiels répondent à la demande croissante de données suscitée par l'essor des smartphones et des objets communicants, connectés en réseau. Elle devrait favoriser le cloud computing (informatique en nuage), l'intégration, l'interopérabilité d'objets communicants et de réseaux électriques intelligents, dans un environnement domotisé, contribuant à l'essor du concept de « ville intelligente ». Elle pourrait aussi développer la synthèse d'images 3D ou holographique, l'exploration de données, la gestion du big data et de l'Internet des objets, les jeux interactifs et multijoueurs complexes, la traduction automatique et assistée instantanée ou encore le contrôle commande à distance dans des domaines comme la télémédecine et les véhicules autonomes8, et l'automatisation industrielle3.
À l'inverse, des mouvements de contestation se développent de la part des associations d'électrosensibles et de scientifiques qui s'opposent à cette technologie au nom de la lutte contre le réchauffement climatique, de ses effets possibles sur la santé et la biodiversité et de l'absence de démocratie quant à son déploiement et à ses objectifs.
Histoire et contexte
La 1G (1980) a permis la transmission sans fil analogique de la voix, la 2G (1990) a ouvert la voie à la transmission numérique et a permis les SMS, la 3G (2000) a permis le développement du Web mobile, puis la 4G (2010) a permis la voix sur 4G (VoLTE) et augmenté le débit des connexions mobiles.
Recherche et développement technique
En Chine, elle est principalement développée par Huawei, et ZTE, en coopération avec Ericsson depuis 2015, et testée par China Mobile9.
En octobre 2014, le chinois Huawei et l'opérateur japonais NTT Docomo, travaillant avec le fabricant d'électronique NEC, font un test conjoint à grande échelle de réseau 5G via la technologie du MIMO massif à Chengdu (province du Sichuan)10.
En France, le 22 septembre 2015, l'Arcep autorise Orange à tester des technologies 5G11 dans les bandes de 3,7 GHz, 10,5 GHz et 17 GHz dans la ville de Belfort.
En juillet 2016, l'Institut de recherche technologique b-com est retenu par l'Arcep pour tester la 5G à Rennes12.
En décembre 2016 Huawei et NTT DoCoMo font un test dans le quartier Minato Mirai 21 à Yokohama (région du Kantō), sur les fréquences de 4,5 GHz, avec une macro-cellule et 23 équipements d'utilisateurs. Ils obtiennent un débit de 11,29 Gbit/s, avec une latence de 0,5 ms10.
En janvier 2017, le LETI annonce le déploiement sur le complexe Minatec d'un réseau 5G afin de tester une nouvelle forme d'onde multiporteuse13. Le même mois, Orange, en partenariat avec le géant suédois Ericsson, devient le premier opérateur français à réaliser un test 5G. Les résultats permettent d'atteindre un potentiel 75 fois supérieur à celui de la 4G14. Cette performance est toutefois à prendre avec des réserves puisque les conditions optimales du laboratoire dans lequel s'est déroulé le test ne permettent pas de garantir un tel débit dans un environnement lambda.
En février 2017, l'opérateur sud-coréen KT fait des démonstrations de réalité virtuelle en 5G au Mobile World Congress (MWC) de Barcelone15.
En France, le 22 juin 2017, un communiqué de l'Arcep indique qu'elle souhaite préparer la procédure d'attribution de fréquences dans la bande 3,5 GHz (3 400 à 3 800 MHz) pour l'accès fixe à Internet à très haut débit à partir de 2018. Elle souhaite également s'engager dans les travaux préparatoires au lancement des réseaux mobiles 5G dans la bande des 3,46 à 3,80 GHz vers 202016.
En juillet 2017, l'italien TIM signe un accord avec le gouvernement du micro-État Saint-Marin en vue de faire passer son réseau 4G en 5G17.
Définition des standards et phases de test
En juillet 2017, les 28 ministres des télécommunications de l'Union européenne et de la Norvège signent une déclaration d'intention à Tallinn en Estonie, pour « des bases communes des futurs standards 5G et confirmer la volonté des États signataires de positionner l'Europe comme un leader du marché de la 5G18 ».
En Chine, lors de tests de 5G New Radio (NR), Huawei atteint en juin 2017 des débits de 6 Gbits/s9.
Début octobre 2017, l'Arcep autorise Free mobile à tester des technologies 5G19 dans la bande de 3,6 GHz à 3,7 GHz dans la ville de Paris à la mi-octobre 2017.
Le 29 novembre 2017, la société Verizon Communications Inc. annonce qu'elle va déployer un service 5G dans cinq villes des États-Unis dès mi-201820.
En décembre 2017, les grands acteurs concernés s'accordent sur les premières spécifications du protocole à Lisbonne (Portugal), à la suite des essais faits par les différents acteurs21.
En janvier 2018, aux États-Unis, la société AT&T promet de la 5G dès fin 2018, d'abord pour 12 agglomérations22.
En février 2018, Vodafone et Ericsson font une démonstration en Irlande des préstandards de la 5G. Une autre démonstration montre le contrôle à partir des États-Unis d'un drone en Angleterre, via le réseau 5G. D'autres démonstrations ont eu lieu depuis, notamment en France et en Suède. Aux jeux olympiques d'hiver de Pyeongchang, le sud-coréen KT permet via des casques de réalité virtuelle de suivre en temps réel ce que voient les bobsleighs. Cent caméras déployées autour de la piste de patinage artistique, permettent de tourner à volonté autour des patineurs. Un système de caméras de surveillance, associé à une transmission haute définition, détecte automatiquement des sangliers proches de résidences et, à distance, déclenche un haut-parleur imitant le cri d'un tigre pour les éloigner23.
En mars 2018, Huawei et NTT Docomo annoncent la réussite des premiers essais de technologie 5G Integrated Access Backhaul (IAB) dans la bande spectrale des ondes millimétriques. Le test a été conduit dans le quartier Minato Mirai 21 à Yokohama sur une fréquence de 39 GHz. Ils obtiennent un débit de 650 Mbit/s avec une faible latence de 1,6 ms10.
En mars 2018, les participants du Mobile World Congress dénoncent la lenteur du déploiement de la 5G en Europe24,25 à la suite de nombreux désaccords sur les licences d’utilisations des bandes radioélectriques et à la complexité du processus décisionnel européen26.
Toutefois, les démonstrations continuent de montrer l'avancement des travaux, comme en avril 2018 avec Telefónica et un véhicule connecté.
En septembre 2018, l'opérateur China Telecom fait un test réseau 5G à Shenzhen (province du Guangdong), ainsi que 5 autres villes de Chine, Xiong'an (Hebei), Shanghai, Suzhou (Jiangsu) et Chengdu (Sichuan). Le débit à Shenzhen est au minimum 10 fois plus important que la 4G, oscillant de 1 à 3 Gbit/s. Le réseau devrait être étendu à certaines petites régions en 2019, avec une commercialisation en 202027,28. L'Amérique latine espère 8 % d'usagers ayant accès à la 5G avant 202529. En Afrique, le royaume du Lesotho est choisi en septembre 2018 pour tester la première installation 5G en Afrique30.
Attribution des licences et exploitation commerciale
Le partage intelligent du spectre électromagnétique attribuable à la 5G par un grand nombre d'opérateurs civils, industriels et militaires, en utilisant le principe d'optimisation par la radio intelligente, ou radio cognitive (peut être bientôt dotée d'algorithmes bio-inspirés ou assistée par intelligence artificielle)31, tout en limitant les risques pour l'environnement et la santé, est un enjeu technico-économique, cyberstratégique, environnemental faisant l'objet d'âpres discussions dans les années 2010-202032, y compris au niveau géopolitique33.
En février 2019, en Suisse, les licences pour les fréquences 5G sont attribuées à trois opérateurs Swisscom, Sunrise et Salt pour 379,3 millions de francs suisses34. Après la Finlande, la Suisse est le second pays d'Europe à avoir attribué des fréquences à la 5G35.
Le 3 avril 2019, la Corée du Sud est le premier pays à déployer une offre commerciale 5G au niveau national36.
Le 4 avril 2019, l'opérateur Sunrise en Suisse devient le premier opérateur du pays à déployer une offre commerciale sur 150 localités37. Il couvrait 173 localités début mai 201938.
Le 17 avril 2019, Swisscom met en service 338 antennes 5G et annonce vouloir couvrir l'ensemble du territoire suisse avant fin 201939.
Le 15 juillet 2019 en France l'Arcep annonce le lancement officiel de la procédure d'attribution des fréquences par le gouvernement40. Avec l'objectif de proposer les premières offres commerciales 5G à l'horizon 2020, le gouvernement met en vente les premières bandes de fréquences à des tarifs fixes ; ces bandes seront mises à disposition à des tarifs avantageux afin d'inciter les opérateurs à développer la 5G en priorité. Pour certains blocs de fréquences, ce sont toutefois des enchères qui permettront aux opérateurs de se départager, dont pour une partie de la bande de fréquences 3,4 à 3,8 GHz41 et dans un avenir proche, de la bande de fréquences 24,25 à 27,5 GHz.
Dans un contexte géopolitique complexe (avec par exemple les questions de cybersécurité et d'indépendance économique posées à partir de 2018 par Huawei en Occident)42,33, d'abord prévue pour début 2020 en France, l'attribution des licences 5G est reportée au printemps 202043 puis à l'automne à cause de la pandémie de Covid-19. Les enchères pour la bande 3,5 GHz se sont achevées en octobre 2020, et les autorisations d'implantation ont commencé en novembre 202044.
Recherche, tendances et prospective
Tous les grands opérateurs du secteur des télécommunications s'intéressent au sujet ainsi que de grandes institutions et de nombreux États : par exemple, l'Union européenne a financé ou cofinancé de grands programmes comme 5G now, IJoin, Tropic et METIS (Mobile and wireless communications Enablers for the Twenty-twenty Information Society).
Alors que l'impact environnemental du numérique croît exponentiellement45,46, de grandes entreprises et des réseaux de chercheurs tentent d'imaginer ou préfigurer une « 5G verte »47,48, à moindre empreinte carbone et préservant des ressources naturelles souvent peu renouvelables ou peu recyclées.
En juillet 2014, le suédois Ericsson a fait la démonstration d'une préversion de la technologie 5G. L'entreprise de télécommunication avait alors atteint un débit de 5 Gbit/s49,50.
En juin 2016, le Laboratoire d'électronique et de technologie de l'information lance le projet de démonstrateur de technologie 5G, à l'occasion des Jeux olympiques d'hiver de 2018 devant se dérouler à Pyeongchang en Corée du Sud. En collaborant avec des entreprises comme Thales Alenia Space ou Telespazio, le laboratoire compte s’appuyer sur les technologies d'onde radioélectrique de la bande de fréquence 28 GHz qui existent déjà dans le domaine spatial pour arriver à ses fins51.
En juillet 2017, Saint-Marin signe un protocole d'accord avec Telecom Italia pour le déploiement expérimental de la 5G sur son territoire, ce qui fera d'elle la première nation à mener des tests poussés à grande échelle de cette technique52.
Enjeux
Économie
Selon Nicolas Sironneau, de la Fondation Concorde, la 5G présente trois intérêts économiques :
soulager les réseaux de télécommunications mobiles qui vont arriver à saturation, et ainsi éviter un phénomène d'engorgement des données53 ;
permettre aux entreprises d'optimiser certains processus, à travers l'automatisation et la fluidification de tâches (prenant l'exemple de la réalité augmentée utilisée dans des usines pilotes d'Ericsson pour aider la détection de défaut de fabrication) ;
permettre le développement de nouvelles applications s'appuyant sur les nouvelles performances (par exemple la télé-chirurgie permise par un temps de latence très court et garanti)54.
De nombreux acteurs voient là un gisement émergent d'applications et débouchés nouveaux dans des domaines aussi variés que la santé (diagnostic automatique ou distant, chirurgie et médication commandées à distance)55, du travail (télétravail), du déploiement d'objets communicants (dont voitures et autres véhicules sans conducteurs), de détecteurs et senseurs du commerce en ligne, des réseaux électriques intelligents, de l'intelligence artificielle, de la sécurité (télésurveillance, gestion des flux de personnes, véhicules, denrées, biens et services en temps réel, etc.), de l'éducation et de l'accès à l'information. De nouvelles applications 5G seront développées s'appuyant sur la multiplication des objets connectés en réseau.
En France, fin 2020, Arnaud Montebourg prend acte de l'arrivée de la 5G et se dit favorable à une intervention de l'État pour favoriser le développement d'une solution nationale en matière d'équipements, citant l'ex-société Alcatel56.
En 2019, les États-Unis souhaitent favoriser l'entreprise Cisco Systems face aux leaders du moment, Huawei, ZTE (Chine), Nokia et Ericsson (Union européenne). Lors d'un sommet organisé à la Maison-Blanche, le président de la Commission fédérale des communications (FCC) déclare : « Le leadership américain dans la technologie 5G est un impératif national pour la croissance économique et la compétitivité »57.
Sécurité nationale
Développer la 5G, technologie aussi prometteuse que sensible, implique de disposer d’équipementiers télécoms, qui deviennent un enjeu stratégique de souveraineté et de sécurité nationale.
La Chine dispose de deux équipementiers : Huawei et ZTE ; l’Europe aussi, Nokia et Ericsson. Les États-Unis, en revanche, n’en ont plus, et s'intéressent aux entreprises européennes58.
L’équipementier Huawei suscite l'hostilité d’un nombre grandissant de pays occidentaux qui redoutent que ce poids lourd des télécoms serve de cheval de Troie à la Chine, et l’aide à espionner les puissances étrangères. Les États-Unis, l’Australie, la Nouvelle-Zélande et le Japon ont déjà banni l’entreprise du marché de la 5G.
Le 29 janvier 2020, la Commission européenne et la présidence du Conseil de l'Union européenne ont présenté une approche européenne concertée sur la sécurité des réseaux de télécommunications 5G européens59,60.
Dès 2019, le gouvernement français fait part de ses inquiétudes à l'Autorité de régulation des communications électroniques, des postes et de la distribution de la presse (Arcep) sur les problèmes de sécurité du futur déploiement des infrastructures réseaux Télécom 5G qui ferait à la fois planer une menace sur la souveraineté nationale mais aussi sur des applications critiques61.
Le gouvernement français va légiférer62 pour créer un régime d’autorisation préalable aux équipements radioélectriques. Concrètement, l’Agence nationale de la sécurité des systèmes d'information (ANSSI) pourrait examiner les nouveaux équipements des réseaux mobiles avant leur installation et les interdire si elle juge qu’ils menacent « les intérêts de la défense et de la sécurité nationale ».
En 2018, l’État finlandais prend une participation dans la société Nokia63, ce qui lui donne un droit de regard. « Nous avons renforcé et stabilisé l'actionnariat national de cette société très importante au niveau de notre pays », a déclaré le directeur général de Solidium, Antti Mäkinen. Nokia sera un des deux fournisseurs européens d'infrastructure de télécommunications en particulier pour la 5G. Nokia a pris le contrôle de la société Alcatel-Lucent en 201563.
En mars 2020, un rapport de la Fondation Concorde sur la 5G invite à créer « une certification européenne unifiée des réseaux 5G [au niveau européen] pour en garantir la sécurité », et à renforcer « les moyens de l’ENISA, l’European Network and Information Security Agency afin d’intervenir sur les questions de cybersécurité liées à la 5G »54, Nicolas Sironneau (co-auteur du rapport) mettant en garde contre la perte de contrôle sur les infrastructures cœur des réseaux de demain53. Des professeurs comme Dominique Boullier vont dans le même sens, proposant « un cahier des charges sur les questions de sécurité »64.
En juillet 2020, le directeur de l’ANSSI indique que les opérateurs français utilisant les équipements de Huawei dans leurs réseaux déjà déployés disposeront d'autorisations d’exploitation limitées de trois à huit ans65. D'autres pays européens prennent également des mesures de restriction contre les opérateurs voulant déployer un réseau 5G avec Huawei66.
Si les pays européens bannissent les fournisseurs chinois de leurs réseaux 5G, le ministère chinois du Commerce envisagerait des mesures contre les activités chinoises de deux fabricants européens d'équipements de télécommunications, tels des contrôles à l'exportation qui empêcheraient Nokia et Ericsson d'exporter des produits fabriqués en Chine vers d'autres pays67.
Météorologie
En 2019, face à leurs nouveaux besoins, des entreprises de télécommunications américaines ont acheté une nouvelle partie du spectre électromagnétique pour élargir leur bande passante en utilisant la 5G. Cela inquiète les météorologues.
En avril et novembre 2019, deux articles de la revue Nature émettent l'hypothèse que certaines fréquences utilisées en 5G pourraient entrer en conflit dans la bande millimétrique des 26 GHz avec l'observation de la vapeur d'eau et réduire la précision des relevés météorologiques68,69,70. Cet afflux de signaux puissants peut parasiter ou submerger de nombreux signaux plus faibles émis par la vapeur d'eau, situés dans une bande toute proche du spectre, signaux qui sont nécessaires à une bonne prévision météorologique. En août 2019 aux États-Unis, Gabriel Popkin (vulgarisateur scientifique) s'est associé à l'animatrice Sarah Crespi pour sensibiliser aux effets négatifs possibles d'une utilisation de cette partie du spectre électromagnétique par les signaux de la 5G ; ils suggèrent qu'une réglementation encadre ce développement. Cette alerte a été relayée par la revue Science71.
Le Centre européen pour les prévisions météorologiques à moyen terme (ECMWF) regrette72 également les décisions prises lors de la Conférence mondiale des radiocommunications de 2019 (CMR-19)73 de l'ITU.
En France, l'Agence nationale des fréquences (ANFR) nuance ce risque74, du moins en ce qui concerne l'Europe.
Selon un rapport du Haut Conseil pour le climat de décembre 2020, l'utilisation d'une troisième gamme de fréquence dans le futur (autour de 26 GHz) risque de provoquer « des interactions avec les fréquences utilisées par les satellites d'observation de la Terre »75.
Effets sur la santé
Article connexe : Effet des rayonnements électromagnétiques sur la santé.
Article détaillé : Impact sanitaire et environnemental de la 5G.
En 2014, l'OMS déclare qu'« un grand nombre d’études ont été menées au cours des deux dernières décennies pour déterminer si les téléphones portables représentent un risque potentiel pour la santé. À ce jour, il n’a jamais été établi que le téléphone portable puisse être à l’origine d’un effet nocif pour la santé76. »
La course internationale au déploiement de la 5G suscite des craintes sanitaires, notamment car la 5G nécessite l'utilisation intensive d'une nouvelle gamme de longueurs d'onde (fréquences plus élevées), et la création d'un grand nombre de nouveaux réseaux cellulaires étendus (ou WAN). Ces réseaux seront constitués de minuscules stations de base fournissant une couverture mobile haute fréquence, sur une portée de 200 à 400 m seulement77 ; ces stations devront donc être « positionnées tous les quelques centaines de mètres dans les zones urbaines densément peuplées »78. À la différence de la 4G, la 5G passera aussi par un signal plus concentré vers les appareils, ce qui pose de nouvelles questions sanitaires78.
En septembre 2017, 171 scientifiques, issus de 37 pays (99 dans l'Union européenne et 72 dans les autres pays) ont réclamé un moratoire sur le déploiement de la 5G, en attendant que les risques potentiels sur la santé humaine et l'environnement aient été pleinement étudiés par des scientifiques indépendants du secteur79.
En 2018, en France, une parlementaire demande au gouvernement de « faire réaliser des études indépendantes et approfondies concernant les effets de la 5G ». Le gouvernement s'engage à travailler avec l'Agence nationale des fréquences et l’Agence nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail « afin qu’elles puissent examiner d’une part, l’exposition aux ondes électromagnétiques et d’autre part, l’impact sanitaire éventuel de ces nouveaux développements technologiques, dès la phase des expérimentations »80.
Début 2019, de nombreuses inquiétudes sur l'impact de cette technologie sur la santé accompagnent le déploiement de la 5G en Suisse81. Le déploiement de 10 000 nouvelles antennes fait craindre une augmentation considérable de l’exposition au rayonnement de radiofréquences82. Une pétition demandant un moratoire recueille plus de 56 000 signatures. Alors que Swisscom a lancé en avril 2019 le premier réseau 5G de Suisse, certains cantons comme ceux de Vaud, de Genève et du Jura optent pour le principe de précaution et suspendent le déploiement des antennes83,84.
En 2019 la professeure (retraitée) Marie-Claire Cammaerts de l'université libre de Bruxelles, spécialiste du comportement des fourmis85, et le professeur André Vander Vorst de l’UCLouvain s'inquiètent du déploiement de beaucoup plus d’antennes qui provoquerait une exposition accrue aux champs électromagnétiques86.
En juin 2020, en France, la campagne des municipales offre une caisse de résonance aux mouvements opposés à la 5G : plusieurs candidats de la mouvance écologiste, souvent en bonne position pour être élus, réclament un moratoire sur le déploiement de la 5G. La ministre de la Transition écologique et solidaire, Élisabeth Borne et Olivier Véran, ministre de la Santé ont saisi le Premier ministre à ce sujet, souhaitant que la 5G ne soit pas déployée avant que l'Agence nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail (Anses) rende son rapport sur les conséquences sanitaires de la 5G87. En janvier 2020, l'Agence nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail rend un rapport préliminaire sur les risques sanitaires liés à la 5G, mais son analyse des travaux existants met en évidence « un manque de données scientifiques sur les effets biologiques et sanitaires potentiels »88.
Un texte proposé par la députée d’Europe Écologie Les Verts, Laurence Abeille, est adopté par l’Assemblée nationale française début 2015. Le texte vise l'encadrement de l'exposition aux ondes électromagnétiques par une concertation à plusieurs niveaux lors de l’installation d’équipements radioélectriques, une meilleure information sur les sources d’émission, l'interdiction de la publicité pour les téléphones portables et autres terminaux sans accessoire permettant de limiter l'exposition (oreillette) – l'opérateur de téléphonie doit fournir un accessoire limitant l'exposition adapté aux enfants de moins de 14 ans si un acheteur le demande –, et demande au gouvernement un rapport sur l’électro-hypersensibilité89. Ce rapport, rendu finalement en 2019, recommande de suivre l'exposition de la population aux champs électromagnétiques et de poursuivre la recherche sur le sujet, tout en rappelant qu'aucun lien n'a à ce jour pu être établi entre l'exposition à ces champs et les symptômes rapportés par les personnes se disant électro-hypersensibles90.
Un rapport parlementaire publié le 19 juin 2020, initié par deux députés européens écologistes, l’Allemand Klaus Büchner et la Française Michèle Rivasi, accuse la Commission internationale de protection contre les rayonnements non ionisants, organisation non gouvernementale dont les travaux servent de base à la détermination des limites d'exposition fixées par l'Union européenne, d’être sous l’influence des géants des télécommunications et de ne pas prendre en compte les publications scientifiques alertant sur les risques sanitaires liés au développement de la 5G91.
Une étude sur l'impact sanitaire de la 5G92, commandée par le gouvernement français au Conseil général de l'environnement et du développement durable, à l'Inspection générale des affaires sociales, à l'Inspection générale des finances et au Conseil général de l’économie, est présentée le 14 septembre 2020. Elle conclut que les risques pour la santé humaine de l'exposition aux fréquences radioélectriques ne sont pas avérés en l'état actuel des connaissances scientifiques et note qu'aucun des pays qui ont déjà lancé la 5G n'a constaté de problème d'ordre sanitaire93.
En avril 2021, l'ANSES publie une évaluation qui conclut que la 5G ne présente pas de risques nouveaux pour la santé au vu des données disponibles. Plus précisément, elle estime que le déploiement de la 5G dans la bande de fréquences 3,5 GHz ne devrait pas présenter de risques nouveaux, mais que les données disponibles actuellement ne suffisent pas pour conclure à l’existence ou non d’effets sanitaires dans le cas de la bande 26 GHz, qui doit compléter le réseau dans quelques années. Elle appelle donc à poursuivre les recherches dans ce domaine94.
Environnement et énergie
Articles détaillés : Efficacité énergétique des communications 5G et Impact sanitaire et environnemental de la 5G.
Articles connexes : Impact environnemental du numérique et Sobriété numérique.
Les opérateurs annoncent que l'efficacité énergétique de la technologie 5G sera améliorée (à quantité égale de données transportées), car la technologie massive MIMO réorganisera l'accès au réseau mobile grâce à des faisceaux orientables et plus fins, orientés vers les utilisateurs (beamforming95) et parce qu'une concentration des équipements promet une meilleure efficacité énergétique. De plus, des technologies déployables de sleeping mode permettront d'économiser la batterie et les communications entre terminaux. L'augmentation éventuelle de la consommation énergétique et du besoin de serveurs sera donc surtout due à l'augmentation de l'offre et de la demande induite par l'augmentation du débit (effet rebond)96.
Le rapport du Haut Conseil pour le climat de décembre 2020, en France, pointe l'augmentation des émissions de dioxyde de carbone (CO2) liée à la mise en œuvre de la 5G. Cette augmentation résultera notamment du renouvellement des téléphones mobiles, qui représente 54 % de l'impact carbone de la 5G d'après le rapport. La construction des nouvelles infrastructures, les antennes et les centres de données comptent respectivement pour 14 % et 8 % du total. Les émissions liées au déploiement de la 5G seront majoritairement situées à l'étranger, et donc comptabilisées comme émissions de CO2 importées. Le rapport recommande que l'Europe adopte des normes pour réduire les émissions importées liées aux équipements électriques et électroniques. L'utilisation de la 5G ne compte que pour 24 % de ses émissions de CO2. Le Haut Conseil déplore que l'Arcep n'ait pas parmi ses missions la question climatique et qu'il n'y ait pas eu d'étude d'impact avant l'attribution des fréquences75,97. Le rapport du Haut Conseil pour le climat (HCC) recommande aussi de s'assurer que l'augmentation de la consommation d'électricité causée par le déploiement de la 5G, estimée entre 16 et 40 TWh en 2030, soit 3 à 8 % de toute l'électricité consommée en France en 2019, n'affecte pas la programmation pluriannuelle de l'énergie. Une augmentation des usages au niveau européen pourrait par ailleurs avoir des effets sur le prix de électricité et la justice sociale97,98. Les auteurs du rapport abordent rapidement la question des économies d'énergie que cette nouvelle technologie pourrait permettre99, mais se sont heurtés à la difficulté de quantifier ces économies97.
Internet des objets
Article principal : 5G pour l'Internet des objets.
La 5G permet de nouvelles fonctionnalités, notamment la virtualisation et de nouvelles architectures, propice au développement des objets connectés, des applications hébergées dans le cloud, en passant par diverses couches réseaux. La maison connectée, le véhicule autonome, les vidéos immersives et l’arrivée de la médecine 2.0 devraient en bénéficier. Plus de 80 milliards d’objets pourraient ainsi être « connectés » en 2024100.
Couverture réseau et infrastructure
Les propriétés de propagation de la 5G dans la bande des 3,5 GHz sont telles que, pour arriver à un taux de couverture et de services équivalents à la 4G, il faut fortement densifier les réseaux. Une simulation de réseaux radio ATOLL faite par le cabinet de conseil indépendant Tactis101, montre qu'en zone rurale, il faudrait tripler le nombre de pylônes en 5G à 3,5 GHz pour obtenir une couverture équivalente à celle de la 4G. Cette densification n'est pas nécessaire pour la bande des 700 MHz.
En France, selon l'Arcep, la technologie 5G ne nécessite pas d'envoyer de nouveaux satellites dans l'espace102.
Techniques
Le 12 mai 2013, Samsung a annoncé avoir testé pour la première fois avec succès des techniques de sa future offre de réseaux 5G qu'il prévoit pour 2020, avec des débits de données d'un Gbit/s (1 gigabit par seconde) et pouvant aller dans le futur à 10 Gbit/s103,104,105.
En 2015, le Centre d’innovation consacré à la 5G (5GIC) de l’université de Surrey, en Grande-Bretagne, annonce avoir réussi à atteindre un débit d'un Tbit/s106 (1 térabit par seconde) sur des fréquences supérieures à 6 GHz. La même année, le centre mathématiques et algorithmiques de Huawei à Paris propose 5 technologies permettant des débits compatibles avec les prérequis de la 5G : Le F-OFDM (Filtered OFDM) pour la forme d'onde, le SCMA (Sparse Code Multiple Access) pour la technique d'accès, les codes polaires (pour le codage des différents types de paquets), le MU-MIMO massif (pour le système d'antennes avec des techniques de précodages non linéaires) et enfin le full duplex radio (qui combine les modes TDD et FDD). L'ensemble de ces technologies ont permis de démontrer lors d'essais en extérieur à Chengdu avec NTT Docomo en Chine en octobre 2015 des efficacités spectrales en liaison descendante de 50 bit/s/Hz et une capacité multipliée par 3 en liaison montante sur des fréquences inférieures à 6 GHz.
La 5G permettra théoriquement de télécharger un film de 33 Go en 4K (UHD) en moins de 10 secondes[réf. souhaitée].
Catégories de terminaux mobiles
Nouvelles catégories de terminaux 5G (3GPP rel.15)107, ETSI F5G (rel.1.1.1)108
Catégorie LTE
18
19
20
21
22
23
24
25
26
Débit crête (Mbit/s)
Descendant
1 174
1 566
1 948
1 348
2 349
2 695
2 936
3 132
3 422
Montant
211
13 563
316
301
422
527
633
738
844
Caractéristiques fonctionnelles minimales
Largeur de la bande de fréquence de chaque porteuse
1,4 à 20 MHz
Nombre de porteuses radio agrégées dans le sens descendant
2, 4, 8
2, 4
2, 4, 8
Nombre de porteuses radio agrégées dans le sens montant
2, 3 ou +
Modulations sur chaque sous-porteuse
Descendante
64QAM, 256QAM
64QAM, 256QAM, 1024QAM
64QAM, 256QAM
64QAM, 256QAM, 1024QAM
Montante
64QAM, 256QAM
64QAM
64QAM, 256QAM
Types d'antenne sur la liaison descendante
MIMO 2×2
Oui
MIMO 4×4
Oui
MIMO 8×8
Oui
Non
Oui
MU-MIMO
Lors du test de Huawei, le système multi-utilisateur MIMO (multi-user MIMO (en)) a pris en charge jusqu'à 24 utilisateurs et 24 couches de transmission parallèles sur une même ressource temporelle de fréquence. Les tests ont démontré que le système MU-MIMO peut atteindre un débit moyen de 3,6 Gbit/s par cellule sur une bande passante de 100 MHz, soit près de dix fois les performances obtenues avec un système de base LTE. L'essai a confirmé l'intégration optimale de ces nouvelles technologies radio, ainsi que le potentiel des technologies flexibles d'interface radio 5G. Ces tests ont également été l'occasion de procéder à une évaluation des risques techniques, qui vient étayer le travail actuel de normalisation du 3GPP.
Onde radio centimétriques et millimétriques en 5G
Les ondes centimétriques désignent les ondes radio à hautes fréquences, comprises entre 3 et 30 GHz (également appelées supra-haute fréquence ou SHF), et les ondes millimétriques celles de fréquences comprises entre 30 et 300 GHz (extrêmement haute fréquence ou EHF). L'utilisation d'ondes millimétriques est jusqu'à présent restreinte aux applications d'intérieur et aux faisceaux hertziens. L'une des raisons de cette restriction repose sur le fait que les ondes millimétriques subissent plus d'affaiblissement de propagation.
En France, la bande 3,5 GHz (3,4 – 3,8 GHz) est en cours de déploiement, tandis que la bande 26 GHz (24,25 – 27,5 GHz) fait l'objet d'expérimentations. D'autres pays mènent des expérimentations dans le domaine des fréquences comprises entre 24 et 60 GHz (SHF et EHF)109.
Full-duplex
Le mode full-duplex a été testé dès la première phase des essais 5G, montrant qu'il permet la transmission et la réception simultanées des données au niveau de la station de base, avec trois niveaux de technologie en cascade, à savoir l'annulation analogique passive, l'annulation analogique active et l'annulation numérique. Ces tests montrent que le full-duplex permet d'optimiser l'annulation de l'auto-interférence (en) de plus de 113 dB en situation réelle, ce qui augmente de 90 % le débit du système par rapport aux modes half-duplex traditionnellement utilisés.
Tableau récapitulatif des techniques 5G
Les futures générations de réseaux mobile 5G
Génération
Acronyme
Normes 3GPP - ETSI
Fréquences
Débit indicatif (download) en bit/s(théorique/pratique/usuel)
5G
IMT-2020
ETSI TS V15.6.0 (3GPP rel.15)107
octobre 2019
ETSI F5G (rel.1.1.1)108
décembre 2020
Plusieurs bandes de fréquences deux segments :
5G sub-6 GHz 700 MHz, 2,1 GHz, 3,5 GHz
5G mmWave de 24 GHz, (Génération 5G), jusqu'à 100 GHz.
Référence 1-10 Gbit/s
50 Gbit/s110 (débit théorique annoncé en 2013)
Financements
En mars 2013, la Commission européenne annonce 50 millions d'euros de subventions pour des projets liés à la 5G111.
La Commission supervise et cofinance le consortium Metis (partenariat public-privé112 contractuel de recherche « cPPP »), et a annoncé (en décembre 2013) ne pas vouloir prendre de retard sur la 5G ; il sera doté d'un budget de 700 millions d'euros pour la période 2014-2020113.
En novembre 2013, la compagnie chinoise Huawei annonce avoir investi dans ces techniques dès 2009 et réussi à faire le premier test mondial d'un réseau cellulaire. L'entreprise investira 600 millions de dollars dans la recherche et développement de la 5G et prévoit à l'horizon 2018 que les utilisateurs auront un accès mobile à Internet avec un débit de 1 Gbit/s avec la 4.5G et jusqu'à 50 Gbit/s avec la 5G, comme annoncé lors des Mobile World Congress de 2011 et 2012114. Dans ce cadre, Huawei a mis en place un centre en mathématiques et algorithmiques de 100 personnes à Paris autour de la 5G et l'intelligence artificielle pour les réseaux, dirigé par le professeur Mérouane Debbah115,116,117. Les investissements nationaux devraient dans le domaine atteindre 2,8 trillions de yuans (soit 411 milliards $ de dollars US) entre 2020 et 2030, dans ce qui est déjà le plus important réseau mobile au monde9.
Début 2014, la Corée du Sud a annoncé investir 1,1 milliard d'euros pour la mise en place de la 5G en 2020118,119,120.
En août 2018, Samsung investit dans des technologies d'avenir. Le conglomérat annonce le 8 août qu'il va injecter 19 milliards de dollars dans des programmes liés à l'intelligence artificielle et la 5G.
Mouvements et sujets de contestation
La contestation s'organise autour de deux principaux thèmes :
l'effet sanitaire des ondes électromagnétiques : depuis les années 1990, aux États-Unis notamment, certains défenseurs de la santé, de l'environnement s'inquiètent d'éventuels effets sanitaires des champs électromagnétiques, jugent que les normes d'exposition sont trop peu exigeantes, parfois non respectées, et que les organismes de réglementation comme la Commission fédérale des communications sont sous l'influence des lobbyistes de l'industrie des télécommunications78 ;
l'impact environnemental de cette technologie : un appel de mille scientifiques121, publié le 20 février 2020 dans le quotidien français Le Monde, déclare : « Continuer à promouvoir des technologies superflues et énergivores comme la 5G ou la voiture autonome est irresponsable à l'heure où nos modes de vie doivent évoluer vers plus de frugalité » ;
Manifestation contre la 5G à Lyon en 2019.
Aux États-Unis et en Europe, des mouvements semblables ont réussi, dans les années 1990 et 2000, à faire modifier certaines recommandations et réglementations sur la proximité et/ou la puissance des antennes et du Wi-Fi à proximité des zones résidentielles ou d'écoles122. En 2019 et 2020, plusieurs villes des États-Unis, et Bruxelles (Belgique) ont, par précaution, interrompu les déploiements de la 5G en réponse aux manifestations, au manque de données sur d'éventuels risques sanitaires ou environnementaux, pour des problèmes d'esthétique, etc.123,124.
En France, en 2020 une pétition en ligne est lancée par deux associations, Agir pour l'environnement et Priartem, pour un gel par le gouvernement du déploiement de la 5G125.
En septembre 2020, un sondage Ifop pour le site lemon.fr montre que 63 % des Français souhaitent que les pouvoirs publics facilitent le déploiement de la 5G en France. Même les sympathisants d'EELV sont à 57 % favorables au développement de la 5G. Pour autant, près d'un Français sur deux (48 %) était favorable à la suspension du déploiement de la 5G en France au moins jusqu’à l’été 2021126.
Une autre tribune publiée en janvier 2020 par les dirigeants de l'association The Shift Project127 statue qu'un équipement 5G consomme trois fois plus d'énergie qu’un équipement 4G, et qu'avec la 5G il faudra trois fois plus de sites qu’avec la 4G pour assurer la même couverture, en conséquence estime à 10 TWh la consommation supplémentaire d'électricité pour les opérateurs mobiles d'ici à cinq ans à cause de la 5G, soit 2 % de la consommation annuelle française ; elle souligne que « le problème du numérique, c'est précisément la surconsommation », et appelle à réserver la 5G à certains usages bien précis128.
Évoquant cette contestation, le président de la République française Emmanuel Macron réaffirme le 14 septembre 2020 que la France déploiera la 5G en déclarant « Évidemment on va passer à la 5G. La France c'est le pays des Lumières (...) Certains voudraient revenir à la lampe à huile, moi je ne crois pas au modèle Amish ». Il abandonne ainsi la demande d'un moratoire émise par la Convention citoyenne pour le climat129.
Théories du complot et Covid-19
Communication de l'OMS démentant un lien entre 5G et Covid-19.
S'appuyant sur des inquiétudes anciennes, et souvent sur de la désinformation130, plusieurs théories du complot sont nées au sujet de la 5G (par exemple en Australie, au Royaume-Uni et aux États-Unis)131, technologie qui serait selon certaines de ces théories une cause de la pandémie de Covid-19 en 202078,132. Ces théories sont multiformes, évolutives et parfois contradictoires133,131,130.
Selon Meese (2020)78, ces « conspirateurs » n'opèrent pas dans le vide, mais en s'appuyant beaucoup sur les réseaux sociaux, ils s'inspirent de méthodes éprouvées134,135 antérieurement développées par des protestataires, lobbyistes et conspirateurs. Leur répertoire utilise la « perception sélective » des connaissances scientifiques136, des formes d'action directe, jusqu'à l'intervention dans l'élaboration des politiques locales, étatiques et fédérales, et d'autres formes de « subversion coordonnée »137 visant à freiner le déploiement technique de la 5G. Le sujet n'est d'ailleurs pas entièrement neuf : la 5G exacerbe des préoccupations déjà apparues pour la 4G et les effets des champs électromagnétiques, suscitant des pétitions, des manifestations et des vandalismes d'antennes78.
Les auteurs d'une étude de 2020 sur ce sujet soutiennent que pour bien comprendre ces évènements, il faut voir « au-delà des théories du complot ». Selon eux, « la bataille pour le contrôle de l'infrastructure 5G peut être comprise en termes géopolitiques, comme une forme de politique économique, ce qui explique en partie pourquoi les gouvernements sont de plus en plus soucieux de contrer la désinformation autour de la 5G »78.
Une nouvelle théorie a été en 2020 de faire passer la 5G pour une cause ou un facteur aggravant de la pandémie de Covid-1978 : une première vague affirmait que le rayonnement induit par la 5G affecte notre système immunitaire, nous rendant plus vulnérable au virus SARS-CoV-2138, une théorie proche de celle, plus ancienne, voulant que des cancers ou autres maladies soient induits par des ondes (non-ionisantes) telles que celles des téléphones mobiles ou du compteur Linky139 ; une autre vague, plus importante, avec diverses variantes, affirme que la 5G cause directement la Covid-19, utilisant des affirmations fausses : la Covid-19 aurait été inventée pour couvrir les effets délétères du rayonnement 5G139,132 ; le confinement serait une couverture pour permettre aux opérateurs d'installer des antennes en toute tranquillité132 ; selon une autre théorie, la pandémie serait apparue à Wuhan car cette ville aurait « été la ville cobaye de la 5G »140, alors qu'en réalité Wuhan n'est qu'une des 50 grandes villes testant la 5G en Chine (toutes depuis le 31 octobre 2019) et que par ailleurs, la 5G à usage commercial la plus développée a été activée plus tôt (avril 2019) en Corée du Sud, pays particulièrement peu touché par la pandémie à ce moment132. Le site Siècle digital ajoute que « des pays, comme l’Iran, très touché par le coronavirus (...) n’ont pas une seule antenne 5G sur leur territoire »132.
L'origine des théories relatives à la Covid-19 est souvent difficile à détecter. Le médecin généraliste belge Kris Van Kerckhoven a pu jouer un rôle en déclarant dès le 22 janvier 2020 pour l’édition régionale du journal belge Het Laatste Nieuws que la 5G était dangereuse et qu'elle pouvait « être liée au coronavirus »141,132. Des militants anti-5G néerlandophones ont relayé cette affirmation sur internet via les communautés militantes des réseaux sociaux141. Des groupes (New Agers, groupes d'extrême droite comme InfoWars, des sites conspirationnistes comme Zero Hedge ou QAnon) prétendant vouloir révéler au monde la « vérité » sur la pandémie142 ont alors décliné cette idée en de nouveaux contenus. Facebook et YouTube ont été des relais vers des millions de personnes143,132. BuzzFeed a signalé que dès mi-2019, des vidéos publiées au Royaume-Uni (où la 5G commençait son déploiement) sont rapidement devenues parmi les plus populaires en ligne142,144) ; la plupart ne citaient pas la Covid-19, mais, selon Meese, elles ont « contribué à attiser des craintes plus générales concernant la 5G »78.
Des personnalités ou célébrités ont ensuite relayé ces théories, dont Woody Harrelson dans une vidéo sur Instagram prétendant « montrer des citoyens chinois renversant une antenne 5G », ou le professeur émérite Martin Pall, qui a prétendu à tort que « Wuhan était la première « ville intelligente » de Chine à intégrer le réseau plus rapide »138, la rappeuse M.I.A., l'acteur John Cusack, le boxeur Amir Khan, la chanteuse Anne-Marie, Keri Hilson et des personnalités de la télévision comme Amanda Holden143,132,141,145.
L'infodémie n'a pas épargné le monde francophone : par exemple le 4 avril 2020, dans un post sur Facebook, une utilisatrice a publié une carte comparant un soi-disant déploiement des antennes 5G en France avec la taille des foyers d’infection de coronavirus dans l’Hexagone, deux cartes semblant concorder132. En réalité cette carte, produite par l'Autorité de régulation des communications électroniques, des postes et de la distribution de la presse, était ancienne et représentait le déploiement de la fibre optique ; elle s'expliquait surtout par la densité de population ; de plus, la vraie carte du déploiement de la 5G, publiquement disponible, montrait que la région Grand-Est, alors la plus touchée, n'avait encore aucune antenne 5G146. Enfin, les antennes 5G expérimentales n'ayant pas encore d'utilisateurs, elles émettaient très peu147, ce que montre une étude de l’ANFR publié en avril 2020.
En réponse, partout dans le monde, de nombreux sites d'informations et des responsables de la santé ont tenté de contrer ces rumeurs et fausses informations, notamment en demandant aux plateformes de médias sociaux de mieux contrer ou signaler la désinformation. Beaucoup de ces plateformes ont placé sur leurs pages des liens vers les informations de l'Organisation mondiale de la santé et des gouvernements, et se sont engagées à lutter contre la désinformation sur la Covid-19140.
Le 16 septembre 2021, deux moines de la communauté capucine d’observance traditionnelle sont pris en flagrant délit par les gendarmes alors qu’ils tentaient de mettre le feu à un pylône téléphonique. Ils reconnaissent alors avoir mis le feu à un premier pylône téléphonique, la veille, à Saint-Forgeux, « pour prémunir la population des effets nuisibles » de la 5G148,149.
Déploiement de la 5G
Allemagne
Du 19 mars au 12 juin 2019, les enchères pour la 5G se sont déroulées entre les quatre opérateurs en lice, Deutsche Telekom, Vodafone, Telefónica et 1&1 Drillisch (en). Le président de l’agence fédérale allemande des réseaux, Jochen Homann, déclare que la vente aux enchères est un succès, celle-ci rapportant 6,55 milliards d’euros à l'État allemand150.
En juin 2020, à l'occasion de son plan de relance, l'Allemagne engage 7 milliards d'euros pour accélérer le déploiement de la 5G, qui est classé au rang de haute priorité. La technologie est « l'occasion de renforcer notre souveraineté numérique et en même temps la puissance d'innovation de nos entreprises »151.
Belgique
L'opérateur Proximus a lancé le déploiement de la 5G au 1er avril 2020 dans certaines villes de Belgique. La capitale, Bruxelles, n'est pas encore directement concernée à cause d'une réglementation plus stricte sur les puissances d'émission.
Corée du Sud
La Corée du Sud se positionne en tant que chef de file mondial de la 5G et prévoit d'investir plus 30 trillions de KRW (26 milliards de dollars) pour construire un réseau 5G à l’échelle du pays d’ici 2022.
Le 3 avril 2019, la Corée du Sud devient la première nation dont le réseau est entièrement équipé pour la 5G. Les trois opérateurs de télécommunications, SK Telecom, KT et LG Uplus, annoncent simultanément le lancement du service. Quelques jours plus tard on dénombre plus de 100 000 abonnés avec des mobiles de la marque Samsung152.
En avril 2019, le réseau 5G de KT est prêt à l'usage dans 85 villes de Corée du Sud et comprend la couverture des services 5G sur les principales autoroutes et chemin de fer du pays153.
KT a déployé son infrastructure 5G sur une base Samsung. SK Telecom déploie avec Ericsson, Nokia et Samsung (Huawei est exclue de sa liste de fournisseurs d'équipement). LG Uplus utilise Huawei153.
Au premier trimestre 2020, la Corée du Sud compte déjà plus de 5 millions d'abonnements enregistrés154.
Selon Bloomberg, en 2020, à la suite de la pandémie de Covid-19, le gouvernement sud-coréen dévoile un « nouvel accord » pour remodeler l'économie ; ce plan vise en particulier à promouvoir l’utilisation des réseaux sans fil de cinquième génération et de l'intelligence artificielle dans tous les secteurs.
États-Unis
AT&T (155 millions de clients), Verizon (118 millions) et le nouvel ensemble T-Mobile/Sprint (80 millions)155 sont les principaux opérateurs de télécommunications des États-Unis.
Début 2020, le réseau 5G de Sprint est en service dans certaines parties d'Atlanta, Houston, Dallas-Fort Worth, Kansas City, Phoenix, Arizona, la ville de New York, Washington D.C., Los Angeles, Chicago. La 5G de Sprint couvre plus de 5 400 kilomètres carrés desservant une population de 11 millions d'habitants aux États-Unis156. Après de nombreuses péripéties, en juillet 2019, le ministère de la Justice américain annonce donner son accord à la fusion de Sprint et T-Mobile155. La fusion est finalisée le 1er avril 2020 ; la nouvelle société conserve le nom de T-Mobile. La fusion T-Mobile/Sprint est motivée par l'arrivée de la 5G, déjà une réalité dans plusieurs villes des États-Unis, la nouvelle société s'engage sur une couverture 5G sur 99 % du territoire américain six ans après la fusion.
En mai 2020, le réseau 5G (nommé 5G+) de AT&T et celui de Verizon sont mis en service dans certaines villes157,158. Verizon passe une importante commande 5G à Samsung pour 6,6 milliards de dollars et pénalise les résultats de Nokia, un autre de ses fournisseurs159.
Les États-Unis sont un des rares pays à avoir lancé la 5G sur des basses fréquences. AT&T et T-Mobile, les deux opérateurs qui ont déployé beaucoup de stations 5G sur des bandes de faible largeur, proches des 700 MHz, n’offrent pas un gros gain en débit par rapport à la 4G160.
France
Le 26 février 2020, les quatre principaux opérateurs français se portent candidats pour le déploiement de la 5G161, Bouygues Telecom, Free, Orange et SFR ont déposé leur candidature dans le cadre de l’attribution des fréquences, a annoncé l’Arcep.
Le prix de chaque bloc de 50 MHz a été fixé à 350 millions d’euros, avec un engagement des opérateurs de respecter un calendrier de couverture du territoire en 5G par opérateur162 :
3 000 sites en 2022 ;
8 000 sites en 2024 ;
10 500 sites en 2025 ;
couverture progressive du réseau routier.
La 5G ne sera donc pas installée sur tout le territoire tout de suite : 10 500 antennes par opérateur, soit 42 000 antennes, seront déployées d’ici à 2025 sur les 85 000 sites déjà existants163. Grâce à des données communiquées par l'Agence nationale des fréquences, il est possible de connaître l'arrivée de la 5G à proximité d'une adresse164. Si la 5G est dans un premier temps disponible dans les principales villes de France, le déploiement sera progressif et la France devrait être intégralement couverte en 5G ou équivalent (240 Mbit/s) à l'horizon 2030 d'après les prévisions de l'Arcep165.
Les enchères d’attribution des fréquences entre Orange, SFR, Bouygues Telecom et Iliad (Free), qui devaient se tenir le 21 avril 2020, sont reportées166 au 29 septembre 2020167. En contrepartie d’un cahier des charges plus souple sur le déploiement de la 5G (levant l’obligation de couvrir au moins deux villes avant la fin 2020), l’Autorité de régulation des communications électroniques, des postes et de la distribution de la presse (Arcep) renforce les obligations des opérateurs concernant la 4G, imposant « la généralisation de l’accès à la 4G+ » (LTE Advanced), une version plus puissante du LTE qui devra couvrir 75 % des sites fin 2022168.
Pour le déploiement de la 5G, Orange a choisi, pour la France, Nokia (40 %) et Ericsson (60 %) qui étaient déjà ses fournisseurs pour les générations précédentes de réseau mobile. Free a annoncé un accord stratégique avec Nokia, son fournisseur historique. SFR et Bouygues Telecom, qui ont chacun une moitié de leurs réseaux actuels équipés par Huawei, n'ont pas dit avec qui ils travailleraient pour la 5G169.
Bouygues Telecom redoute que l'État lui interdise d'avoir recours à l'équipementier chinois Huawei pour la 5G alors que celui-ci équipe déjà la moitié de son réseau 4G. Selon Olivier Roussat, président de Bouygues Telecom « Si Huawei est interdit en France (...) il faut des mesures d'indemnisation. Aux États-Unis, un fonds de 1 milliard de dollars a été mis en place pour aider les petits opérateurs régionaux à retirer les équipements Huawei de leurs réseaux »170. En août 2020, Bouygues Télécom annonce qu'il va retirer 3 000 antennes de téléphonie mobile Huawei dans les zones très denses en population d'ici à 2028, à la demande du gouvernement français, pour des raisons de sécurité informatique171. Le 5 février 2021, le Conseil constitutionnel valide les dispositions de le loi du 1er août 2019 qui avait conduit l'Agence nationale de la sécurité des systèmes d'information (Anssi) à restreindre les autorisations d’exploitation accordées à Huawei172.
En octobre 2020, l'État vend 31 blocs de fréquences pour la 5G, de 10 MHz chacun, pour un montant total de 2,8 milliards d'euros, payables sur une durée de 15 ans173,174,175. Peu après, Orange annonce les tarifs de ses premiers forfaits 5G176.
Part des fréquences attribuées en France par opérateur177
Opérateur
MHz attribuées
Orange
90
SFR
80
Bouygues Telecom
70
Free
70
En octobre 2020, à la suite de plusieurs collectivités locales, comme l'Assemblée de Corse en août, la métropole de Bordeaux fin septembre et la municipalité de Saint-Herblain, près de Nantes, la mairie de Lille adopte un moratoire sur la 5G dans l'attente du rapport de l’Anses prévu en 2021 concernant les risques sanitaires de cette nouvelle technologie. Ces décisions pourraient être attaquables juridiquement, car le déploiement de la 5G dépasse les compétences des autorités locales. Elles permettent de poursuivre le débat sur cette nouvelle technologie178.
En janvier 2021, selon l’Arcep, depuis le résultat des enchères sur les fréquences 3,5 GHz, les sites activés par les opérateurs français sur cette bande de fréquences sont au nombre de : 579 pour Orange, 322 pour Free, 145 pour Bouygues Telecom et 152 pour SFR. Les opérateurs se servent par ailleurs des fréquences déjà utilisées pour la 4G pour annoncer plus de sites « 5G »179,180.
En janvier 2021, la municipalité de Paris annonce un accord avec les opérateurs qui permettra le déploiement commercial de la 5G dans la capitale180.
Madagascar
En 2019, un contrat commercial signé avec Ericsson, d'un montant de 100 millions de dollars, prévoit sur quatre ans le déploiement de 2 000 sites mobiles qui permettront à l’opérateur télécoms de compléter sa couverture réseau du pays. Le déploiement de sites 4.5G puis 5G dans des zones à haute densité est prévu181.
L'opérateur Telma annonce le lancement commercial de son réseau 5G le 1er juillet 2020, en partenariat avec Ericsson182.
Royaume-Uni
En 2020, 31 villes du Royaume-Uni sont équipées en 5G. En janvier 2020, le Royaume-Uni pose des garde-fous sur le déploiement de la 5G par Huawei, aucun équipement dans les cœurs de réseaux, part de marché limitée à 35 % et aucune présence sur les sites critiques, comme les centrales nucléaires183.
En juin 2020, selon le Daily Telegraph, Boris Johnson prévoirait une désinstallation progressive des équipements 5G de Huawei d'ici 2023. EE, Vodafone et 3 utilisent des équipements 5G de Huawei sur leurs réseaux183.
En juillet 2020, Le Royaume-Uni va exclure Huawei de son réseau 5G. L’achat de nouveaux équipements Huawei sera interdit dès la fin 2020 et les équipements existants devront être retirés d’ici à 2027, a déclaré le ministre chargé de la culture et du numérique, Oliver Dowden, à la Chambre des communes à l’issue d’une réunion du Conseil de sécurité nationale (NSC) présidée par le premier ministre conservateur Boris Johnson184.
Suède
Quatre opérateurs ont été retenus pour l'adjudication des fréquences 2,3 et 3,5 gigahertz aux enchères : Telia, Hi3G Access (3), Net4Mobility (Telenor/Tele2) et Teracom185.
La Suède va interdire les nouveaux équipements de télécommunication des groupes chinois Huawei et ZTE de son nouveau réseau 5G au nom de la sécurité nationale. Les équipements déjà installés devront être retirés au plus tard le 1er janvier 2025185.
Suisse
Sunrise et Swisscom ont commencé le déploiement de la 5G en mars 2019, Salt plus tard dans l'année.
Lors de la présentation du résultat financier du troisième trimestre 2019186, Swisscom ambitionnait de couvrir 90 % de la population avant la fin de l'année. Ces objectifs ont ensuite été revus à la baisse187 du fait de divers ralentissements par certains cantons qui ont mis en place des moratoires, bien que cela ne relève pas de leur compétence188.
Sunrise se présente comme leader en matière de déploiement de la 5G. En octobre 2019, il couvrait 309 localités en 5G. Il propose plusieurs services grâce à ce réseau, comme Internet/TV/téléphone à la maison par la 5G189.
Notes et références
(en) Pulkit Gupta, « Evolvement of mobile generations: 1G To 5G », International Journal For Technological Research In Engineering, vol. 1, no 3, novembre 2013 (ISSN 2347-4718, lire en ligne [archive] [PDF]).
Ericsson, « 5G vers la fin du temps de latence ? » [archive], Les Échos, 17 juillet 2019 (consulté le 30 juin 2020).
« Avec un débit ultra-haut et des temps de latence faible, la 5G et la vie future » [archive], sur reneelab.fr, 12 août 2019.
« la 5G joue son avenir en pleine pandémie de Covid-19 » [archive] , Le Monde, 19 avril 2020.
« La 5G devrait vous faire rêver », Le Monde, 25 février 2014 (lire en ligne [archive] ).
« Alcatel et le Coréen KT partenaires dans la 5G mobile » [archive], Les Échos, 19 mai 2015 (consulté le 21 mai 2015).
« Technologies clés 2020 : Préparer l'industrie du futur » [archive] [PDF], mai 2016.
Éric Gibory, Fawzi Nashashibi, « Flottes d’entreprise : « De nouveaux services pour la voiture connectée vont apparaître avec la 5G » » [archive] , Le Monde, 24 octobre 2019 (consulté le 25 mai 2020)
(en) « China Poised to Lead the World in 5G » [archive], sur sdxcentral.com.
(en) Corinne Reicher, « Huawei and NTT DoCoMo trial 5G tech » [archive], sur ZDNet, 23 mai 2018lddll.
« Technologies 5G : l’ARCEP autorise Orange à mener une première expérimentation en France » [archive], sur arcep.fr, 22 septembre 2015.
« Rennes va tester la 5G » [archive], sur zdnet.fr, 26 juillet 2016.
(en) « Leti To Demonstrate New Multicarrier Waveform For 5g Networks On Minatec Campus » [archive], sur embedded-computing.com, 10 janvier 2017 (consulté le 14 mai 2017).
« 5G : Orange et Ericsson atteignent un débit de 15 Gbit/s lors d'une démonstration », MonPetitForfait, 27 janvier 2017 (lire en ligne [archive], consulté le 18 juin 2018).
Frédéric Djardias, « En Corée du Sud, les JO servent de terrain de jeu pour tester la 5G » [archive], sur francetvinfo.fr, 19 février 2018.
« L'Arcep publie la synthèse des contributions à la consultation publique « De nouvelles fréquences pour le très haut débit dans les territoires, pour les entreprises, la 5G et l'innovation » lancée le 6 janvier 2017 » [archive], sur arcep.fr, 22 juin 2017.
(en) « San Marino set to become first country upgraded to 5G nationwide » [archive], sur Financial Times.
(en) « iCOMPET: EU flagship initiative, the 5G declaration signed by EU ministers in Tallinn » [archive], Estonian Presidency of the Council of the European Union, 18 juillet 2017 (consulté le 1er novembre 2017).
Free Mobile a été autorisé à expérimenter son réseau 5G [archive] frandroid.com, le 18 octobre 2017.
(en) « Verizon to launch 5G residential broadband services in up to 5 markets in 2018 » [archive], Verizon Communications Inc., 29 novembre 2017 (consulté le 30 novembre 2017).
(en) Corinne Reichert, « 5G standards approved as tech industry signals accelerated deployment » [archive], sur ZDNet, 21 décembre 2017.
AT&T promet de la 5G mobile dès fin 2018 [archive], generation-nt.com.
Frédéric Djardias, « Internet 5G à Pyeongchang : réalité virtuelle en direct et lutte anti-sangliers » [archive], 22 février 2018.
« La 5G en panne en Europe », euractiv.com, 5 mars 2018 (lire en ligne [archive], consulté le 7 mars 2018).
« Télécoms : l'Europe à la traîne dans la 5G » [archive], Les Échos (consulté le 16 mars 2018).
Sébastien Gavois, « Les lourdeurs du trilogue européen pointées du doigt », nextinpact.com, 13 mars 2018 (lire en ligne [archive], consulté le 15 mars 2018).
« Les premières antennes 5G testées en Chine » [archive], 3 septembre 2018.
« Les premiers terminaux 5G devraient arriver l'année prochaine » [archive], sur Le Quotidien du Peuple, 24 avril 2018.
(es) Mike Cortez, « América Latina Se Prepara Para La Llegada Del 5G », Latam Outsource, 20 mars 2018 (lire en ligne [archive]).
« Afrique : le petit royaume du Lesotho choisi pour tester la 5G » [archive], sur Europe 1, 8 septembre 2018.
Ali Saoucha N (2020) Exploitation des techniques de l’intelligence artificielle pour l’optimisation de la QoS et l’efficacité spectrale dans les réseaux de radio cognitive [archive] (thèse de doctorat, 4 mars 2020).
Fisseha Mekuria et Luzango Mfupe, « Spectrum Sharing for Unlicensed 5G Networks », 2019 IEEE Wireless Communications and Networking Conference (WCNC), Institute of Electrical and Electronics Engineers, avril 2019, p. 1–5 (ISBN 978-1-5386-7646-2, DOI 10.1109/WCNC.2019.8885763, lire en ligne [archive], consulté le 7 octobre 2020).
Kavé Salamatian, « Trump contre Huawei : enjeux géopolitiques de la 5G », Hérodote, nos 177-178, 2020, p. 197 (ISSN 0338-487X et 1776-2987, DOI 10.3917/her.177.0197, lire en ligne [archive], consulté le 7 octobre 2020).
« Comment Swisscom, Sunrise et Salt se partageront la 5G suisse » [archive], sur ictjournal.ch (consulté le 19 février 2019).
Zeliha Chaffin, « Téléphonie : la 5G, vedette du Salon de Barcelone », Le Monde, 23 février 2019 (lire en ligne [archive], consulté le 23 février 2019).
« La Corée du Sud devient le premier pays au monde à commercialiser la 5G » [archive], RFI, 4 avril 2019.
« « 5G for People » est lancé : les premiers clients Sunrise utilisent la 5G » [archive], sur Sunrise, 4 avril 2019 (consulté le 4 avril 2019).
« Couverture Sunrise 5G en Suisse » [archive], sur Sunrise (consulté le 13 mai 2019).
« Découvrez sur notre carte si une antenne 5G se situe près de chez vous » [archive], sur Radio télévision suisse, 17 avril 2019 (consulté le 18 avril 2019).
« Coup d'envoi de l'attribution des fréquences 5G en France » [archive], sur MonPetitForfait, 17 juillet 2019 (consulté le 19 juillet 2019).
« Fréquences 5G : procédure d'attribution de la bande 3,4 - 3,8 GHz » [archive], sur Arcep, 16 novembre 2020.
(en) Ewan Sutherland, « 5G Security – The Politics of Huawei Equipment in the United Kingdom », SSRN Electronic Journal, 2020 (ISSN 1556-5068, DOI 10.2139/ssrn.3654596, lire en ligne [archive], consulté le 7 octobre 2020).
« L'attribution des licences 5G reportée finalement au printemps 2020 » [archive], sur BFM Business (consulté le 22 novembre 2019).
« La 5G déployée en France » [archive], sur anfr.fr (consulté le 3 août 2021)
Sylvain Rolland, « Comment le numérique pollue dans l'indifférence générale » [archive], La Tribune, 18 décembre 2018 (consulté le 2 août 2019).
Frédéric Bordage, Sobriété numérique, les clés pour agir, Buchet Chastel, p. 29 et 48.
(en) Li-Chun Wang et Suresh Rangapillai, « A survey on green 5G cellular networks » [archive], sur researchgate.net, juillet 2012 (DOI 10.1109/SPCOM.2012.6290252), p. 1-5.
(en) « Toward Green 5G Mobile Networks (5GrEEn) - new project launched » [archive], sur eitdigital.eu, 18 janvier 2013.
« La 5G dans les starting-blocks » [archive], ZDNet, 29 janvier 2015.
(en) « Ericsson hits crazy-fast 5Gbps wireless speed in 5G trial » [archive], sur cnet.com, 1er juillet 2014.
« Le CEA-Leti mise sur les technologies spatiales pour tester la 5G aux JO… de 2018 » [archive], sur usine-digitale.fr, 6 août 2016 (consulté le 21 août 2017).
Nicolas Richaud, « Saint-Marin sur le point de devenir la première nation 5G » [archive], Les Échos, 17 juillet 2017.
Smart Tech [archive], Delphine Sabattier, David Barruchel, Nicolas Sironneau, Viktor Arvidsson (15 juillet 2020) B Smart..
Nicolas Sironneau, « La 5G : prendre le virage du monde d’après » [archive], sur Fondation Concorde, mars 2020.
« Tout savoir sur la 5G : éligibilité, débits, dangers... [Guide complet] » [archive], sur Forfait 5G (consulté le 22 août 2019).
Arnaud Montebourg, propos recueillis par Christian Chavagneux, « La mondialisation doit faire l'objet d'un débat démocratique », Alternatives économiques, no 407, 1er décembre 2020.
Pascal Samama, « 5G : Les États-Unis misent-ils sur Cisco pour affronter Huawei ? » [archive], sur BFM TV, 20 février 2019.
Pierre Manière, « 5G : pourquoi Washington s'intéresse à Nokia et Ericsson » [archive], La Tribune, 7 février 2020.
« La France accueille favorablement la publication de la « boîte à outils 5G », Agence nationale de la sécurité des systèmes d'information » [archive], sur ssi.gouv.f, 29 janvier 2020.
Pia de Bondy, « Un nouveau paradigme pour la 5G européenne » [archive], sur portail-ie.fr, 11 février 2020.
Amélie Charnay et Gilbert Kallenborn, « La 5G pose-t-elle un problème de sécurité nationale ? » [archive], sur 01net, 20 février 2019.
« Proposition de loi no 1722 visant à préserver les intérêts de la défense et de la sécurité nationale de la France dans le cadre de l'exploitation des réseaux radioélectriques mobiles » [archive], sur assemblee-nationale.fr, 20 février 2019.
AOF, « Nokia, l'État finlandais prend une participation de 3,3 % au capital » [archive], sur Capital.fr, 13 mars 2018 (consulté le 22 juillet 2020).
« Les titres de la presse du vendredi 3 juillet 2020 » [archive], sur Autorité de régulation des communications électroniques, des postes et de la distribution de la presse, 3 juillet 2020.
« « Il n’y aura pas un bannissement total de Huawei » dans la 5G en France, prévient le patron de l’ANSSI » [archive], Le Monde, AFP, Reuters, 5 juillet 2020 (consulté le 6 juillet 2020).
Yannick Chavanne et Fabian Kindle, « L'Italie ne veut pas de Huawei pour la 5G : la Suisse en Sonderfall ? » [archive], 26 octobre 2020 (consulté le 23 novembre 2020).
« 5G : la Chine menace Nokia et Ericsson » [archive], Capital, 21 juillet 2020 (consulté le 28 août 2020).
(en) Alexandra Witze, « Global 5G wireless networks threaten weather forecasts », Nature, vol. 569, 26 avril 2019 (DOI 10.1038/d41586-019-01305-4, lire en ligne [archive]).
(en) Alexandra Witze, « Global 5G wireless deal threatens weather forecasts », Nature, vol. 575, 22 novembre 2019 (DOI 10.1038/d41586-019-03609-x, lire en ligne [archive]).
Olivier Lascar, « Quand la 5G menace les prévisions météo » [archive], sur Sciences et Avenir, 12 novembre 2019 (consulté le 17 janvier 2020).
Sarah Crespi et Gabriel Popki, Next-generation cellphone signals could interfere with weather forecasts, and monitoring smoke from wildfires to model nuclear winter [archive], Science, 8 août 2019.
(en) Centre européen pour les prévisions météorologiques à moyen terme(ECMWF), « ECMWF statement on the outcomes of the ITU WRC-2019 conference » [archive], sur le site du Centre européen pour les prévisions météorologiques à moyen terme, 25 novembre 2019 (consulté le 29 novembre 2019).
ITU, « Conférence mondiale des radiocommunications de 2019 (CMR-19), Charm el-Cheikh, Égypte, 28 octobre-22 novembre 2019 » [archive], sur le site de l'Union internationale des télécommunications, novembre 2019 (consulté le 29 novembre 2019).
« Non, la 5G n'affectera pas les prévisions météo » [archive], sur ZDNet France (consulté le 17 janvier 2020).
Sandy Dauphin, « La 5G pourrait augmenter significativement les émissions de CO2 de la France, d'après un nouveau rapport » [archive], sur France Inter, 19 décembre 2020 (consulté le 19 décembre 2020).
« Champs électromagnétiques et santé publique : téléphones portables » [archive], Organisation mondiale de la santé, 8 octobre 2014.
(en) Mike Wood, « Small cells bringing fast mobile coverage to where it’s needed most » [archive], sur Telstra Exchange, 15 avril 2019.
(en) James Meese, Jordan Frith et Rowan Wilken, « COVID-19, 5G conspiracies and infrastructural futures », Media International Australia, 27 août 2020 (ISSN 1329-878X et 2200-467X, PMCID PMC7506181, DOI 10.1177/1329878X20952165, lire en ligne [archive], consulté le 23 septembre 2020).
Sébastien Meurs, « 5G L'ultra haut débit mobile sera-il-dangereux pour la santé ? » [archive], Capital, 6 août 2018.
Julien Lausson, « La 5G, des effets sur la santé ? Le gouvernement rassure » [archive], sur Numerama, 20 août 2018 (consulté le 28 avril 2019).
« 5G et santé: lectrices et lecteurs du Temps s’interrogent » [archive], Le Temps, 1er avril 2019 (consulté le 28 avril 2019).
« 5G, la décision du Conseil fédéral qui divise » [archive], sur illustre.ch, 19 février 2019 (consulté le 28 avril 2019).
Le Jura opte lui aussi pour la prudence face aux antennes de la 5G [archive], RTS Info, avril 2019.
Anouch Seydtaghia, « La fronde anti-5G, une particularité suisse », Le Temps, 14 avril 2019 (ISSN 1423-3967, lire en ligne [archive], consulté le 28 avril 2019).
(en) « Marie-Claire Cammaerts's research » [archive], sur researchgate.net.
La 5G est-elle dangereuse pour la santé ? Les scientifiques sonnent l'alarme [archive], fr.express.live.
De Nantes à Besançon, les candidats « anti-5G » font irruption aux municipales [archive], Les Échos, 25 juin 2020.
« Déploiement de la 5G en France : l’Anses se mobilise pour évaluer les risques pour la santé » [archive], sur Agence nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail, 27 janvier 2020.
Loi no 2015-136 du 9 février 2015 relative à la sobriété, à la transparence, à l'information et à la concertation en matière d'exposition aux ondes électromagnétiques [archive].
« Rapport au Parlement sur l'électro-hypersensibilité » [archive] [PDF], sur Ministère des Solidarités et de la Santé, octobre 2019.
Stéphane Mandard, « 5G : l’impartialité du comité qui guide l’Europe pour protéger la population des ondes en question » [archive], Le Monde, 19 juin 2020.
« Déploiement de la 5G en France et dans le monde : aspects techniques et sanitaires » [archive] [PDF], sur Ministère de l'Économie, des Finances et de la Relance, septembre 2020.
Sébastien Dumoulin, « 5G : le gouvernement veut aller de l'avant » [archive], Les Échos, 15 septembre 2020.
« 5G : pas de risques nouveaux pour la santé au vu des données disponibles » [archive], sur Agence nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail, 20 avril 2021.
« Évaluation de l’exposition du public aux ondes électromagnétiques 5G » [archive] [PDF], sur Agence nationale des fréquences, avril 2020.
Mélenn Gautier, « La 5G est-elle « extrêmement consommatrice d’énergie », comme l'affirme Julien Bayou ? » [archive], sur Libération, CheckNews, 17 juillet 2020.
« La 5G risque d’augmenter les émissions de CO2, alerte le Haut Conseil pour le Climat » [archive], L'Obs (consulté le 19 décembre 2020).
Sébastien Dumoulin, « 5G : le Haut Conseil pour le Climat prédit un bond des émissions de CO2 » [archive], Les Échos, 19 décembre 2020.
Haut Conseil pour le climat, « Maitriser l'impact carbone de la 5G » [archive] [PDF], décembre 2020, encadré page 13.
« La technologie 5G : pourquoi elle va changer le monde de demain ? » [archive], sur TopMeilleurs, 20 mai 2020 (consulté le 5 juillet 2020).
« Doit-on s’attendre à une couverture 5G inférieure à celle de la 4G ? » [archive], sur Tactis.fr, 4 février 2020.
« Parlons 5G : toutes vos questions sur la 5G » [archive], sur Autorité de régulation des communications électroniques, des postes et de la distribution de la presse, 18 septembre 2020.
(en) « Samsung to offer 5G service by 2020 »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) - Yonhapnews Agency, 12 mai 2013.
(en) « Samsung wants to offer 5G in 2020, speeds of 1 Gbit/s reached in tests »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) - pocket-lint.com, 12 mai 2013.
Téléphonie mobile : Samsung teste avec succès un réseau 5G à 1 Gbit/s [archive] - Marc Zaffagni, Futura-Sciences.com, 15 mai 2013.
« Nouveau record de vitesse en 5G : vous téléchargerez 27 films en une seconde ! » [archive], sur 01net, 26 février 2015.
(en) [PDF] [1] [archive] etsi.org, novembre 2019.
(en) [PDF] [2] [archive] etsi.org, décembre 2020.
(en) « Major European 5G trials and pilots » [archive], sur 5gobservatory.eu (consulté le 27 février 2021).
« La Chine prépare déjà la 5G » [archive], sur 01net, 12 novembre 2013.
« Télécoms : Bruxelles déjà en piste pour la « 5G » » [archive], Les Échos, 26 février 2013.
liste des partenaires de METIS [archive], consultée 3 mars 2014.
5G : Bruxelles accentue ses efforts [archive] - Numerama, 21 décembre 2013.
Huawei toutes voiles dehors vers la 5G [archive] - Johann Breton, lesnumeriques.com, 7 novembre 2013.
(en) J. Hoydis, S. ten Brink et M. Debbah, « Massive MIMO in the UL/DL of Cellular Networks: How Many Antennas Do We Need? » [archive], IEEE Journal on Selected Areas in Communications, vol. 31, no 2, Bell Labs., Alcatel-Lucent, février 2013 (consulté le 2 mars 2016), p. 160–171.
(en) E. Bjornson, E. G. Larsson et M. Debbah, « Massive MIMO for Maximal Spectral Efficiency: How Many Users and Pilots Should Be Allocated? » [archive], IEEE Transactions on Wireless Communications, vol. 15, no 2, Institute of Electrical and Electronics Engineers, février 2016 (consulté le 2 mars 2016), p. 1293-1308.
(en) E. Bjornson, L. Sanguinetti, J. Hoydis et M. Debbah, « Optimal Design of Energy-Efficient Multi-User MIMO Systems: Is Massive MIMO the Answer? » [archive], IEEE Transactions on Wireless Communications, vol. 14, no 6, Institute of Electrical and Electronics Engineers, juin 2015 (consulté le 2 mars 2016), p. 3059-3075.
« La Corée du Sud investit plus d'un milliard d'euros dans la 5G », Le Monde, 22 janvier 2014 (lire en ligne [archive], consulté le 21 mai 2015).
« 5G : Orange et Bouygues Telecom ont obtenu le feu vert de l’Arcep ! » [archive], sur actu.meilleurmobile.com, 4 mars 2018.
« 5G : la France représente bien l’Europe aux côtés du Royaume-Uni et de l’Allemagne » [archive], sur actu.meilleurmobile.com, 19 avril 2018.
« L’appel de 1 000 scientifiques : « Face à la crise écologique, la rébellion est nécessaire » », Le Monde, 20 février 2020 (lire en ligne [archive]).
(en) Naomi Buck, « Could WiFi in schools be harming our kids? » [archive], The Globe and Mail, 11 mai 2014.
(en) Christopher Mims, « Cities Are Saying No to 5G, Citing Health, Aesthetics—and FCC Bullying » [archive], The Wall Street Journal, 24 août 2019.
(en) « Radiation concern halts Brussels 5G development, for now » [archive], The Brussels Times (en), 1er avril 2019.
Pierre Manière, « Santé : des associations tirent à boulets rouges sur la 5G » [archive], La Tribune, 25 février 2020.
« Les Français soutiennent-ils le déploiement de la 5G en France ? » [archive], sur lemon.fr, 16 septembre 2020.
Hugues Ferreboeuf et Jean-Marc Jancovici, « La 5G est-elle vraiment utile ? » [archive], sur Le Monde, 9 janvier 2020.
Sébastien Dumoulin, « 5G : les ondes de la colère » [archive], Les Échos, 5 mars 2020.
Frédéric Sergeur, « 5G : « Je ne crois pas au modèle amish », le tacle d’Emmanuel Macron aux écologistes » [archive], Capital, 14 septembre 2020 (consulté le 15 septembre 2020).
(en) « Your 5G Phone Won’t Hurt You. But Russia Wants You to Think Otherwise. » [archive], The New York Times, 12 mai 2019.
(en) Sabrina Weiss, « health risks are the internet's new favourite conspiracy theory » [archive], Wired, 12 juin 2019.
« 5G et coronavirus : propagation d'une infodémie » [archive], sur siecledigital.fr, 17 avril 2020 (consulté le 23 septembre 2020).
« COVID-19 et 5G : des chercheurs montrent comment cette fake news s'est propagée dans le monde » [archive], sur Radio-télévision belge de la Communauté française, 9 août 2020.
Ogilvie, M, Rootes, C (2016) The British anti-windfarm and anti-fracking movements: a comparative analysis. In:Price, S, Sanz Sabido, R (eds) Sites of Protest: Protest, Media and Culture. London: Rowman & Littlefield, p. 143–162.
Taylor V (2016) Contention, tactical repertoires of. In: Ritzer, G (ed.) The Blackwell Encyclopedia of Sociology, p. 779–782. Malden, MA: Blackwell Publisher.
Weingart, Engels and Pansegrau (2000) Risks of communication: discourses on climate change in science, politics and the mass media. Public Understanding of Science 9: 261–283.
(en-GB) Suzanne Goldenberg, « Conservative thinktanks step up attacks against Obama's clean energy strategy », The Guardian, 8 mai 2012 (ISSN 0261-3077, lire en ligne [archive], consulté le 23 septembre 2020).
(en) Alex Shultz, « Here’s the bonkers conspiracy theory blaming 5G for the coronavirus » [archive], GQ, 7 avril 2020.
(en) Isobel Asher Hamilton, « Here’s what we know about the bizarre coronavirus 5G conspiracy theory that is leading people to set mobile phone masts on fire » [archive], Business Insider Australia, 6 avril 2020.
(en) « 5G, coronavirus and contagious superstition », The Guardian, 26 avril 2020 (lire en ligne [archive], consulté le 23 septembre 2020).
(en) James Temperton, « How the 5G coronavirus conspiracy theory tore through the internet » [archive], Wired, 6 avril 2020.
(en) Ryan Broderick, « A conspiracy theory that 5G is causing the coronavirus is spreading alongside the pandemic » [archive], sur BuzzFeed, 3 avril 2020.
(en) Axel Bruns, Stephen Harrington et Edward Hurcombe, « ‘Corona? 5G? or both?’: the dynamics of COVID-19/5G conspiracy theories on Facebook », Media International Australia, 4 août 2020 (ISSN 1329-878X et 2200-467X, PMCID PMC7404088, DOI 10.1177/1329878X20946113, lire en ligne [archive], consulté le 23 septembre 2020).
(en) Jim Waterson, « Revealed: ‘former Vodafone executive’ in 5G conspiracy video is UK pastor » [archive], The Guardian, 24 avril 2020.
(en) Ryan Gallagher, « 5G virus conspiracy theory fuelled by coordinated effort » [archive], sur Bloomberg, 9 avril 2020.
« Tableau de bord des expérimentations 5G en France » [archive], sur Autorité de régulation des communications électroniques, des postes et de la distribution de la presse (consulté le 23 septembre 2020).
« Les ondes émises par les antennes 5G très inférieures au seuil légal » [archive], sur siecledigital.fr, 15 avril 2020 (consulté le 23 septembre 2020).
« Deux moines contre la 5G mis en examen pour avoir ciblé des antennes-relais », Le Monde, 20 septembre 2021 (lire en ligne [archive], consulté le 20 septembre 2021).
Le Parisien avec AFP, « Hostiles à la 5G, deux moines arrêtés après avoir incendié des antennes relais dans le Rhône » [archive], Le Parisien, 21 septembre 2021 (consulté le 21 septembre 2021).
« Fréquences 5G : en Allemagne, les enchères rapportent 6,55 milliards d’euros » [archive], sur Le Monde, 13 juin 2019 (consulté le 15 juin 2020)
Ninon Renaud, « L'Allemagne met 7 milliards sur la table pour accélérer dans la 5G » [archive], Les Échos, 5 juin 2020 (consulté le 26 juin 2020)
« La Corée du Sud leader mondial de la 5G » [archive], sur s-ge.com, 3 mai 2019 (consulté le 23 juillet 2020).
Campbell Kwan, « 5G : le réseau commercial de KT et Samsung atteint 1 Gb/s à Séoul » [archive], sur ZDNet, 3 avril 2019 (consulté le 23 juillet 2020).
Tristan Gaudiaut, « La Corée du Sud fait la course en tête » [archive], sur statista.com, 14 juillet 2020 (consulté le 23 juillet 2020).
Raphael Balenieri, « La justice américaine valide la méga-fusion entre T-Mobile et Sprint » [archive], sur Les Échos, 26 juillet 2019 (consulté le 26 juin 2020).
(en) « Sprint 5G Rollout: Here's Everything You Need to Know » [archive], sur digitaltrends.com, 1er novembre 2019 (consulté le 23 juin 2020).
(en) Ed Oswald, Christian de Looper, « AT&T 5G: Everything You Need to Know About the Rollout » [archive], sur digitaltrends.com, 27 mai 2020 (consulté le 23 juin 2020).
(en) « Verizon 5G Rollout: Here's Everything You Need to Know » [archive], sur digitaltrends.com, 28 mai 2020 (consulté le 23 juin 2020).
Raphaël Balenieri, « 5G : Ericsson profite des difficultés de Huawei et Nokia » [archive], Les Échos, 9 octobre 2020 (consulté le 16 novembre 2020).
Nicolas Six, « Tour du monde des réseaux mobiles 5G : les particuliers ne sont pas conquis » [archive], Le Monde, 17 septembre 2020 (consulté le 19 septembre 2020).
Vincent Fagot, « 5G : les quatre principaux opérateurs français se portent candidats », Le Monde, 25 février 2020 (lire en ligne [archive]).
« La 5G déployée en France » [archive], sur Agence nationale des fréquences (consulté le 26 août 2021).
Mathilde Damgé, « Qu’est-ce que la 5G va changer pour les particuliers ? » [archive], Le Monde, 19 septembre 2020 (consulté le 19 septembre 2020).
« Test 5G : localiser les antennes 5G les plus proches de chez soi » [archive], sur MonPetitForfait (consulté le 29 janvier 2021).
« 5G » [archive], sur Arcep, 16 décembre 2020.
Charles de Laubier, « La 5G joue son avenir en pleine pandémie », Le Monde, 19 avril 2020 (lire en ligne [archive]).
« Les enchères pour les fréquences 5G débuteront le 29 septembre en France », L'Usine nouvelle, 7 septembre 2020 (lire en ligne [archive], consulté le 8 septembre 2020).
« Les enchères de la 5G auront lieu entre le 20 et 30 septembre », Le Télégramme, 11 juin 2020 (lire en ligne [archive], consulté le 15 juin 2020).
Sébastien Dumoulin, « 5G : Orange fait l'impasse sur Huawei en France » [archive], Les Échos, 31 janvier 2020 (consulté le 27 juin 2020).
Raphaël Balenieri et Sébastien Dumoulin, « 5G : Martin Bouygues met le gouvernement face à ses choix » [archive], Les Échos, 10 juin 2020 (consulté le 26 juin 2020).
Nicolas Sandanassamy, « Bouygues Telecom va retirer des milliers d’antennes de téléphonie mobile Huawei » [archive], Capital, 27 août 2020 (consulté le 28 août 2020).
« 5G : le Conseil constitutionnel valide la loi « anti-Huawei » visant à préserver les intérêts de la sécurité nationale » [archive], Le Monde, 5 février 2021 (consulté le 5 février 2021).
Sébastien Dumoulin et Raphaël Balenieri, « 5G : les enchères rapportent moins de 3 milliards » [archive], Les Échos, 1er octobre 2020.
« Fréquences 5G : procédure d’attribution de la bande 3,4 - 3,8 GHz en métropole » [archive], sur Autorité de régulation des communications électroniques, des postes et de la distribution de la presse, 1er octobre 2020.
Benjamin Terrasson, « L’Arcep et l’État s’accordent pour échelonner le paiement des fréquences 5G sur 15 ans » [archive], sur siecledigital.fr, 18 décembre 2019.
Dominique Filippone, « Orange dégaine ses premiers forfaits 5G » [archive], sur Le Monde informatique, 8 octobre 2020.
« 5G : Orange rafle la mise, l'État empoche 2,8 milliards d'euros » [archive], sur Stratégies, 2 octobre 2020.
« La mairie de Lille adopte un moratoire sur la 5G » [archive], Le Monde, 10 octobre 2020 (consulté le 10 octobre 2020).
Raphaël Grably, « 5G : voici la carte des antennes déployées par les quatre opérateurs dans l’Hexagone » [archive], sur BFM TV, 17 décembre 2020 (consulté le 20 décembre 2020).
« La 5G pourrait être déployée à Paris « dans les prochaines semaines » » [archive], Le Monde, 20 février 2020 (consulté le 20 février 2020).
« Madagascar : Telma a signé un contrat de près de 100 millions de dollars avec Ericsson pour moderniser son réseau et se projeter vers la 5G » [archive], sur agenceecofin.com, 1er octobre 2019 (consulté le 2 juillet 2020).
« Telma Madagascar lance avec Ericsson les premiers services 5G en Afrique » [archive], sur agenceecofin.com, 1er juillet 2020 (consulté le 2 juillet 2020)
Raphaël Balenieri, « Le Royaume-Uni pourrait fermer ses portes à Huawei dès 2023 » [archive], Les Échos, 24 mai 2020 (consulté le 26 juin 2020).
« Le Royaume-Uni va finalement exclure Huawei de son réseau 5G » [archive], Le Monde, AFP, 14 juillet 2020 (consulté le 15 juillet 2020).
Le Monde avec AFP, « 5G : la Suède bannit à son tour les équipements des chinois Huawei et ZTE » [archive], 20 octobre 2020 (consulté le 21 octobre 2020).
« EBITDA stable – Les abonnements haut débit, TV et mobile progressent au troisième trimestre » [archive], sur swisscom.ch, Swisscom, 31 octobre 2019 (consulté le 16 novembre 2019).
Bilan, « Swisscom : retards en vue avec le déploiement de la 5G, admet le patron » [archive], sur bilan.ch, 5 septembre 2019 (consulté le 18 septembre 2019).
« Les moratoires sur les antennes 5G sont illégaux » [archive], sur 24heures.ch, 5 mai 2019 (consulté le 16 novembre 2019).
Sunrise, « Expansion de la 5G : plus de 309 villes/localités couvertes par la 5G » [archive], sur sunrise.ch, 1er novembre 2019 (consulté le 16 novembre 2019).
Voir aussi
Bibliographie
(en) Abdullah Gani, Xichun Li, Lina Yang, Omar Zakaria, Nor Badrul Anuar (2009), Multi-Bandwidth Data Path Design for 5G Wireless Mobile Internets, WSEAS Transactions on Information Science and Applications archive, vol. 6, no 2, février 2009. (ISSN 1790-0832), résumé [archive]
(en) METIS (2013), The 5G future scenarios identified by METIS –The first step toward a 5G mobile and wireless communications system [archive]
(en) METIS (2013), Deliverable D1.1 Scenarios, requirements and KPIs for 5G mobile and wireless system [archive] [PDF]
(en) METIS (2013), Deliverable D2.1 Requirement analysis and design approaches for 5G air interface [archive] [PDF]
(en) METIS (2013), Deliverable D3.1 Positioning of multi-node/multi-antenna technologies [archive] [PDF]
(en) METIS (2013), Deliverable D4.1 Summary on preliminary trade-off investigations and first set of potential network-level solutions [archive] [PDF]
(en) METIS (2013), Deliverable D5.1 Intermediate description of the spectrum needs and usage principles [archive] [PDF]
(en) METIS (2013), Deliverable D6.1 Simulation guidelines [archive] [PDF]
(en) METIS (2013), Deliverable D7.1 Academic Dissemination & Exploitation Plans [archive] [PDF]
(en) Sachi Pandey, Manoj Kumar, Atendra Panwar & Ishita Singh (2013) A Survey: Wireless Mobile Technology Generations With 5G, in International Journal of Engineering Research and Technology, vol. 2, no 4, avril 2013, ESRSA Publications (lien de téléchargement [archive]).
(en) Suvarna Patil, Vipin Patil & Pallavi Bhat (2012) A Review on 5G Technology. International Journal of Engineering and Innovative Technology[PDF] [archive] (IJEIT), 1(1), 26-30 (5 pages)
(en) Mohammed Maroof Siddiqui (2011) Vision of 5G Communication. In High Performance Architecture and Grid Computing (p. 252-256). Springer Berlin Heidelberg (résumé [archive]).
(en) Li-Chun Wang & Suresh Rangapillai (2012) A survey on green 5G cellular networks, in International Conference on Signal Processing and Communications (SPCOM) (p. 1-5). IEEE ; (ISBN 978-1-4673-2013-9) (résumé [archive]).
Articles connexes
Télécommunications
Opérateur de télécommunications
Accès à Internet à très haut débit
5G NR
5G pour l'Internet des objets
Impact sanitaire et environnemental de la 5G
Troisième révolution industrielle
Ericsson
Huawei
Nokia
ZTE
Samsung Electronics
6G
Liens externes
Notice dans un dictionnaire ou une encyclopédie généraliste
:Swedish Nationalencyklopedin [archive]
« 5G, pour quelques gigas de plus » [archive], La méthode scientifique, par Nicolas Martin, France Culture, le 10 avril 2019
« 5G, technologie à haut débat » [archive], Entendez-vous l'éco ?, par Tiphaine de Rocquigny, France Culture, en trois épisodes :29 septembre 2020 : Le progrès contre l'environnement ?
30 septembre 2020 : Le moteur d’une nouvelle révolution industrielle ?
1er octobre 2020 : 5G des villes, fibre des champs
5G : une guerre froide sino-américaine [archive], Pierre-Olivier François (producteur), Emilie Aubry (présentatrice), dans Le Dessous des cartes sur Arte (21 novembre 2020)
[masquer]
5G
Précédé par
Suivi par
4G+
5G
6G
[afficher]v · m
Normes et générations de téléphonie mobile
Portail des télécommunications
Portail de la production industrielle
Portail de l’économie
Portail de l’environnement
Uranium
Pour les articles homonymes, voir Uranium (homonymie).
L’uranium est l'élément chimique de numéro atomique 92, de symbole U. Il fait partie de la famille des actinides.
L'uranium est le 48e élément naturel le plus abondant dans la croûte terrestre6, son abondance est supérieure à celle de l'argent, comparable à celle du molybdène ou de l'arsenic, mais quatre fois inférieure à celle du thorium. Il se trouve partout à l'état de traces, y compris dans l'eau de mer.
C'est un métal lourd radioactif (émetteur alpha) de période très longue (~ 4,468 8 milliards d'années pour l'uranium 238 et ~ 703,8 millions pour l'uranium 235). Sa radioactivité, additionnée à celle de ses descendants dans sa chaîne de désintégration, développe une puissance de 0,082 watt par tonne d'uranium, ce qui en fait, avec le thorium 232 (quatre fois plus abondant, mais trois fois moins radioactif) et le potassium 40, la principale source de chaleur qui tend à maintenir les hautes températures du manteau terrestre, en ralentissant de beaucoup son refroidissement7.
L'isotope 235U est le seul isotope fissile naturel. Sa fission libère une énergie voisine de 202,8 MeV par atome fissionné dont 9,6 MeV d'énergie non récupérable, communiquée aux neutrinos produits lors de la fission. L'énergie récupérable est plus d'un million de fois supérieure à celle des combustibles fossiles pour une masse équivalente. De ce fait, l'uranium est devenu la principale matière première utilisée par l'industrie nucléaire.
La production mondiale d'uranium s'est élevée à 54 742 tonnes en 2019, réparties pour l'essentiel entre le Kazakhstan (41,7 %), le Canada (12,7 %), l'Australie (12,1 %), la Namibie (10 %), l'Ouzbékistan (6,4 %), le Niger (5,4 %), la Russie (5,3 %) et la Chine (3,4 %). En 2020, la production a chuté à 47 731 tonnes. Pour son utilisation dans les réacteurs nucléaires, les ressources récupérables à un coût inférieur à 130 dollars/kg d'uranium étaient estimées en 2019 par l'AIEA à 6,15 millions de tonnes dans le monde, réparties essentiellement entre l'Australie (28 %), le Kazakhstan (15 %), le Canada (9 %), la Russie (8 %) et la Namibie (7 %).
Uranium naturel
Le minerai d'uranium exploité dans des gisements granitiques ou sédimentaires possède une teneur moyenne en uranium pouvant varier de 0,1 % à 2 %8, pouvant exceptionnellement approcher les 20 %9. L'uranium est dit naturel quand il est constitué d'isotopes dans leur proportion d'origine (identique pour tous les minerais d'uranium) : soit 99,2743 % d'uranium 238 accompagné de 0,7202 % d'uranium 235 et d'une quantité infime d'isotope 234 (0,0055 %).
Découverte
L'uranium fut mis en évidence en 1789 par le chimiste prussien Martin Heinrich Klaproth à partir de l'analyse d'un morceau de roche qu'on lui avait apporté de la mine de Saint Joachimsthal10. Cette roche était de la pechblende, un minerai d'uranium qui contient principalement de l'U3O8. Klaproth parvint en la chauffant à en extraire un corps gris métallique. Dans sa communication du à l'Académie royale prussienne des sciences et intitulée « Ueber den Uranit, ein neues Halbmetalln 1 », il proposa le nom d'« urane » ou « uranite » au composé qu'il venait d'identifier (un oxyde d'uranium et non le corps pur), en référence à la découverte de la planète Uranus faite par William Herschel en 178111. Cet oxyde, rebaptisé uranium en 1790, avait comme propriété de donner une fine fluorescence aux verres et une couleur jaune verdâtre aux émaux, si bien que la pechblende était extraite de la mine de Joachimsthal et de mines d'étain en Cornouaille et des uranates alcalins utilisés (diuranate d'ammonium et de sodium) par les verriers de Bohême et les céramistes saxons12.
Ce n'est qu'en 1841 que le chimiste français Eugène-Melchior Péligot put l'isoler à l'état de pureté en réduisant le tétrachlorure d'uranium (UCl4) par le potassium. Il établit que l'urane était composé de deux atomes d'oxygène et d'un métal qu'il isola. L'uranium entra dans la nomenclature de la chimie. Il estima alors13 la masse volumique de l'uranium à 19 g/cm3.
Le Français Henri Becquerel ne découvrit la radioactivité de l’uranium que beaucoup plus tard, le , lorsqu'il constata que des plaques photographiques placées à côté de sels d'uranium (extraits d'un lot de pechblende de Joachimsthal) avaient été impressionnées sans avoir été exposées à la lumière. Les plaques avaient été noircies par les rayonnements émis par les sels : c'était la manifestation d'un phénomène jusqu'alors inconnu, la radioactivité naturelle. Pierre et Marie Curie isolèrent deux éléments nouveaux naturellement radioactifs, le polonium et le radium.
Gisements et exploitation
Le minerai d'uranium est appelé uraninite, ou pechblende. Les cinq plus gros producteurs au monde sont le Kazakhstan, le Canada, l'Australie, le Niger et la Namibie. À proximité des mines, l'uranium est concentré sous forme de yellowcake14. Il est néanmoins trop peu concentré en isotope fissile pour être utilisé directement dans les centrales nucléaires de type à eau pressurisée (PWR, pour pressurized water reactor). C'est la raison pour laquelle il est souvent enrichi en uranium 235 par diffusion gazeuse ou centrifugation. Les centrales de type CANDU utilisent l'uranium non enrichi mais exigent beaucoup d'eau lourde comme modérateur.
Un Centre de recherche sur la géologie de l'uranium (Cregu) a été créé dans les années 1980, à Vandœuvre-lès-Nancy pour mieux connaitre la géologie et la géochimie de l'uranium et faciliter l'accès des prospecteurs à cette ressource15, par exemple en le reliant aux discordances géologiques connues ou à découvrir16.
Abondance et répartition
L'uranium est répandu dans les profondeurs du globe terrestre. La désintégration d'uranium 238 et 235 et d'autres radionucléidesn 2 comme le thorium 232 et le potassium 40 entretient encore en énergie thermique le noyau terrestre, mais surtoutn 3 le manteau rocheux terrestre, et donc toute la géothermie.
Il est plus abondant dans la nature que l'or ou l'argent17. Il est également présent dans toute l'écorce terrestre, surtout dans les terrains granitiques et sédimentaires, à des teneurs d'environ 2,7 g/t18 (soit 2,7 ppm). Ainsi, le sous-sol d'un jardin sur un carré de 20 m de côté peut-il en contenir, sur une profondeur de 10 m, environ 24 kg, ce qui fait de l'ordre du millier de milliards de tonnes rien que pour l'écorce terrestre, sans compter le manteau.
En termes de réserve mondiale, cependant, l'immense majorité de cette masse est inexploitable dans les conditions économiques actuelles. La teneur du minerai varie beaucoup selon les roches, de 0,1 ppm dans les carbonates à 350 ppm dans les phosphates19.
L'eau de mer contient environ 3,3 mg d'uranium par mètre cube selon le CEA et la COGEMA20, soit 4,5 milliards de tonnes d'uranium dissous dans les océans.
Les eaux douces en contiennent souvent aussi en diverses concentrations. La concentration moyenne du Rhône en uranium est de 0,5 μg/l (soit un demi-milligramme par mètre cube). La masse d’uranium transitant chaque jour dans le Rhône peut ainsi être estimée à environ 80 kg21, soit près de trente tonnes par an, provenant essentiellement du ruissellement des roches uranifères des Alpes.
Les ressources dites « identifiées » récupérables à un coût inférieur à 260 dollars/kg U étaient évaluées en 2019 à 8 070 kt, dont 4 724 kt de réserves « raisonnablement assurées » et 3 346 kt de réserves « présumées » (en anglais : inferred). Les ressources récupérables à un coût inférieur à 130 dollars/kg U étaient évaluées à 6 148 ktb 1, dont 27,5 % en Australie, 14,7 % au Kazakhstan, 9,2 % au Canada, 7,9 % en Russie, 7,3 % en Namibie, 5,2 % en Afrique du Sud, 4,5 % au Brésil, 4,5 % au Niger, 4 % en Chine, 2,3 % en Mongolie, 2,2 % en Ouzbékistan, etc (seulement 0,8 % aux États-Unis)b 2. Des ressources additionnelles (« présagées » et « spéculatives ») sont estimées à 5 614 kt, dont 23 % en Mongolie, 12,5 % au Canada, 12 % en Afrique du Sud, 9,6 % en Russie, 9 % au Brésil, 6,7 % en Ukraine et 5,7 % au Vietnamb 3.
| Rang | Pays | Réserves 2007 | % | Réserves 2013 | % | Réserves 2019 | % |
| 1 | 725 | 22,0 | 1 706 | 29 | 1 693 | 28 | |
| 2 | 378 | 11,5 | 679 | 12 | 907 | 15 | |
| 3 | 329 | 10,0 | 494 | 8 | 565 | 9 | |
| 4 | 172 | 5,2 | 506 | 9 | 486 | 8 | |
| 5 | 176 | 5,3 | 383 | 6 | 448 | 7 | |
| 6 | 284 | 8,6 | 338 | 6 | 321 | 5 | |
| 7 | 157 | 4,8 | 276 | 5 | 276,8 | 4,5 | |
| 8 | 243 | 7,4 | 405 | 7 | 276,4 | 4,5 | |
| 9 | nd | nd | 199 | 4 | 249 | 4 | |
| 10 | nd | nd | nd | nd | 143 | 2 | |
| ... | |||||||
| 16 | 334 | 10,3 | 207,4 | 4 | 47,9 | 1 | |
| Total monde | 3 300 | 100 | 5 903 | 100 | 6 148 | 100 |
| Pays | 2004 | 2014 | Variation 2014/2004 (%) |
% 2014 | 2019 | Variation 2019/2014 (%) |
% 2019 | 2020 | |
| 1 | 3 719 | 23 127 | +522 | 41,1 | 22 808 | -1,4 | 41,7 | 19 477 | |
| 2 | 11 597 | 9 134 | −21 | 16,2 | 6 938 | -24 | 12,7 | 3 885 | |
| 3 | 8 982 | 5 001 | −44 | 8,9 | 6 613 | +32 | 12,1 | 6 203 | |
| 4 | 3 038 | 3 255 | +7 | 5,8 | 5 476 | +68 | 10,0 | 5 413 | |
| 5 | 2 016 | 2 400 | +19 | 4,3 | 3 500 | +46 | 6,4 | 3 500 | |
| 6 | 3 282 | 4 057 | +24 | 7,2 | 2 983 | -26 | 5,4 | 2 991 | |
| 7 | 3 200 | 2 990 | −7 | 5,3 | 2 911 | -3 | 5,3 | 2 846 | |
| 8 | 750 | 1 500 | +100 | 2,7 | 1 885 | +26 | 3,4 | 1 885 | |
| 9 | 800 | 926 | +16 | 1,7 | 800 | -14 | 1,5 | 400 | |
| 10 | nd | 573 | 1,0 | 346 | -40 | 0,6 | 250 | ||
| 11 | nd | 385 | 1,0 | 308 | -20 | 0,6 | 400 | ||
| 12 | nd | 573 | 1,0 | 71 | -88 | 0,1 | 71 | ||
| 13 | 878 | 1 919 | +119 | 3,4 | 58 | -97 | 0,1 | 6 | |
| Total mondial | 40 178 | 56 041 | +40 | 100 | 54 742 | -2,3 | 100 | 47 731 |
En 2017, la production mondiale est proche de 60 000 tonnes auxquels s'ajoutent 17 000 tonnes de ressources de « deuxième main » (combustible retraité MOX, militaire...), alors que la consommation d'uranium stagne autour de 65 000 tonnes/an ; le cours du minerai a été divisé par deux en 2016 et les principaux producteurs réduisent fortement leur production24.
La production industrielle a commencé après 1945 pour atteindre 10 000 t/an dès 1953, 50 000 t en 1958, décroit jusqu'à 30 000 t en 1965, remonte jusqu’à un plateau de 65 000 en 1980, redescend jusqu’à 30 000 t dans les années 1990 et remonte dans les années 2000.
La production mondiale 2012 était estimée par l'AIEA à 58 816 tonnes d'uranium, dont 36 % extraites du Kazakhstan, 15 % du Canada, 12 % de l'Australie, 8,2 % du Niger, 7,9 % de Namibie, 5 % de Russie, 4 % d'Ouzbékistan et 3 % des États-Unis25. Des estimations plus récentes de l'Association nucléaire mondiale évaluent la production 2015 à 60 514 tonnes U, dont 39 % du Kazakhstan, 22 % du Canada, 9 % de l'Australie, 7 % du Niger, 5 % de Russie, 5 % de Namibie, 4 % d'Ouzbékistan, 3 % de Chine et 2 % des États-Unis26.
Le Kazakhstan a connu une forte hausse de production dans les années 2000, passant de 3 300 t en 2001 à 17 803 t en 2003. Cette hausse s'est poursuivie en faisant du pays le leader du marché avec 33 % de la production mondiale (soit 17 803 tonnes en 2010)27 et d'importantes réserves minières (17 % de la réserve mondiale). Selon l'OCDE, l'intensification de la production de ce pays a permis une augmentation de plus de 25 % de la production mondiale de 2008 à 201028.
L'uranium est une ressource non renouvelable (comme tous les métaux). Les réserves facilement accessibles sont en léger recul, mais il reste des réserves plus coûteusement accessibles pour 135 ans selon l'OCDE et l'AIEAb 4. La quantité d'énergie extractible à partir de l'uranium naturel pourrait théoriquement être multipliée jusqu'à près de cent fois29 grâce à la surgénération et au retraitement, qui permettraient de fissionner l'uranium 238, beaucoup plus répandu que l'uranium 235.
Dans l'eau de mer et les eaux naturelles
Les concentrations en uranium (l'élément chimique uranium) dans les eaux « naturelles » sont les suivantes30 :
- l'eau de mer : 3,3 µg/L ;
- le Rhône : 0,56 µg/L (débit annuel d’uranium = 29 t) ;
- l'Indus : 4,94 µg/L ;
- le Gange : 7 µg/L ;
- le fleuve Jaune : 7,5 µg/L.
Dans les eaux de boisson :
- eau de Badoit : 58 µg/L à la source, 5,45 µg/L après traitement31 ;
- eau de Vichy : 20 µg/L32.
Le seuil OMS pour les eaux de boisson était fixé jusqu'en 2011 à 15 µg/L33, puis en 2011 la quatrième édition des « Directives pour la qualité de l'eau de boisson » l'a fixé à 30 µg/L34.
Cinétique hydrogéologique
La solubilité de l’uranium est liée aux conditions d’oxydoréduction du milieu. Dans des conditions oxydantes (augmentation de la concentration en oxygène dissous), l’uranium devient plus facilement soluble (passage de la valence IV à la valence VI). Les conditions oxydantes favorisent la complexation de l’uranium en solution avec certains ligands19. Les principaux ligands sont, par ordre d’affinité décroissante :
- les carbonates ;
- les groupes hydroxyle ;
- les nitrates35 ;
- les phosphates.
L’uranium présente une très forte affinité pour les oxyhydroxydes de fer19. Cette adsorption peut s’effectuer très rapidement lors de changements des conditions d’oxydoréduction, une diminution de la teneur en oxygène (condition réductrice) engendre une précipitation rapide de l’uranium sous forme d’oxyde (UO2)19. C'est une telle précipitation qui est par exemple à l'origine du gisement d'Oklo.
Synthèse chimique des fluorures d'uranium (UFx)
Deux étapes sont nécessaires à la synthèse :
- le raffinage :
- Le minerai d'uranium pulvérisé « yellowcake » — est dissous dans l'acide nitrique, fournissant une solution de nitrate d'uranyle UO2(NO3)2,
- Éventuellement filtration,
- Le nitrate d'uranyle pur est obtenu par extraction par solvant, avec une solution de TBP,
- cette étape permet d'obtenir un nitrate d'uranyle UO2(NO3)2 de grande pureté (>99,95 %) ;
- la conversion en elle-même :
- Précipitation du nitrate d'uranyle par l'ammoniac gazeux pour obtenir du diuranate d'ammonium (NH4)2U2O7 (DUA),
- Calcination du diuranate d'ammonium, vers 400 °C, pour produire l'UO3,
- Réduction de l'UO3 par l'hydrogène pour obtenir de l'UO2,
- Hydrofluoration d'UO2 par l'acide fluorhydrique HF dans un four pour produire du tétrafluorure d'uranium UF4,
- Réduction de l'UF4 avec du calcium finalement pour obtenir du métal pur.
-
Yellowcake + nitrate d'uranyle.
Propriétés
Propriétés radiologiques
Produit fissile naturel
L'uranium 235 est le seul nucléide naturel qui soit fissile (ou, très rarement, fissible), autrement dit il peut, par capture de neutron, se scinder en deux noyaux fils avec émission de neutrons (fission nucléaire). Par suite, l'uranium enrichi en cet isotope est aujourd'hui utilisé comme combustible nucléaire dans les réacteurs nucléaires (voir Cycle du combustible nucléaire) ou encore dans les armes nucléaires, que ce soient les bombes atomiques, ou comme amorce dans les bombes H.
Au contraire de l'uranium 235, l'uranium 238, lorsqu'il capture un neutron, ne fissionne pas (sauf neutrons rapides). Il devient de l'uranium 239 instable qui, par désintégration β−, va se transformer en neptunium 239. Or ce dernier est lui aussi radioactif β−, et va alors donner naissance à un nouveau noyau, le plutonium 239. Ce radioisotope est fissile, comme l'uranium 235. L'uranium 238 est un isotope fertile, qui peut produire des produits fissiles.
L'uranium 234 n'est, lui, ni fissile, ni fertile, et provient de la décomposition radioactive de l'uranium 238 comme indiqué dans la précédente section.
La fission d'un atome d'uranium 235 libère de l'ordre de 193,2 MeVn 4 d'énergie récupérable en réacteur (la valeur exacte dépendant des produits de fission) et 9,6 MeV communiquée aux neutrinos inutiles et quasiment indétectables. De même, la fission d'un atome de plutonium 239 libère de l'ordre de 198,6 MeVn 4 d'énergie récupérable et 8,6 MeV communiquée aux neutrinos. Ces valeurs sont à comparer avec celles de la combustion de carburants fossiles, qui libèrent de l'ordre de 5 eV par molécule de CO2 produit36 : l'ordre de grandeur des énergies libérées par les combustibles nucléaires est un million de fois plus importante que celle des énergies fossiles chimiques.
Le potentiel d'énergie de l'uranium n'est exploité que très partiellement dans les réacteurs actuels, mais la différence reste nette : 1 kg d'uranium naturel permet la production d'environ 500 000 MJn 5 dans un réacteur conventionnel, à comparer avec les 49 MJ obtenus par 1 kg de gaz naturel, 45 MJ pour 1 kg de pétrole, et 20 à 30 MJ pour le charbon37.
Isotopes de l'uranium naturel
L'uranium possède 26 isotopes connus, tous radioactifs, dont trois seulement sont présents à l'état naturel : 238U, 235U et 234U. On trouve dans une tonne d'uranium naturel pur 7,2 kg d'uranium 235 et 56 g d'uranium 234, le reste étant de l'uranium 238.
- Uranium 238 et uranium 235
Les isotopes 238U et 235U ont beaucoup d'applications, militaires notamment, mais aussi civiles, comme la datation de l'âge de la Terre à partir de la datation radiométrique par l'uranium-plomb ou par l'uranium-thorium.
Quelles que soient les teneurs en uranium des milieux, les proportions entre les deux principaux isotopes formant l'uranium naturel sont pratiquement les mêmes : 238U : 99,28 %, 235U : 0,72 %, 234U : 0,0056 %.
La proportion d'235U décroît à l'échelle des temps géologiques. Leur rapport de formation dans une supernova est de 1 à 1,6538, c'était (approximativement) la proportion de l'uranium présent sur Terre il y a ~4,5 milliards d'années, ce qui est juste inférieur à l'âge de la formation de ces isotopes (voir Formation et évolution du système solaire).
Il y a deux milliards d'années, lors de la période de fonctionnement du réacteur nucléaire naturel d'Oklo, la proportion d'235U était encore de près de 4 %, ce qui a permis à ce gisement d'atteindre la criticité, lors de la précipitation des composés dissous formant le nouveau minerai.
- Uranium 234
Le troisième isotope, 234U, appartient à la chaîne de désintégration de l'238U.
L'isotope 234 est toujours présent sur Terre, à l'état de traces, bien qu'il ait une demi-vie de seulement 245 500 ans ; car il est constamment créé par désintégration radioactive de l'isotope 238 (après trois étapes : une transition α donnant 234Th, puis deux transitions β− donnant 234Pa, puis 234U). Quand il est à l'équilibre séculaire, la proportion entre 238U et 234U est égale au rapport des demi-vies, soit 0,0056 %.
Cependant, les rapports isotopiques peuvent varier légèrement d'un gisement à l'autre, entre 0,005 % et 0,006 % pour l'234U39, du fait d'une légère différence de comportement dans le changement U6+↔ U4+40. Le rapport isotopique 234U/238U peut être perturbé par différents processus environnementaux, tandis que le rapport 235U/238U reste assez largement constant17.
- Autres isotopes
L'industrie nucléaire produit deux autres isotopes artificiels de l'uranium, relativement stables à échelle humaine :
- l'isotope 236 est produit en réacteur par irradiation de l'isotope 235, qui dans près de 18 % des cas ne fissionne pas mais absorbe un neutron. Il tend à s'accumuler dans l'uranium de recyclage, dont il augmente fortement la radioactivité, et dont (étant neutrophage) il diminue le potentiel énergétique. Bien qu'ayant une demi-vie de 23 millions d'années, presque du centuple de celle de l'isotope 234, cet isotope a disparu depuis longtemps dans la nature. Son produit est du thorium 232, qui s'est « confondu » avec le thorium 232 « initial » et se trouve à présent majoritairement sous cette forme ainsi que des éléments de sa chaîne de désintégration ;
- l'isotope 233 est un élément fissile produit en réacteur par irradiation du thorium. Il est à la base du cycle du thorium. Sa demi-vie de 159 000 ans est largement supérieure à celle du plutonium.
Activité massique
L'uranium pur est radioactif, son activité massique dépendant à la fois de son enrichissement, et de la fraîcheur de sa purification chimique.
Si l'on considère les isotopes purs de l'uranium, 238U a une activité massique de 12,4 Bq/mg, 235U de 80 Bq/mg, et 234U de 230 Bq/µg, soit 230 000 Bq/mg — quatre ordres de grandeur au-dessus des précédents.
- L'uranium naturel, quand il est chimiquement purifié (essentiellement composé de 235U et de 238U en équilibre avec son descendant 234U), a une activité spécifique de l'ordre de 25 Bq/mg. En amont, à poids égal d'uranium, la radioactivité d'un minerai, où il est en équilibre avec tous les éléments radioactifs de sa chaîne de désintégration, est naturellement 3 (si le radon peut s'échapper) à 7 fois plus importante.
- L'uranium enrichi est plus actif, partiellement du fait de l'activité plus importante de 235U (6,33 fois plus radioactif que l'238U), mais surtout à cause de la concentration différentielle en 234U (10 000 fois plus radioactif que 238U), toujours présent à l'état de traces dans la chaîne de désintégration de l'isotope 238. Elle atteint typiquement 2 500 Bq/mg pour un enrichissement de 90 % (uranium dit de qualité militaire). Pour les enrichissements de l'ordre de 3 %, destinés aux centrales nucléaires, l'activité spécifique est de l'ordre de 60 Bq/mg.
- Inversement, l'uranium appauvri est presque entièrement débarrassé non seulement de sa fraction de l'isotope 235, mais également de son descendant l'isotope 234. Immédiatement après l'enrichissement, son activité massique tend à se rapprocher de celle de 238U pur, c'est-à-dire de l'ordre de 12,5 Bq/mg (en pratique, un peu plus du fait de la présence résiduelle d'235U). Cependant, l'équilibre entre 238U et ses deux premiers descendants (le thorium 234 de période 24 jours, et le protactinium 234) est atteint rapidement, en 2 mois. La radioactivité spécifique à l'équilibre (avec ses deux premiers descendants) étant déjà de 41,5 Bq/mg41.
Sections efficaces
Aux neutrons thermiques, avec :
σa= section efficace d'absorption (= capture + fission le cas échéant)
σf= section efficace de fission
À 20 °C :
233U : σa = 585,9 barns ; σf = 532,8 barns
235U : σa = 676,1 barns ; σf = 568,4 barns
238U : σa = 2,72 barns
À 240 °C :
233U : σa = 587,3 barns ; σf = 534,9 barns
235U : σa = 647,0 barns ; σf = 543,1 barns
238U : σa = 2,60 barns
À 300 °C :
233U : σa = 588,9 barns ; σf = 536,1barns
235U : σa = 642,4 barns ; σf = 538,8 barns
238U : σa = 2,58 barns
Propriétés chimiques
De symbole U, l'uranium est le dernier élément naturel du tableau périodique. Chaque atome d'uranium possède 92 protons et entre 125 et 150 neutrons.
À l'état pur, l'uranium solide est un métal radioactif gris à blanc (voire argenté), qui rappelle la couleur du nickel. Il est dur et très dense. De plus, l'uranium est l'atome le plus lourd (qui contient le plus de nucléons) présent naturellement sur la Terre.
En raison de son affinité pour l'oxygène, l'uranium s'enflamme spontanément dans l'air à température élevée, voire à température ambiante lorsqu'il se trouve sous forme de microparticules. Il est pyrophorique.
L’uranium a quatre valences possibles (+III à +VI), les valences IV et VI étant les plus répandues dans les minerais. Les conditions de passage de la valence IV à la valence VI dépendent du potentiel d'oxydoréduction du milieu19.
Ainsi dans la nature, l'élément uranium se retrouve toujours combiné à d’autres éléments, tels l'oxygène, l'azote, le soufre, le carbone sous forme d'oxydes, de nitrates, de sulfates ou de carbonates. On le trouve, par exemple, combiné à l'oxygène dans l'uraninite et la pechblende, deux des principaux minerais d'uranium, constitués d'oxyde uraneux (UO2).
Enfin, les ions uranyle UO22+ se dissolvent très bien dans la plupart des acides, comme dans l'acide nitrique HNO3 ou l'acide fluorhydrique HF en donnant des sels d'uranyle tels que le nitrate d'uranyle UO2(NO3)2. L'équation de la dissolution de l'ion uranyle en sel d'uranyle dans l'acide nitrique est la suivante :
Dérivés organo-uraniens
Comme la plupart des métaux, l'uranium a une chimie organométallique et de nombreux complexes organométalliques, tels l'uranocène, sont connus.
Applications
Utilisations historiques
Le minerai d'uranium a été utilisé comme pigment dans la verrerie, la céramique et la faïence, sous forme de diuranate de sodium ou d'ammonium17. Dans le verre, l'uranium est typiquement utilisé à des concentrations de 0,1 % à 2 % en masse pour produire de l'ouraline, solide d'un jaune fluorescent ou légèrement vert facile à identifier17. Il a été utilisé pour colorer des céramiques dentaires à de très faibles concentrations17. Il produit une pigmentation jaune à faibles concentrations, puis crème, orange, brune, verte, ou noire, quand la concentration augmente17.
Il sert également de catalyseur dans certaines réactions chimiques spécialisées et dans des films photographiques17.
L'uranium appauvri a également été utilisé pour ces emplois physico-chimiques17. Sous forme d'acétate d'uranyle et de zinc (réactif de Blanchetière), il donne des cristaux jaune-vert fluorescents avec les ions sodium Na+. Il permet donc de caractériser facilement ce métal lors des analyses en chimie minérale.
En métallurgie, il a été utilisé comme élément d’alliage dans la fabrication d'aciers rapides. D'appréciables quantités de ferrouranium ont été produites entre 1914 et 191642. À la fin des années 1950, l'apparition d'importants stocks d'uranium appauvri aux États-Unis relance la recherche sur la production et l'utilisation d'alliages d'acier contenant de l'uranium, mais aucun débouché majeur n'est identifié43.
Industrie nucléaire
Historiquement, la première utilisation du minerai d'uranium par l'industrie nucléaire a été d'en extraire le radium, pour des applications médicales.
Le principal usage contemporain de l'uranium exploite ses propriétés nucléaires.
- L'uranium 235 est le seul isotope fissile naturel, ce qui permet l'exploitation de l'uranium dans les réacteurs nucléaires (après un éventuel enrichissement), ainsi que pour la fabrication d'armes nucléaires (après un fort enrichissement).
- L'uranium 238 est à la fois fissible dans les réacteurs à neutrons rapides, et fertile : par capture neutronique, il se transforme finalement en plutonium 239, fissile. Il est envisagé d'exploiter cette double possibilité dans le cycle du combustible nucléaire, pour des cycles fondés sur la combustion du plutonium.
- L'uranium 233, qui peut être artificiellement produit par irradiation du thorium, est également fissile en neutrons thermiques. Cette possibilité est à la base d'un cycle surgénérateur fondé sur le thorium.
Médecine nucléaire
Contrôle des matières nucléaires
L'uranium est une matière nucléaire dont la détention est réglementée (Article R1333-1 du code de la défense).
Uranium appauvri
L'uranium appauvri, un sous-produit de l'enrichissement de l'uranium, est remarquable par sa dureté et sa densité.
Usage militaire
L'uranium appauvri n'est pas employé pour son aspect radioactif mais pour ses propriétés mécaniques. Il est pyrophorique, employé comme arme antichar dotée d'un fort pouvoir à la fois pénétrant et incendiaire : à très haute vitesse, il perfore aisément les blindages en s'enflammant lors de l'impact, provoquant un incendie qui fait exploser le véhicule touché. Ainsi, des munitions à base d'uranium appauvri (obus de 20 à 30 mm des avions ou hélicoptères chasseurs de chars) ont été utilisées lors des guerres du Golfe (guerre du Koweït et guerre en Irak) et du Kosovo. L'uranium appauvri est également utilisé pour faire des plaques de blindages17.
Concernant sa toxicité, l'Organisation Mondiale de la Santé précise que "Dans les zones de conflit où l’uranium appauvri a été utilisé, il n’est pas nécessaire de soumettre les populations à un dépistage ou à un contrôle généralisé des effets éventuels sur leur santé. Les personnes qui pensent avoir été exposées à des doses excessives doivent aller consulter leur médecin qui les examinera, les traitera si elles ont des symptômes et assurera le suivi"44. Concernant les militaires, les études de suivi des vétérans blessés par des fragments d'uranium appauvri, encore inclus dans leur organisme, révèlent des "concentrations décelables d’uranium appauvri dans leurs urines, mais sans effet indésirable apparent pour la santé"44. Plus de 95% de l'uranium pénétrant dans l'organisme n'est pas absorbé et est éliminé via les selles et les urines (en 24 heures pour l'uranium sanguin)44.
Usage civil
L'uranium appauvri constitue un combustible nucléaire appelé « combustible MOX » lorsqu'il est complété par du plutonium. Il sert d'élément fertile dans les réacteurs, où l'238U se transforme par irradiation en 239Pu fissile. Le MOX contribue ainsi au recyclage du plutonium.
L'uranium appauvri a autrefois été utilisé comme contrepoids en aviation, sur les premiers Boeing 747, les McDonnell Douglas DC-10, les Lockheed L-1011 TriStar par exemple17, ce qui pose le problème du recyclage de ces avions qui, pour beaucoup, arrivent en fin de vie. Dans cet emploi, il est progressivement remplacé par le tungstène17. La quille de certains voiliers de compétition a contenu de l'uranium appauvri avant que la réglementation n'interdise son usage. Il enfin utilisé pour les écrans de protection radiologique où il est également plus efficace que le plomb17.
Concernant sa toxicité, « l’exposition excessive des professionnels à l’uranium appauvri par ingestion est improbable là où des mesures de sécurité ont été prises pour le lieu de travail »44. « Les études à long terme portant sur des professionnels exposés à l’uranium ont signalé certains troubles de la fonction rénale selon l’intensité de l’exposition. Il semblerait néanmoins d’après certaines données que ces troubles puissent être transitoires et que la fonction rénale revienne à la normale après élimination de la source d’une exposition excessive »44.
Imprégnation des populations humaines
Elle est a priori plus élevée dans les régions de mines d'uranium et chez les travailleurs de l’industrie nucléaire (en particulier impliqués dans l'extraction, le raffinage, la production de combustible nucléaire et son retraitement). Certains militaires (exposés aux vapeurs ou particules de munitions à uranium appauvri ont aussi été potentiellement exposés, sachant que par exemple 20 261 militaires français ont participé aux opérations extérieures dans le Golfe Persique en 1990-1991), potentiellement susceptibles d'avoir développé un « syndrome de la guerre du Golfe »45 ; dans les années 1990-2000, les auteurs n’ont souvent pas particulièrement retenu le rôle de l’uranium appauvri dans ce syndrome 46,47,45
Ces personnes sont plus exposés au risque d'incorporation d'uranium, principalement par inhalation, ingestion, ou à la suite d'une blessure48. On cherche rétrospectivement à reconstituer49 leur niveau d'exposition à l'uranium pur, et/ou aux composés suivants : NU (Nitrate d'uranyle) ; UF6 (Hexafluorure d’uranium) ; UF4 (Tétrafluorure d'uranium) ; U – TBP (tributylphosphate d'uranium) ; DAU (Diuranate d'ammonium) ; UO2F2 (Fluorure d'uranyle) ; UO2 (Dioxyde d'uranium) ; UO3 (Trioxyde d'uranium) ; UO4 (Tétraoxyde d'uranium) ; UF6 (Hexafluorure d'uranium) ; Effluents uranifères acides ; U3O8 (Sesquioxyde d'uranium) ; UO2F2 (Fluorure d'uranyle...)50.
Au milieu des années 2000-2010, si les effets de l’irradiation externe sont déjà bien explorés via l'épidémiologiques à grande échelle51, les effets (en termes de risque de cancer notamment)52,53 de l'exposition interne induite par l’incorporation des particules d'uranium (et d'autres éléments émetteurs alpha) sont encore mal évalués54. En France AREVA a développé en son sein le projet Alpha risk project dans cet esprit55. Le tabagisme et l'ingestion de boissons alcoolisées sont aussi des sources d'intégration d'uranium52.
En 2018 en France le « Volet périnatal » du programme national de biosurveillance a publié une évaluation de l'imprégnation des femmes enceintes dont pour l'uranium (et douze autres métaux ou métalloïdes ainsi que quelques polluants organiques). Le dosage de l'uranium a été fait dans les urines de 990 femmes enceintes au moment de leur arrivée à la maternité. Elles faisaient toutes partie de la « Cohorte Elfe », un pannel ne comprenant que des femmes ayant accouché en France en 2011 hors Corse et TOM56. Seules 28 % de ces 990 femmes présentaient une quantité détectable d'uranium dans leurs urines (95e centile de la distribution : 20,8 μg/L, pour 29,5 μg/g de créatinine)56. Ces quantités évoquent les mêmes ordres de grandeur que d'autres études faites en France et à l’étranger chez les femmes adultes (à cause du faible taux de quantification de cet élément, l'étude de 2018 n'a pas recherché les déterminants d’imprégnation56).
Toxicité
Toxicité chimique
Elle est du même ordre que celle du plomb (autre métal lourd). La dose létale pour l'homme semble être de quelques grammes57.
Chez un humain adulte et en bonne santé, le système digestif absorbe globalement entre 0,2 et 2 % de l’uranium présent dans l'eau et les aliments.
Les composés solubles de ce métal sont plus facilement absorbés que les composés insolubles58. Plus de 95 % de l'uranium ingéré ne sont pas absorbés par la muqueuse intestinale, éliminés dans les fèces. Puis environ 67 % de l'uranium passé dans le sang sera filtré par les reins et excrété dans les urines (dans les 24 heures)58. Les deux tiers de l'uranium restant seront intégré par l'organisme ; par accumulation dans les os et pour 16 % dans le foie, pour 8 % dans les reins et 10 % dans les autres tissus58.
Selon l'OMS, le contenu attendu en uranium d'un corps humain en équilibre avec son environnement est d'environ 90 à 150 μg d'uranium59. Il résulte d'un apport journalier de l'ordre de 1 à 2 µg/jour par l'eau courante et l'alimentation.
Le rein est l'organe critique en termes de toxicité chimique. Le suivi de cohortes de professionnels exposés à l'uranium a mis en évidence des troubles rénaux (néphrites), avec une gravité dépendant de la dose60.
À forte dose, l'uranium induit une néphropathie sévère, due à la dégradation des tubules proximaux, et à l'atteinte des structures glomérulaires61,62,63. L'observation histologique et morphologique montre que l'architecture de l'épithélium des structures glomérulaires est altérée62. Puis l'épithélium tubulaire proximale se nécrose61. Certaines données58,61 ont un temps fait croire que ces troubles n'avaient qu'un caractère transitoire, car une expérience sur l'animal a montré un retour à une situation rénale apparemment normale après élimination de la source d’une exposition excessive. L'épithélium lésé peut effectivement se régénérer après la disparition des apports en uranium, y compris après plusieurs injections de fluorure d'uranyle UO2F2 (à 0,66 ou 1,32 mg U/kg de poids corporel (chez l'animal)61 ; cependant l'observation histologique a montré (chez le rat) que les cellules mortes ou lésées sont remplacées par des cellules structurellement anormales, et dépourvues de certaines capacités fonctionnelles64.
Le seuil de toxicité chimique rénale est estimé à 70 µg/kg de poids corporel ou 16 µg/g de rein (limite de 3 µg/g de rein pour la protection des travailleurs)65. La dose létale 50 (DL50) par voie orale est de 204 mg/kg chez le rat de laboratoire (la souris s'y montre un peu plus résistante avec de 242 mg/kg comme dose létale (DL50) par voie orale. En 1959, la Commission Internationale de Protection Radiologique (CIPR) recommandait de ne pas dépasser 3 μg/g dans le rein, mais cette valeur-seuil est aujourd'hui controversée, car des doses bien inférieures suffisent à induire des dégâts dans les tubules proximaux (avec protéinurie et enzymurie, par exemple pour 0,7 à 1,4 μg d'uranium par gramme de rein61.
Dans tous les cas, c'est la toxicité chimique rénale (néphrite tubulaire aiguë) qui entraîne la mort de l'animal66. Le mécanisme toxique est expliqué comme suit : l'uranium non-excrété par le rein y est réabsorbé et s'y accumule, en se fixant sur les cellules tubulaires proximales67 où en raison de l'acidité du milieu, le complexe uranium-uranyle se dissocie pour éventuellement se combiner avec certains composants de la membrane luminale. Les ions uranyle peuvent alors pénétrer la cellule. Ils s’accumulent notamment dans les lysosomes. Ils y forment des aiguilles de phosphate d’uranyle, ainsi que dans les mitochondries67. On a aussi montré in vitro que l'uranium à haute dose peut induire l'apoptose (suicide cellulaire) en activant certains enzymes (caspases 3 et 9, protéases à cystéine) via des signaux intrinsèques des mitochondries68. Les symptômes de la néphropatie sont accompagnés d'anomalies fonctionnelles (polyurie, enzymurie, protéinurie, élévation sanguine de la créatinine et de l'urée66,61,69,70. Les lésions sont moindres et plus réversibles si le taux rénal d'uranium est bas et le temps d’exposition court.
Perturbation endocrinienne : des expériences récentes (sur modèle animal) ont montré qu'une exposition chronique à de faibles doses d'uranium appauvri (ce n'est donc pas la radiotoxicité qui est ici en cause) se traduit par une diminution du taux de 1,24,25(OH)3D3 (ou 1,25-trihydroxyvitamine D3, une forme hormonalement active de la vitamine D)60.
Cette diminution est accompagnée de modifications moléculaires des enzymes de types cytochromes P450 (CYPs), enzymes protéiques importantes pour le métabolisme, présente chez presque toutes les espèces animales, végétales, fongiques, et qui jouent un rôle important pour la détoxication de l'organisme. On observe aussi des modifications des récepteurs nucléaires associés60. La même étude que ci-dessus a montré que l'uranimum appauvri et – de la même manière – l'uranium enrichi affectent l'expression de VDR (vitamin D receptor) et de RXR α (retinoic X receptor alpha), ce qui signifie que l'uranimum (enrichi ou non) peut perturber l'expression des gènes cibles de la vitamine D (impliqués dans le transport du calcium au niveau rénal)60.
Radiotoxicité
Contrairement à la radioactivité, qui se mesure en becquerels, la radiotoxicité de l'uranium (c'est-à-dire l'effet de son rayonnement ionisant sur l'homme) se mesure en microsieverts (μSv).
Quel que soit son enrichissement, la radioactivité de l'uranium est toujours du type alpha, de l'ordre de 4,5 MeV. Sa radiotoxicité dépend donc de son activité massique et faiblement de sa composition. Elle est de l'ordre de 0,6 µSv/Bq (F) à 7 µSv/Bq (S) en inhalation, 0,05 µSv/Bq (F) à 0,008 µSv/Bq (S) en ingestion, les poumons et les os étant alors les organes critiques71.
La radiotoxicité de l'uranium serait du même ordre de grandeur que celle de la toxicité chimique : elle l'emporte pour des enrichissements supérieurs à 6 %, la toxicité chimique étant sinon prépondérante41.
Effets sur la reproduction
L'uranium est aussi reprotoxique via notamment un effet délétère sur les organes reproducteurs ; soit du fait de sa radioactivité, soit du fait de sa chimiotoxicité, et peut-être des deux.
L'uranium a chez l'animal des effets démontrés ; sur le système reproducteur : chez le rongeur de laboratoire, la barrière hémato-testiculaire (ou BHT) qui était réputée protéger le testicule peut en être franchie par le plutonium, l'américium et le polonium au moins grâce à la transferrine.
- De l'uranium est significativement trouvé dans les testicules de rats ayant reçu un implant d'uranium dans le muscle d'une des pattes. Les récepteurs à la transferrine présent dans l'épithélium séminifère humain pourrait donc expliquer la présence d'uranium dans le sperme de soldats blessés par des munitions à l'uranium appauvri.
- Des rats ayant des implants sous-cutanés d'uranium, et des souris abreuvées d'eau contenant de l'uranium produisent des cellules de Leydig altérées, ce qui perturbe la production d'hormones stéroïdes et se traduit par un sperme dégradé (spermatozoïdes moins nombreux et moins mobiles), expliquant les observations faites dès 1949 de diminution du nombre de portées et du nombre de petits par portée chez plusieurs espèces d'animaux ayant régulièrement ingéré de faibles doses de nitrate d'uranyle72,73.
Effets sur le développement
- Il induit une toxicité fœtale et embryonnaire chez la souris chez laquelle un implant d'uranium a été posé dans le muscle d'une patte.
- Il est tératogène à doses plus élevées, avec mort de l'embryon exposé à une concentration 50 mg·kg-1·j-1 durant 9 jours, 20 % inférieure à la dose létale pour l'adulte.
- Une souris gestante abreuvée avec une eau correspondant à une ingestion de 25 mg d'uranium/kg et par jour produit moins de jeunes. Ceux-ci ont ensuite des problèmes de développement et de survie74.
La plupart des études et réglementations se fondent sur les effets sur l'animal, or les premières études ex vivo permises par les nouvelles techniques de cultures cellulaires laissent penser que les gonades humaines seraient plus sensibles à l'uranium que ne le sont celles des rongeurs utilisés en laboratoire. Le testicule fœtal humain pourrait aussi être plus sensible que ceux des rongeurs de laboratoire75.
Normes
Il n'y a pas de consensus sur les normes ni la NOAEL (dose sans effet nocif observé) de l'uranium, certains estimant que les effets délétères de la radioactivité peuvent exister quelle que soit la dose.
Pour la potabilité de l'eau, l'OMS a fixé une teneur maximale de 1,4 mg·l-176, tout en recommandant dans ses lignes directrices une concentration en uranium cent fois plus faible, inférieure à 0,015 mg/l, pour les eaux de boisson courante77. Au Canada, l'eau potable possède une concentration maximale acceptable de 0,02 milligramme d'uranium par litre (mg/L)78.
Prix
Le prix de l'uranium a baissé dans les années 1980 et 1990 pour plusieurs raisons :
- les politiques d'économie d'énergie ont permis de limiter la consommation d'électricité ;
- des gisements d'uranium économiquement exploitable ont été découverts ;
- les stocks d'uranium militaire constitués dans le contexte de la guerre froide ont été convertis en stocks civils et utilisés dans les réacteurs nucléaires à la suite de l'assouplissement des tensions américano-soviétiques.
Le prix de l'uranium a atteint un minimum en à 14,1 dollars par kilogramme de U3O880.
Le prix de l'uranium a progressivement augmenté depuis 2001 pour atteindre un pic à 298 $/kg en . Ce pic s'explique par la diminution des stocks, la faible augmentation de production, et par des événements ponctuels tels que l'inondation de la mine de Cigar Lake au Canada et l'incendie de la mine Olympic Dam en Australie81.
L'uranium est redescendu à 102,5 $/kg en . En , il se situait à environ 138,9 $/kg. Il est à prévoir une tendance à la hausse en raison de l'épuisement des stocks militaires prévu vers 201582.
En le cours de l'uranium est au plus bas : aux alentours de 52,9 $/kg de U3O8. Ceci s'explique par le faible coût de production des mines du Kazakhstan et par l'offre qui surpasse la demande83.
Le prix de revient du kWh est peu sensible au prix de l’uranium. Certes, le coût du cycle du combustible représente environ 20 % du prix de revient du kWh, mais ce cycle comprend toutes les transformations physiques et chimiques qu’il faut faire subir à l’uranium naturel pour en faire un combustible utilisable. Le coût du combustible nucléaire constitue environ 5 % du prix final du kWh nucléaire en 201484. Cependant, des études économiques montrent que le prix de l'uranium commence à avoir un effet significatif sur le coût du kWh d'électricité nucléaire à partir de 110 ou 220 euros par kilogramme de U3O885.
Commerce
La France importe plus que la consommation d'uranium qui lui est nécessaire et exporte ses surplus sous différentes formes, d'après les douanes françaises. En 2014, le prix moyen à la tonne à l'export était de 36 000 €86.
Notes et références
Notes
- « Au sujet de l'uranite, un nouveau métalloïde ».
- Avant la découverte de la radioactivité, Lord Kelvin avait estimé l'âge de la Terre à quelque 20 millions d'années, en supposant que la seule source d'énergie capable de s'opposer au refroidissement était la chaleur résiduelle, initialement produite lors de la formation de la Terre. Un âge de seulement quelques dizaines de millions d'années fut considéré beaucoup trop court par les géologues, et un vif débat s'ensuivit entre géologues et physiciens. Celui-ci ne devait prendre fin qu'une vingtaine d'années après la découverte de la radioactivité, trop tard pour Kelvin de faire amende honorable. Plus tard, les physiciens ont pu apporter aux géologues des méthodes de datation absolue des roches qui se basent sur la radioactivité et les abondances actuelles de certains radioéléments et de leurs produits de désintégration (voir Radiochronologie).
- L'uranium est présent sur Terre essentiellement sous forme d'oxydes, donc incorporé dans les roches et très peu dans le noyau métallique. Mais la chaleur dégagée dans le manteau retarde le refroidissement du noyau.
- Voir Fission nucléaire.
- « Théoriquement » la fission complète d'1 kg d'uranium libère une chaleur de 80 TJ. Mais dans un réacteur nucléaire, seulement environ 1 % (à quelques %) de l'uranium initialement présents subit réellement la fission, avant d'être remplacé.
Références
- (en) Uranium 2020: Resources, Production and Demand [archive], p. 18-19, Agence pour l'énergie nucléaire (NEA-OCDE) et Agence internationale de l'énergie atomique, 23/12/2020.
- p. 15
- p. 18
- p. 32
- p. 14
- Autres références
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-420-09084-0)
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », Dalton Transactions, , p. 2832 - 2838 (DOI 10.1039/b801115j)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC, , 89e éd., p. 10-203
- Entrée « Uranium, powder » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 30 juin 2018 (JavaScript nécessaire)
- « Uranium [archive] » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- (en) Argonne National Laboratory, Uranium Quick Facts [archive]
- (en) J. Korenaga, « Earth's heat budget: Clairvoyant geoneutrinos », Nature Geoscience, vol. 4, no 9, , p. 581–582
- Réserves d'uranium naturel dans le monde [archive], Connaissance des énergies, 17 avril 2014.
- Cigar Lake, nouvel Eldorado de l’uranium canadien [archive], Connaissance des énergies, 18 avril 2014.
- Erwin Erasmus Koch (trad. André Pougetoux), Uranium, Paris, André Bonne Paris, coll. « L'homme et l'univers », , 225 p., p. 15
- Jean Talbot, Les éléments chimiques et les hommes, EDP Sciences, , p. 92
- Michel Dumoulin, Pierre Guillen et Maurice Vaïsse, L'énergie nucléaire en Europe, Lang, , p. 11
- Guide de la technique : l'énergie, Presses polytechniques et universitaires romandes, 1993.
- Courrier international, no 1168 du 21 au 27 mars 2013, p. 46.
- Quelques publications [archive] (avec openlibrary.org [archive])
- Les gisements d'uranium liés spatialement aux discordances [archive] (mémoire), 1983, dans la série Géologie et géochimie de l'Uranium, document présenté à un séminaire du Centre de recherche sur la géologie de l'uranium (Cregu, 26 au 28 octobre 1982), mis en ligne par l'AIEA
- Depleted Uranium: Sources, Exposure and Health Effects - Full Report [archive] WHO, Geneva 2001 (WHO/SDE/PHE/01.1)
- CNDP Commission particulière du débat public Gestion des Déchets Radioactifs : Débat public sur les déchets radioactifs ; Réponses aux questions [archive]
- Étude sur l’origine du marquage par l’uranium dans la nappe alluviale de la plaine du Tricastin [archive], IRSN, septembre 2010
- « Uranium : l'abondance au rendez-vous »(Archive.org • Wikiwix • Archive.is • http://www.cea.fr/var/plain/storage/original/application/07eade098598d926eccc4627b584b173.pdf" rel="nofollow" class="external text">Google • Que faire ?) (consulté le ) Les défis du CEA ; décembre-Janvier 2002 no 94 p. 4-5 par Olivier Donnars.
- Étude sur l’origine du marquage par l’uranium dans la nappe alluviale de la plaine du Tricastin [archive], IRSN, 2010.
- (en) Supply of Uranium - Uranium availability [archive], World Nuclear Association, mis à jour en septembre 2021.
- (en) « Uranium production figures, 20011-2020 » [archive], World Nuclear Association, septembre 2021.
- L’industrie minière s’adapte aux niveaux bas des cours de l’uranium [archive], Les Échos, 10 novembre 2017.
- (en) Uranium 2014: Resources, Production and Demand [archive], p. 62, Agence pour l'énergie nucléaire (OCDE) et Agence internationale de l'énergie atomique, 2014.
- (en) World Uranium Mining Production [archive], Association nucléaire mondiale, 19 mai 2016.
- (en) World Uranium mining [archive], World Nuclear Association
- Communiqué OCDE, Des approvisionnements mondiaux en Uranium assurés à long terme [archive] ; Press Room NEA/COM(2012)5 Paris/Vienne, le 26 juillet 2012
- Superphénix [archive], Connaissance des énergies (consulté le 5 juillet 2016).
- L’uranium de l’eau de mer : véritable ressource énergétique ou mythe ? [archive], Revue des ingénieurs, janvier 2003.
- P. Doremus et J.-P. Pierre (IRSN), Retour d’expérience des interventions de l’IRSN – Présentation de quelques cas (chaufferie, industrie métallurgique, industrie du verre, eaux minérales) [archive] [PDF]
- Eaux minérales gazeuses, trop chargées en uranium ? [archive], Principes de santé, 3 mars 2010.
- (en) Directives pour la qualité de l'eau de boisson [archive], 3e éd.
- (en) Directives pour la qualité de l'eau de boisson [archive], 4e éd.
- Jason Nolan et Karrie A. Weber, « Natural Uranium Contamination in Major U.S. Aquifers Linked to Nitrate » [archive], Environ. Sci. Technol. Lett., 2015, 2, 215−220.
- Données citées par la World Nuclear Association. [archive]
- (en) « The Strategic Importance of Australia’s Uranium Resources »(Archive.org • Wikiwix • Archive.is • http://www.aph.gov.au/house/committee/isr/uranium/subs/sub12.pdf" rel="nofollow" class="external text">Google • Que faire ?) (consulté le ), débat parlementaire australien.
- The Cosmic Origins of Uranium [archive], World nuclear association.
- Uranium isotopes [archive], Globalsecurity.
- Mr Greg Brennecka, « Exploration of the mechanisms that cause uranium isotope fractionation and the implications for nuclear forensics »(Archive.org • Wikiwix • Archive.is • http://www.scitopics.com/Exploration_of_the_mechanisms_that_cause_uranium_isotope_fractionation_and_the_implications_for_nuclear_forensics.html" rel="nofollow" class="external text">Google • Que faire ?), Arizona State University, (consulté le ).
- « l'Uranium, propriété et toxicité. »(Archive.org • Wikiwix • Archive.is • http://www.sfrp.asso.fr/MAN/pdf/Metivier.ppt" rel="nofollow" class="external text">Google • Que faire ?) (consulté le )
- (en) Marshall Cavendish Corporation, How It Works : Science and Technology, Marshall Cavendish, , 2880 p. (ISBN 0-7614-7314-9, lire en ligne [archive]), p. 2548
- [PDF](en) James C. O. Harris, Mineral yearbook, (lire en ligne [archive]), p. 631-632
- Uranium appauvri: sources, exposition et effets sur la santé [archive] - Organisation Mondiale de la Santé
- Salamon R (2004) [Rhttps://hal-lara.archives-ouvertes.fr/hal-01571608/document Rapport de l'enquête française sur la guerre du Golfe et ses conséquences sur la santé ; Répondant à la lettre de mission du 6 juin 2001 adressée par le cabinet du Ministre du Ministère de la Défense] ; [Rapport de recherche INSERM], 286 p., bibliographie p. 276 et 277, tableaux, graphiques. hal-01571608
- Gray GC, Kaiser KS, Hawksworth AW, Hall FW, Barrett-Connor E. Increased postwar symptoms and psychological morbidity among U.S. Navy Gulf War veterans. Am J Trop Med Hyg 1999;60(5):758-66.
- Kang HK, Mahan CM, Lee KY, Magee CA, Murphy FM. Illnesses among United States veterans of the Gulf War: a population-based survey of 30,000 veterans. J Occup Environ Med 2000;42(5):491-501.
- Guseva Canu, I. (2008). Etude épidémiologique des travailleurs exposés au risque d'incorporation d'uranium [archive] (Doctoral dissertation, Paris 6) (résumé [archive]).
- Boice JD, Leggett RW, Dupree Ellis ED, et al. A comprehensive dose reconstruction methodology for former rocketdyne/atomics international radiation workers. Health Phys 2006;90(5):409-30.
- IRSN (2007)Etude épidémiologique des travailleurs exposés au risque d’incorporation d'uranium. Reconstitution de l’exposition à l’uranium et aux produits chimiques associés [archive] ; Journées des thèses IRSN, 1-5 octobre 2007 Irina GUSEVA CANU, 2ème année de thèse
- Cardis E, Vrijheid M, Blettner M, et al. Risk of cancer after low doses of ionising radiation: retrospective cohort study in 15 countries. Br Med J 2005;331(7508):77
- Guseva Canu I, Dupree Ellis E, Tirmarche M. Cancer risk in nuclear workers occupationally exposed to uranium. Emphasis on internal exposure. Health Phys 2007
- Guseva Canu I, Rogel A, Samson E, et al. Cancer mortality risk among biology research workers in France: first results of two retrospective cohort studies. Int Arch Occup Environ Health 2007
- Cardis E, Vrijheid M, Blettner M, et al. The 15-Country Collaborative Study of Cancer Risk Among Radiation Workers in the Nuclear Industry: Estimates of radiation Related Cancer Risk. Radiat Res 2007;167(4):396-416.
- Alpha risk project (AREVA): http://www.alpha-risk.org/ [archive].
- : métaux et métalloïde [archive] des recherches de la cohorte Elfe ; Décembre 2016 ; SANTÉ PUBLIQUE France / Imprégnation des femmes enceintes par les polluants de l’environnement en France en 2011]. Volet périnatal du programme national de biosurveillance|PDF, 224p|aussi disponible à partir de l’URL : www.santepubliquefrance.fr
- Health Physics [archive], résumé : vol. 94(2), février 2008, p. 170-179
- Uranium appauvri : sources, exposition et effets sur la santé [archive], OMS 2001
- « Aide-mémoire OMS »(Archive.org • Wikiwix • Archive.is • http://www.who.int/mediacentre/factsheets/fs257/fr/" rel="nofollow" class="external text">Google • Que faire ?) (consulté le ) sur l'uranium appauvri]
- Tissandie E., Étude des effets des radionucléides (uranium et césium 137) sur le métabolisme de la vitamine D chez le rat [archive] [PDF], thèse de doctorat (sciences de la vie et de la santé), université d'Auvergne, 8 novembre 2007
- Diamond G.L., Morrow P.E., Panner, B.J., Gelein R.M. et Baggs R.B. (1989), Reversible uranyl fluoride nephrotoxicity in the Long Evans, Rat. Fundam. Appl. Toxico. l13, 65- 78
- Kobayashi S., Nagase M., Honda N. et Hishida A. (1984), Glomerular alterations in uranyl acetate-induced acute renal failure in rabbits, Kidney Int. 26, 808-15
- Priest N.D. (2001), Toxicity of depleted uranium, Lancet 357, 244-6
- Wrenn, M.E., Durbin P.W., Howard B., Lipsztein J., Rundo J., Still E.T. et Willis D.L. (1985), Metabolism of in gested U and Ra, Health Phys. 48, 601-33
- Présentation de l'ISPN, « L'uranium, propriétés et toxicité »(Archive.org • Wikiwix • Archive.is • http://www.sfrp.asso.fr/MAN/pdf/Metivier.ppt" rel="nofollow" class="external text">Google • Que faire ?) (consulté le )
- Domingo, J.L., Llobet, J.M., Tomas, J.M. et Corbella J. (1987), Acute toxicity of uranium in rats and mice, Bull. Environ. Contam. Toxico. l39, 168-74
- Leggett R.W. (1989), The behavior and chemical toxicity of U in the kidney: a reassessment, Health Phys. 57, 365-83
- Thiebault C., Carriere M., Milgram, S., Simon A., Avoscan L. et Gouget B. (2007), Uranium Induces Apoptosis and Is Genotoxic to Normal Rat Kidney (NRK- 52E) Proximal Cells, Toxicol. Sci. 98, 479-87
- Blantz, R.C. (1975), The mechanism of acute renal failure after uranyl nitrate, J. Clin. Invest. 55, 621-35
- Haley D.P. (1982), Morphologic changes in uranyl nitrate-induced acute renal failure in saline- and water-drinking rats, Lab. Invest. 46, 196–208
- Publication No 68 de la CIPR, citée par l'IPSN dans sa présentation.
- J.L. Domingo, 2001, Reprod Toxicol. 15, 603-9
- Arfsten D.P. et al., 2001, Toxicology in Health, 17 5610
- S. Barillet, M. Carrière, H. Coffigny, V. Rouiller Fabre, B. Lefèvre, R. Habert, Article [archive] de la Revue Biofutur, p. 35 du Dossier spécial Toxicologie nucléaire.
- S. Barillet, M. Carrière, H. Coffigny, V. Rouiller Fabre, B. Lefèvre, R. Habert, Article [archive] de la Revue Biofutur, in Conclusion p. 37 du Dossier spécial Toxicologie nucléaire.
- LENNTECH, « Comparaison de normes sur l'eau potable »(Archive.org • Wikiwix • Archive.is • http://www.lenntech.com/fran%E7ais/Norme-eau%20potable-OMS-UE.htm" rel="nofollow" class="external text">Google • Que faire ?).
- Tableau des recommandations de l'OMS [archive].
- http://www.hc-sc.gc.ca/ewh-semt/pubs/water-eau/uranium-fra.php [archive]
- NUEXCO Exchange Value (Monthly Uranium Spot) [archive]
- « Impact des cours de l'uranium sur les prix de l'électricité »(Archive.org • Wikiwix • Archive.is • http://energie.sia-conseil.com/20080718-l%E2%80%99impact-de-la-flambee-des-cours-de-l%E2%80%99uranium-sur-les-prix-de-l%E2%80%99electricite/" rel="nofollow" class="external text">Google • Que faire ?)
- « L'impact des cours de l'uranium sur les prix de l'électricité »(Archive.org • Wikiwix • Archive.is • http://energie.sia-conseil.com/20080718-l%E2%80%99impact-de-la-flambee-des-cours-de-l%E2%80%99uranium-sur-les-prix-de-l%E2%80%99electricite/" rel="nofollow" class="external text">Google • Que faire ?)
- « Production et consommation d'uranium dans le monde » [archive], sur www.natura-sciences.com (consulté le )
- « Areva ou la fin du rêve nucléaire - JeuneAfrique.com », JeuneAfrique.com, (lire en ligne [archive], consulté le )
- D’où vient l’uranium naturel importé en France ? [archive], Connaissance des énergies, 12 mai 2014.
- Prix de l'uranium et coût de l'électricité nucléaire [archive]
- Douane française, Statistiques nationales du commerce extérieur [archive]
Voir aussi
Bibliographie
- (en) Tom Zoellner, Uranium : War, Energy, and the Rock that Shaped the World, New York, Penguin, , 354 p. (ISBN 978-0-14-311672-1, OCLC 430052044)
- (en) Richard Rhodes, The Making of the Atomic Bomb : 25th Anniversary Edition, New York, Simon & Schuster Paperbacks, (1re éd. 1986), 838 p. (ISBN 978-1-4516-7761-4, OCLC 764385315, lire en ligne [archive])
Articles connexes
- Contrôle des matières nucléaires
- Énergie nucléaire
- Tableau périodique des éléments
- Table des isotopes
- Extraction de l'uranium
- Cycle du combustible nucléaire
- Réacteur nucléaire naturel d'Oklo
- Datation par l'uranium-thorium
Liens externes
-
Notices dans des dictionnaires ou encyclopédies généralistes
- Ressources relatives à la santé
- :
- (en) Medical Subject Headings
- (no + nn + nb) Store medisinske leksikon
- Note d'information. L'uranium et les risques associés [archive] [PDF], IRSN,
- (en) Uranium resources and nuclear energy [archive] [PDF] (Ressources d'uranium et énergie nucléaire)
- Tableau des données concernant l'uranium [archive]
- « Caractéristiques de l'uranium »(Archive.org • Wikiwix • Archive.is • http://francenuc.org/fr_mat/uranium_f1.htm" rel="nofollow" class="external text">Google • Que faire ?) (consulté le )
- (en) Toxicological Profile for Uranium [archive], ATSDR, U.S. Department of Health and Human Services
- (en) « Technical data for Uranium » [archive] (consulté le ), avec en sous-pages les données connues pour chaque isotope
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
| Métaux Alcalins |
Alcalino- terreux |
Lanthanides | Métaux de transition |
Métaux pauvres |
Métal- loïdes |
Non- métaux |
Halo- gènes |
Gaz nobles |
Éléments non classés |
| Actinides | |||||||||
| Superactinides | |||||||||
Plutonium
| Plutonium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
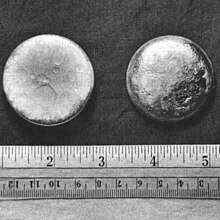 Pastilles de plutonium. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Position dans le tableau périodique | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbole | Pu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom | Plutonium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numéro atomique | 94 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe | – | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Période | 7e période | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bloc | Bloc f | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Famille d'éléments | Actinide | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration électronique | [Rn] 5f6 7s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électrons par niveau d’énergie | 2, 8, 18, 32, 24, 8, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés atomiques de l'élément | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse atomique | 244,06 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique (calc) | 159 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de covalence | 187 ± 1 pm1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État d’oxydation | 6, 5, 4, 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électronégativité (Pauling) | 1,28 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxyde | Amphotère | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergies d’ionisation2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1re : 6,026 0 eV | 2e : 11,2 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopes les plus stables | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques du corps simple | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État ordinaire | solide | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse volumique | 19 816 kg·m-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Système cristallin | Monoclinique | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Couleur | Blanc argenté ternissant à l'air libre | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point de fusion | 640 °C3 640° ± 24,4 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point d’ébullition | 3 228 °C3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de fusion | 2,84 kJ·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de vaporisation | 344 kJ·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molaire | 12,29×10-6 m3·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pression de vapeur | 1 Pa (à 1 483 °C) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitesse du son | 2 260 m·s-1 à 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur massique | 35,5 J·kg-1·K-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité électrique | 685×106 S·m-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité thermique | 6,74 W·m-1·K-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Divers | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No ECHA | 100.028.288 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CE | 231-117-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Précautions | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Radioélément à activité notable |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unités du SI & CNTP, sauf indication contraire. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| modifier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Pour les articles homonymes, voir Plutonium (homonymie).
Le plutonium est l'élément chimique de symbole Pu et de numéro atomique 94. C'est un métal radioactif transuranien de la famille des actinides. Il se présente sous la forme d'un solide cristallisé dont les surfaces fraîches sont gris argenté mais se couvrent en quelques minutes, en présence d'humidité, d'une couche terne de couleur grise, tirant parfois sur le vert olive, constituée d'oxydes et d'hydrures ; l'accroissement de volume qui en résulte peut atteindre 70 % d'un bloc de plutonium pur, et la substance ainsi formée tend à se désagréger en une poudre pyrophorique.
Le plutonium a été produit et isolé pour la première fois le 14 décembre 1940 à l'université de Californie à Berkeley en bombardant de l'uranium 238 par du deutérium. Venant à la suite de l'uranium et du neptunium dans le tableau périodique, ce nouvel élément chimique a été nommé en référence à Pluton, qui vient à la suite des planètes Uranus et Neptune dans le Système solaire. C'est un élément synthétique, produit artificiellement par l'homme, mais on rapporte également l'observation de traces de plutonium naturel dans des minerais d'uranium. Il s'agit d'un métal lourd radiotoxique qui tend à s'accumuler dans les os et, dans une moindre mesure, dans le foie. On observe couramment quatre états d'oxydation du plutonium, de +3 à +6 (l'état +7 est rare), avec des colorations distinctes. La structure électronique du métal pur est déterminée par la bande 5f, qui présente la plus grande densité d'états au niveau de Fermi ; particulièrement étroite, la bande 5f tend à localiser les électrons qui s'y trouvent, de sorte que le plutonium pur à température ambiante est semblable aux matériaux à fermions lourds, avec une capacité thermique et une résistivité électrique élevées.
On connaît pas moins de six allotropes du plutonium à pression atmosphérique, et un septième au-delà de 60 MPa. Ils ont des propriétés bien tranchées et souvent inhabituelles pour un métal. Ainsi, le plutonium α, stable à température ambiante, est l'un des très rares métaux à cristalliser dans le système monoclinique ; ses propriétés physiques et structurelles relèvent davantage des minéraux que des métaux usuels, tandis que ses propriétés mécaniques rappellent celles de la fonte. Le plutonium δ, stable à température plus élevée ou avec une faible fraction molaire de gallium, cristallise en revanche dans une maille cubique à faces centrées, avec une masse volumique inférieure de près de 20 % à celle du plutonium α ; il est davantage métallique, avec des propriétés mécaniques semblables à l'aluminium, mais un coefficient de dilatation thermique négatif (il se contracte en chauffant). Le plutonium est également l'un des rares éléments chimiques dont le liquide est plus dense que le solide au point de fusion. L'existence de multiples allotropes aux énergies internes voisines rend la mise en forme du plutonium particulièrement délicate, au point qu'on utilise plutôt un alliage plutonium-gallium, qui stabilise la phase δ à température ambiante, ce qui facilite l'usinage des pièces en plutonium.
Le plutonium 239 et le plutonium 241 sont des isotopes fissiles par neutrons thermiques, ce qui signifie qu'ils peuvent contribuer à une réaction nucléaire en chaîne et qu'ils peuvent être utilisés dans la conception d'armes nucléaires et de réacteurs nucléaires. Le plutonium 240 présente un taux de fission spontanée très élevé qui impose d'en maintenir un taux inférieur à 7 % dans le plutonium de qualité militaire. Le plutonium 238 a une demi-vie de 88 ans et émet des particules α ; c'est une source de chaleur souvent utilisée par les générateurs thermoélectriques à radioisotopes pour alimenter certaines sondes spatiales en électricité. La séparation des isotopes du plutonium est difficile et ils sont généralement produits spécifiquement par des réacteurs spécialisés. La production de plutonium en quantité suffisante a été l'un des objectifs du projet Manhattan au cours de la Seconde Guerre mondiale afin de développer les premières bombes nucléaires. La première explosion atomique, l'essai Trinity, a utilisé une charge en plutonium, de même que Fat Man, la bombe atomique larguée sur Nagasaki ; la bombe Little Boy larguée trois jours plus tôt sur Hiroshima avait quant à elle un cœur en uranium enrichi.
Propriétés
-
Plutonium vu par la tranche sur le salt cake issu du procédé multicycle de réduction directe d'oxyde (MCDOR) : le dioxyde de plutonium PuO2 est dissous dans le chlorure de calcium CaCl2 fondu de 820 à 875 °C dans un creuset en oxyde de magnésium MgO pour y être réduit en plutonium métallique5.
Physique
Le plutonium est un métal de la famille des actinides présentant, comme la plupart des autres métaux, un aspect argenté brillant comme le nickel. Cependant, au contact de l'air, il se recouvre rapidement d'une couche terne grisâtre, avec des couleurs pouvant tirer sur le jaune ou le vert olive, cette dernière teinte provenant du dioxyde de plutonium6 PuO2.
Comme le neptunium et l'uranium — et, dans une moindre mesure, le protactinium — la structure électronique du plutonium aux conditions normales de température et de pression est déterminée par les orbitales 5f, qui contribuent de manière prépondérante aux liaisons interatomiques. Les distances entre atomes s'en trouvent réduites dans ces matériaux, qui présentent de ce fait une masse volumique particulièrement élevée : celle du plutonium vaut 19,816 g/cm3, plus du double de celle de l'einsteinium (8,84 g/cm3), qui a pourtant une masse atomique supérieure. Or les distances interatomiques dans un cristal influencent la largeur des bandes électroniques : plus ces distances sont petites, plus les bandes sont étroites. La bande 5f étant mathématiquement moins large que les bandes 6d et 7s, elle devient ici suffisamment étroite pour tendre à localiser les électrons dans le cristal, dont les propriétés métalliques sont par conséquent fortement dégradées7. De là provient toute la complexité du plutonium : compte tenu de la structure de bandes très particulière du matériau, où les bandes 5f et 6d ont des niveaux d'énergie très voisins, les électrons 5f du plutonium sont à la limite entre état localisé et état délocalisé dans le cristal, de sorte qu'une légère variation d'énergie interne suffit pour passer de l'un à l'autre, ce qui se traduit par des modifications brutales des propriétés macroscopiques du matériau.
Conséquence de l'influence des électrons 5f, les cristaux des actinides légers sont moins symétriques que ceux des métaux usuels, car les orbitales 5f sont très directionnelles8, et contraignent la géométrie des cristaux. Le protactinium cristallise dans le système quadratique, moins symétrique que ceux des métaux usuels, tandis que l'uranium et le neptunium cristallisent dans le système orthorhombique, encore moins symétrique, et que le plutonium cristallise dans le système monoclinique, le moins symétrique de tous. Il s'ensuit que le plutonium à l'état standard est peu ductile, peu malléable, peu plastique, et est au contraire plutôt dur et fragile ; on compare souvent ses propriétés mécaniques à celles de la fonte grise9.
Autre conséquence de l'influence des électrons 5f, le plutonium à l'état standard présente une faible conductivité électrique et une faible conductivité thermique, mais une capacité thermique élevée, ce qui l'apparente aux matériaux à fermions lourds7. De plus, sa conductivité électrique tend à décroître lorsqu'on refroidit le matériau10, ce qui est à l'opposé du comportement habituel des métaux. La tendance s'observe jusqu'à 100 K, puis s'inverse pour le plutonium frais ; la résistivité croît cependant avec le temps en raison des dommages au réseau cristallin dus à la radioactivité.
| Métal | Conductivité thermique | Résistivité électrique | Compressibilité | Module d'Young |
|---|---|---|---|---|
| Plutonium α | 4,2 W/m/K | 1,45 µΩ m | 0,020 GPa−1 | 100 GPa |
| Plutonium δ (Pu-Ga) | 9,2 W/m/K | 1,00 µΩ m | 0,033 GPa−1 | 42 GPa |
| Acier inoxydable | 15 W/m/K | 0,7 µΩ m | 0,000 7 GPa−1 | 180 GPa |
| Aluminium | 222 W/m/K | 0,029 µΩ m | 0,015 GPa-1 | 70 GPa |
D'une manière générale, la radioactivité désorganise la structure cristalline du plutonium par accumulation de défauts cristallins8. Cependant, l'auto-irradiation peut également chauffer suffisamment le matériau pour conduire à un recuit, ce qui contrebalance l'effet précédent pour des températures supérieures à 1 000 K12.
Isotopes
On connaît une vingtaine d'isotopes du plutonium. Le plutonium 244 présente la demi-vie la plus longue, avec 80,8 millions d'années, suivi par le plutonium 242, avec 373 300 ans, et le plutonium 239, avec 24 110 ans. Tous les autres isotopes du plutonium ont une demi-vie inférieure à 7 000 ans. Le plutonium présente également huit isomères nucléaires, dont la demi-vie est toujours inférieure à une seconde14.
Les isotopes connus du plutonium ont une masse atomique allant de 228 à 247. Le mode de désintégration privilégié des isotopes plus légers que le plutonium 244 est la fission spontanée et la désintégration α, qui produit essentiellement du neptunium et de l'uranium, ainsi qu'une grande variété de produits de fission. Le mode de désintégration privilégié des isotopes plus lourds que le plutonium 244 est la désintégration β, qui produit essentiellement de l'américium. Le plutonium 241 est l'isotope parent de la série de désintégration du neptunium, qui donne de l'américium 241 par désintégration β14,15.
Le plutonium 239 est, avec l'uranium 233 et l'uranium 235, l'un des trois principaux isotopes fissiles utilisés par l'industrie nucléaire ou à des fins militaires. Le plutonium 241 est également fortement fissile, c'est-à-dire qu'il peut fissionner sous l'impact d'un neutron thermique en libérant suffisamment d'autres neutrons pour permettre la fission d'autres atomes et entretenir ainsi une réaction en chaîne ; il est cependant bien plus radioactif que le plutonium 239, et produit, par désintégration β, de l'américium 241, un fort émetteur de particules α indésirables dans les applications habituelles du plutonium. Soumis à des neutrons thermiques, les isotopes 239Pu et 241Pu ont une probabilité d'environ 3⁄4 de fissionner et d'environ 1⁄4 de donner du 240Pu et du 242Pu respectivement, de sorte que le taux de 240Pu dans le plutonium résiduel après une réaction nucléaire est supérieur à celui du plutonium initial.
Sensiblement moins radioactif que la plupart des autres isotopes, le plutonium 239 pur présente cependant un facteur de multiplication keff supérieur à 1, ce qui signifie que ce matériau peut atteindre la masse critique pour peu qu'une quantité suffisante de matière soit rassemblée dans le volume approprié16. Au cours de la fission d'un atome, une fraction de l'énergie de liaison nucléaire, qui assure la cohésion du noyau atomique, est libérée sous forme d'énergie électromagnétique et d'énergie cinétique, cette dernière étant rapidement convertie en énergie thermique. La fission d'un kilogramme de plutonium 239 peut produire une explosion équivalente à 21 kt de TNT (88 000 GJ). C'est cette énergie qui est utilisée par les réacteurs nucléaires et les armes nucléaires15.
La présence de plutonium 240 dans une masse de plutonium 239 limite l'intérêt militaire de celui-ci car cet isotope présente un taux de fission spontanée supérieur de plus de quatre ordres de grandeur à celui du plutonium 239 — environ 440 fissions/s/g, soit plus de 1 000 neutrons/s/g17 — ce qui dégrade les performances explosives du matériau et accroît les risques d'explosion incontrôlée18. Le plutonium est dit de qualité militaire (weapon-grade) lorsqu'il contient moins de 7 % de plutonium 240, et de qualité combustible (fuel-grade) lorsqu'il en contient moins de 19 %. Le plutonium haute qualité (supergrade), contenant moins de 4 % de plutonium 240, est utilisé, en raison de sa plus faible radioactivité, pour les armes nucléaires devant être conservées à proximité immédiate des équipages, dans les sous-marins nucléaires lanceurs d'engins et les divers types de navires de guerre par exemple19. Le plutonium 238 n'est pas fissile mais peut facilement être fissionné sous l'effet de neutrons rapides ainsi que d'une radioactivité α15.
Les deux principaux isotopes synthétisés sont le plutonium 238 et le plutonium 23915. Le plutonium 239 est produit par capture neutronique puis désintégration β à partir d'uranium 23820 :
- 1
0n + 238
92U ⟶ 239
92U → 23.5 m i n β − {\displaystyle \mathrm {\xrightarrow[{23.5\ min}]{\beta ^{-}}} } 239
93Np → 2.3565 d β − {\displaystyle \mathrm {\xrightarrow[{2.3565\ d}]{\beta ^{-}}} } 239
94Pu.
Les neutrons issus de la fission de l'uranium 235 sont absorbés par les noyaux d'uranium 238 pour former de l'uranium 239 ; une désintégration β convertit alors un neutron en proton pour former du neptunium 239, converti par une seconde désintégration β en plutonium 239.
Le plutonium 238 est produit par bombardement d'uranium 238 avec des ions de deutérium21 :
-
2
1D + 238
92U ⟶238
93Np + 2 1
0n238
93Np → 2,117 j β − {\displaystyle \mathrm {\xrightarrow[{2{,}117\;\mathrm {j} }]{\beta ^{-}}} } 238
94Pu
Radioactivité
Hormis le plutonium 240, qui présente un fort taux de fission spontanée, et le plutonium 241, qui se désintègre par radioactivité β, la désintégration spontanée des principaux isotopes du plutonium se fait essentiellement par radioactivité α, c'est-à-dire par émission de particules α (He2+) qui se recombinent avec des électrons du métal pour former de l'hélium, tandis que le plutonium est transmuté en uranium. Ainsi, un cœur typique d'arme nucléaire de 5 kg contient 12,5 × 1024 atomes donnant une activité de 11,5 × 1012 Bq (désintégrations par seconde) émettant des particules α, ce qui correspond globalement à une puissance de 9,68 W 22,23.
-
Modes de désintégration principaux d'isotopes du plutonium24 Isotope Période radioactive
Activité
massiqueMode de
désintégrationNucléide
filsRapport de
branchementÉnergie de
désintégration238Pu 87,76 ans 6,34 × 1011 Bq/g Radioactivité α 234U 71,04 % 5,499 MeV 28,84 % 5,457 MeV 239Pu 24 130 ans 2,295 × 109 Bq/g Radioactivité α 235U 73,30 % 5,156 MeV 15,10 % 5,144 MeV 11,45 % 5,106 MeV 240Pu 6 567,5 ans 8,40 × 109 Bq/g Radioactivité α 236U 72,90 % 5,168 MeV 27,00 % 5,124 MeV 241Pu 14,29 ans 3,81 × 1012 Bq/g Radioactivité β 241Am 99,99 % 20,81 keV
Les radioisotopes du plutonium libèrent une chaleur de désintégration variable selon les isotopes considérés. Cette grandeur est généralement donnée en watts par kilogramme ou en milliwatts par gramme. Elle peut atteindre des valeurs significatives dans les pièces en plutonium de grande taille (par exemple, dans les têtes nucléaires). Tous les isotopes du plutonium libèrent également de faibles rayons γ.
-
Chaleur de désintégration d'isotopes du plutonium25 Isotope Chaleur de désintégration Fission spontanée (neutrons) Remarques 238Pu 560 W/kg 2 600 g−1 s−1 Chaleur de désintégration très élevée mise à profit dans les générateurs thermoélectriques à radioisotope 239Pu 1,9 W/kg 0,022 g−1 s−1 Principal isotope fissile du plutonium. 240Pu 6,8 W/kg 910 g−1 s−1 Principale impureté du plutonium 239. La qualité d'un plutonium est généralement exprimée en pourcentage de 240Pu. Son taux de fission spontanée est défavorable aux applications militaires. 241Pu 4,2 W/kg 0,049 g−1 s−1 Se désintègre en américium 241. Son accumulation présente un risque d'irradiation par les pièces de plutonium anciennes. 242Pu 0,1 W/kg 1 700 g−1 s−1
Allotropes
Il existe six allotropes du plutonium à pression atmosphérique, et un septième au-delà de 60 MPa8. Ces allotropes ont une énergie interne qui varie peu tandis que leurs propriétés physiques varient de façon spectaculaire. La masse volumique du plutonium pur à pression atmosphérique vaut ainsi 19,86 g/cm3 pour le plutonium α à température ambiante, mais seulement 15,92 g/cm3 pour le plutonium δ à 125 °C26, soit une densité 20 % plus faible, correspondant à un allongement linéaire de plus de 7,6 %. Le plutonium peut ainsi réagir violemment à des changements de pression, de température ou d'environnement chimique, et les transitions de phase peuvent s'accompagner de changements de volume significatifs et brutaux8.
-
Phases du plutonium à pression atmosphérique26 Phase Système cristallin Température de
transition de phaseMasse volumiquea α Monoclinique simple —b 19,86 g/cm3 β Monoclinique à bases centrées 124,5 °C 17,70 g/cm3 γ Orthorhombique à faces centrées 214,8 °C 17,14 g/cm3 δ Cubique à faces centrées 320,0 °C 15,92 g/cm3 δ’ Quadratique centré 462,9 °C 16,00 g/cm3 ε Cubique centré 482,6 °C 16,51 g/cm3 Liquide ~640 °C 16,65 g/cm3
- Systèmes cristallins du plutonium pur
-
Monoclinique (α)
-
Monoclinique à bases centrées (β)
-
Orthorhombique à faces centrées (γ)
-
Tétragonal centré (δ’)
-
Cubique centré (ε)
L'existence d'allotropes aussi différents pour des énergies internes aussi voisines rend la mise en forme du plutonium pur particulièrement délicate. Son état standard, la phase α, est monoclinique, faisant du plutonium pur à température ambiante un matériau dur et cassant comme la fonte grise, qui se prête fort peu à l'usinage et est susceptible de connaître de brusques variations de géométrie sous l'effet d'échauffements modérés. En revanche, la phase δ est cubique à faces centrées, comme de nombreux métaux usuels tels que l'aluminium et le nickel, et présente des propriétés mécaniques semblables à celles de l'aluminium. Stable de 320,0 à 462,9 °C pour le plutonium pur, la phase δ peut être stabilisée jusqu'à température ambiante moyennant l'adjonction d'une petite quantité de gallium, d'aluminium, d'américium, de scandium ou de cérium, qui permet d'usiner et de souder des pièces en plutonium10. L'alliage plutonium-gallium est fréquemment utilisé à cet effet, car il permet de s'affranchir des transitions de phases non désirées entraînant des distorsions dues à des gonflements ou des contractions localisés dans la pièce. Le silicium, l'indium, le zinc et le zirconium permettent la formation d'une phase δ métastable par refroidissement rapide. L'adjonction de grandes quantités d'hafnium, d'holmium et de thallium permet également de préserver la phase δ jusqu'à la température ambiante. Le neptunium est le seul élément qui stabilise la phase α monoclinique à température plus élevée8.
L'élasticité de la phase δ est anisotrope, pouvant varier d'un facteur six à sept selon les directions27.
Dans les armes à fission, l'onde de choc qui comprime le noyau (au-delà de quelques dizaines de kilobars) provoque également une transition de la phase δ vers la forme α, nettement plus dense, ce qui permet d'atteindre plus facilement la criticité27.
Alliages
Les alliages de plutonium peuvent être obtenus en ajoutant un métal à du plutonium fondu. Si le métal ajouté est suffisamment réducteur, le plutonium peut être apporté sous forme d'oxydes ou d'halogénures. L'alliage plutonium-gallium et l'alliage plutonium-aluminium, qui stabilisent la phase δ du plutonium à température ambiante, sont obtenus en ajoutant du trifluorure de plutonium PuF3 à du gallium ou de l'aluminium fondus, ce qui présente l'avantage d'éviter de manipuler du plutonium métallique, très réactif28.
- Plutonium-gallium Pu-Ga — Alliage principal utilisé pour la mise en forme, l'usinage et le soudage de pièces en plutonium en évitant les problèmes structurels posés par les transitions de phases α–δ. Il est utilisé principalement pour la réalisation d'armes nucléaires à implosion29.
- Plutonium-aluminium Pu-Al — Alternative à l'alliage plutonium-gallium, mais tend à interagir avec les particules α en émettant des neutrons, ce qui réduit son intérêt pour réaliser des armes nucléaires. Il peut en revanche être utilisé pour réaliser du combustible nucléaire30.
- Plutonium-gallium-cobalt PuCoGa5 — Supraconducteur non conventionnel présentant une supraconductivité en dessous de 18,5 K, un ordre de grandeur au-dessus du plus élevé des systèmes à fermions lourds, et avec un courant critique élevé.
- Plutonium-cérium Pu-Ce et plutonium-cérium-cobalt Pu-Ce-Co — Peuvent être utilisés comme combustibles nucléaires.
- Uranium-plutonium U-Pu — Avec environ 15 à 30 % d'atomes de plutonium, cet alliage peut être utilisé comme combustible nucléaire pour surgénérateurs. Il est pyrophorique et très sensible à la corrosion au point de s'enflammer ou de se désintégrer au contact de l'air, ce qui nécessite de l'allier à d'autres constituants. L'addition d'aluminium, de carbone ou de cuivre n'apporte aucune amélioration notable, tandis que le zirconium et le fer améliorent la résistance à la corrosion, mais ne permettent pas d'éviter la désintégration après plusieurs mois d'exposition à l'air. L'addition de titane ou de zirconium élève le point de fusion de l'alliage31.
- Uranium-plutonium-zirconium U-Pu-Zr — Peut être utilisé comme combustible nucléaire, notamment pour surgénérateurs32,33. Le titane et le zirconium accroissent la résistance à la corrosion, réduisent l'inflammabilité et améliorent la ductilité, la résistance, l'usinabilité et les caractéristiques thermiques. L'alliage uranium-plutonium-molybdène U-Pu-Mo présente la meilleure résistance à la corrosion, mais le titane et le zirconium sont préférés au molybdène en raison de meilleures propriétés physiques31.
- Thorium-uranium-plutonium Th-U-Pu — Étudié comme possible combustible nucléaire pour surgénérateurs31.
Chimie
Le plutonium pur à température ambiante présente des surfaces argentées qui ternissent en quelques minutes au contact de l'air15. Il présente quatre états d'oxydation courants en solution aqueuse, plus un cinquième plus rare35 :
- Pu(III), sous forme d'ion Pu3+ (bleu lavande)
- Pu(IV), sous forme d'ion Pu4+ (brun jaune)
- Pu(V), sous forme d'ion PuO2+ (rose pâle)c
- Pu(VI), sous forme d'ion PuO22+ (rose orangé)
- Pu(VII), sous forme d'ion PuO53− (vert ; cet ion heptavalent est rare).
Un complexe avec du plutonium à l'état d'oxydation formel +2, le [K(2.2.2-cryptand)][PuIICp″3], où Cp″ = C5H3(SiMe3)2, a également été publié37.
La couleur des solutions d'ions de plutonium dépend à la fois de l'état d'oxydation et de la nature de l'anion acide38. C'est ce dernier qui influence le degré de complexation du plutonium.
Le plutonium métallique est obtenu en faisant réagir du tétrafluorure de plutonium PuF4 avec du baryum, du calcium ou du lithium à 1 200 °C39. Il est attaqué par les acides, l'oxygène et la vapeur d'eau, mais pas par les bases. Il se dissout facilement dans l'acide chlorhydrique HCl, l'acide iodhydrique HI et l'acide perchlorique HClO4 concentrés10. Le plutonium fondu doit être maintenu sous vide ou sous atmosphère inerte afin d'éviter la réaction avec l'air10. À 135 °C, le plutonium métallique s'enflamme à l'air libre, et explose en présence de tétrachlorométhane40 CCl4.
Le plutonium réagit avec le carbone pour former des carbures de plutonium Pu3C2, PuC1-δ, Pu2C3 et PuC2 ; il réagit avec l'azote N2 pour former un nitrure PuN, et avec le silicium pour former un siliciure PuSi235,40 ; il réagit avec les halogènes X2, où X peut représenter de fluor, le chlore, le brome et l'iode, en donnant des trihalogénures PuX3. Avec le fluor, outre le trifluorure de plutonium PuF3, on observe également du tétrafluorure de plutonium PuF4 ainsi que de l'hexafluorure de plutonium PuF6. Il se forme par ailleurs des oxyhalogénures PuOCl, PuOBr et PuOI.
Les creusets utilisés avec du plutonium doivent être en mesure de supporter les propriétés très réductrices de ce métal. Les métaux réfractaires, tels que le tantale et le tungstène, ainsi que les oxydes, borures, carbures, nitrures et siliciures les plus stables, peuvent convenir. La fusion dans un four à arc électrique peut permettre de produire de petits lingots de plutonium métallique sans avoir besoin d'un creuset10.
Corrosion
Le plutonium pur exposé à l'humidité, que ce soit dans l'air ou dans l'argon, se recouvre en quelques minutes d'une couche terne constituée d'un mélange d'oxydes et d'hydrures26, qui se désagrège en formant une fine poussière volatile dont l'inhalation peut constituer un risque sanitaire sérieux. C'est la raison pour laquelle le plutonium est manipulé dans des boîtes à gants qui préviennent la dispersion atmosphérique de ces poussières.
Plus précisément, le plutonium exposé à l'air sec se recouvre d'une couche de dioxyde de plutonium PuO2 qui assure une passivation remarquable du métal, réduisant la progression de l'oxydation dans le matériau à une valeur aussi faible que 20 pm/h41. En revanche, la présence d'humidité introduit des hydrures PuHx, avec 1,9 < x < 3, qui catalysent la corrosion par l'oxygène O2, tandis que l'humidité en l'absence d'oxygène introduit des oxydes intermédiaires comme le sesquioxyde Pu2O3 qui favorisent la corrosion par l'hydrogène. Enfin, l'humidité en présence d'oxygène conduit à l'oxydation du dioxyde PuO2 pour former un oxyde supérieur PuO2+x sur la couche de dioxyde qui semble favoriser la corrosion du métal dans l'air humide41.
Les poudres de plutonium, de ses hydrures et de certains oxydes tels que Pu2O3 sont pyrophoriques, c'est-à-dire qu'elles peuvent prendre feu spontanément au contact de l'air à température ambiante, et sont par conséquent manipulées sous atmosphère sèche inerte d'azote N2 ou d'argon Ar. Le plutonium massif ne s'enflamme qu'au-dessus de 400 °C. Le Pu2O3 s'échauffe spontanément et se transforme en dioxyde de plutonium PuO2, qui est stable dans l'air sec, mais réagit à chaud avec la vapeur d'eau42. Les réactions en jeu seraient ainsi :
Le plutonium réagit également avec l'hydrogène H2 pour former des hydrures PuHx, avec 1,9 < x < 3 :
- 2 Pu + x H2 ⟶ 2 PuHx.
La valeur de x dépend de la pression partielle d'hydrogène et de la température de réaction. Ces hydrures, qui sont solides cristallisés dans le système cubique à faces centrées, sont rapidement oxydés par l'air, et se dissocient en leurs éléments constituants lorsqu'ils sont chauffés sous vide dynamique, c'est-à-dire avec pompage continu de l'hydrogène libéré.
Sûreté
Différents types de risques sont à considérer s'agissant de la manipulation du plutonium, qui dépendent étroitement des isotopes en jeu. Les accidents de criticité surviennent lors d'erreurs de manipulation conduisant à la formation d'une masse critique de plutonium et sont susceptibles de provoquer un syndrome d'irradiation aiguë. La radiotoxicité et la reprotoxicité se manifestent à la suite de l'absorption de plutonium dans l'organisme conduisant à l'irradiation des tissus avec des rayonnements ionisants pouvant provoquer des mutations génétiques et induire des cancers.
Les isotopes du plutonium les plus courants sont avant tout des émetteurs α, irradiant des particules α de 4,9 à 5,5 MeV qui sont facilement arrêtées par toute substance solide, notamment l'épiderme. Le plutonium 241 émet des rayons β, plus pénétrants que les rayons α, mais d'à peine 5,2 keV.
D'un point de vue chimique, le plutonium est combustible et pyrophorique, de sorte qu'il présente un risque d'incendie. Sa toxicité chimique, en revanche, n'est pas particulièrement significative.
Criticité
L'accumulation de plutonium dans un volume approchant de la masse critique est susceptible de conduire au déclenchement d'une réaction nucléaire émettant une quantité létale de neutrons et de rayons γ10. Le risque est d'autant plus grand avec le plutonium que la masse critique du plutonium 239 n'est généralement que le tiers de celle de l'uranium 23515. Ce risque est accru en solution en raison de l'effet modérateur de l'hydrogène de l'eau, qui thermalise les neutrons35.
Plusieurs accidents de criticité impliquant du plutonium ont été rapportés au XXe siècle, certains ayant entraîné la mort de personnes touchées. Ce fut par exemple le cas au laboratoire national de Los Alamos le 21 août 1945 lors d'une erreur de manipulation de briques en carbure de tungstène utilisées comme réflecteurs de neutrons autour d'une sphère en plutonium de qualité militaire, ce qui causa 25 jours plus tard la mort d'Harry Daghlian Jr., alors chercheur du projet Manhattan, à la suite d'un syndrome d'irradiation aiguë consécutif à la dose qu'il a reçue, estimée à 5,1 Sv43,44. Neuf mois plus tard, Louis Slotin mourut également à Los Alamos d'un accident semblable en manipulant des réflecteurs en béryllium autour de la même sphère en plutonium, appelée demon core45. Toujours à Los Alamos, un accident différent est survenu en , coûtant la vie à un laborantin, nommé Cecil Kelley, lors d'une opération de purification du plutonium, à la suite de la formation d'une masse critique dans un récipient de mélange. D'autres accidents de ce type se sont produits à travers le monde, que ce soit aux États-Unis, en Union soviétique, au Japon ou dans d'autres pays46.
Radiotoxicité
Élément synthétique produit spécifiquement pour sa radioactivité, le plutonium est surtout connu pour sa radiotoxicité. Celle-ci résulte de trois types de rayonnements ionisants : les rayons α (particules α), les rayons β (électrons) et les rayons γ (photons énergétiques). L'exposition aiguë ou prolongée à ces rayonnements présente des risques pour la santé, susceptibles de se manifester dans le cadre d'un syndrome d'irradiation aiguë, avec mutations génétiques et cancers. Les risques croissent avec la dose absorbée, mesurée en grays (Gy), et plus précisément en fonction de la dose équivalente, mesurée en sieverts (Sv), qui pondère l'impact physiologique des différents types de rayonnements reçus en fonction de leur capacité à causer des dommages dans les tissus irradiés. Cette pondération est introduite par le facteur de dose, mesuré typiquement en microsieverts par becquerel (µSv/Bq) :
-
Isotope Plutonium 238 Plutonium 239 Plutonium 240 Plutonium 241 Plutonium 242 Activité massique47 ~630 GBq/g ~2,3 GBq/g ~8,5 GBq/g ~3 700 GBq/g ~0,15 GBq/g Facteur de dose48 0,23 µSv/Bq 0,25 µSv/Bq 0,25 µSv/Bq 0,004 8 µSv/Bq 0,24 µSv/Bq
Ainsi, les rayons γ traversent tous les tissus et touchent l'ensemble de l'organisme, tandis que les rayons β sont moins pénétrants et que les rayons α ne franchissent pas l'épiderme mais sont bien plus énergétiques (quelques mégaélectron-volts, contre quelques kiloélectron-volts pour les rayons β et γ). Ainsi, les particules α sont dangereuses lorsqu'elles sont émises au sein même des tissus par le plutonium absorbé40. Le principal risque est l'inhalation de particules contenant du plutonium, notamment sous forme de dioxyde de plutonium PuO2, qui se forme rapidement au contact de l'air et qui tend à se désagréger en fines poussières en présence d'humidité. On a ainsi montré une incidence accrue du cancer du poumon chez des salariés du secteur nucléaire49. Le risque de cancer du poumon croît lorsque la dose équivalente de plutonium inhalé atteint 400 mSv50. En revanche, l'ingestion ne permet d'absorber que 0,04 % du PuO2 ingéré40. Les risques concernent également les os, où le plutonium s'accumule, ainsi que le foie, où il est concentré10.
Tous les isotopes du plutonium ne présentent pas le même niveau de radiotoxicité. Le plutonium de qualité militaire, constitué à plus de 92 % de plutonium 239, présente ainsi une radiotoxicité plutôt modérée51, en raison de son activité massique plus faible que celle du plutonium 240 et surtout du plutonium 238. Le plutonium 241 a une activité un millier de fois plus élevée, émettant des rayons β qui sont plus pénétrants que le rayonnement α, bien qu'un millier de fois moins énergétiques.
-
Énergie par mode de désintégration47 Isotope Plutonium 238 Plutonium 239 Plutonium 240 Plutonium 241 Plutonium 242 Rayonnement α 5,5 MeV 5,1 MeV 5,2 MeV < 1 keV 4,9 MeV Rayonnement β 11 keV 6,7 keV 11 keV 5,2 keV 8,7 keV Rayonnement γ 1,8 keV < 1 keV 1,7 keV < 1 keV 1,4 keV
Le plutonium 238 présente la plus forte radiotoxicité, tandis que le plutonium 241, dont la concentration dans le plutonium croît avec le temps, produit rapidement de l'américium 241, qui émet des rayons γ énergétiques susceptibles d'exposer l'environnement à une irradiation significative52.
La dose mortelle par syndrome d'irradiation aiguë constatée sur les expérimentations in vivo est de l'ordre de 400 à 4 000 µg/kg en une seule prise, une contamination chronique ayant des effets plus diffus53. On estime de ce fait qu'une quantité de l'ordre d'une dizaine de milligrammes provoque le décès d'une personne ayant inhalé en une seule fois des oxydes de plutonium. En effet, les tests effectués sur des babouins et des chiens conduisent à estimer pour l'homme une mortalité de 50 % au bout de 30 jours avec 9 mg, au bout d'un an avec 0,9 mg et 1 000 jours avec 0,4 mg54.
L'apparition de tumeurs pulmonaires a été mise en évidence chez le chien et le rat après inhalation de composés peu solubles tels que les oxydes de plutonium : la relation dose-effet mise en évidence comporte un seuil d'apparition des tumeurs pour une dose au poumon autour de 1 Gy54,55. Ce seuil d'apparition des tumeurs correspondrait chez l'homme à un dépôt pulmonaire d'environ 200 kBq, soit 87 µg) de 239PuO254.
Inflammabilité
Le plutonium présente un risque d'incendie, particulièrement lorsqu'il est sous forme de poudre finement divisée. En présence d'humidité, il forme à sa surface des hydrures qui sont pyrophoriques et sont susceptibles de prendre feu à température ambiante. Le risque est réel, et s'est matérialisé en 1969 par un important feu de plutonium au laboratoire national de Rocky Flats56. L'accroissement de volume résultant de l'oxydation du plutonium peut atteindre 70 % et briser les récipients de confinement42. La radioactivité de ce métal combustible constitue un risque supplémentaire.
L'oxyde de magnésium MgO est sans doute la substance la plus efficace pour éteindre un feu de plutonium : il refroidit le métal en agissant comme dissipateur thermique tout en coupant l'alimentation en oxygène de la combustion. Afin de prévenir les risques d'incendie, il est recommandé de manipuler le plutonium sous atmosphère sèche inerte42.
Toxicologie
Le plutonium présente la toxicité d'un métal lourd au même titre que l'uranium, par exemple, mais elle est moins documentée que celle de ce dernier, et les études ne placent pas la toxicité chimique comme risque majeur associé au plutonium57,58. Plusieurs populations exposées à des poussières de plutonium ont été suivies de près afin d'évaluer l'impact sur leur santé de leur contamination au plutonium59, comme les personnes résidant à proximité de sites d'expérimentation nucléaires atmosphériques lorsqu'ils étaient autorisés, les personnes travaillant dans des installations nucléaires, les rescapés du bombardement atomique de Nagasaki, voire des patients « en phase terminale » de maladies mortelles à qui a été injecté du plutonium dans les années 1945-1946 pour en observer la métabolisation dans le corps humain. Ces études ne montrent généralement pas de toxicité particulièrement élevée pour le plutonium, avec des exemples de cas célèbres comme celui d'Albert Stevens, cité par Bernard Cohen (en)58, qui vécut jusqu'à un âge avancé après avoir subi des injections de plutonium. Plusieurs dizaines de chercheurs du laboratoire national de Los Alamos ont également inhalé des quantités significatives de poussières de plutonium dans les années 1940 sans développer de cancer du poumon60.
Certains discours antinucléaires61,62,63,64,65,66 affirment que « l'ingestion d'un seul millionième de gramme est fatale », ce qui n'est pas étayé par la documentation existante67. Les données épidémiologiques des membres du « club des UPPUd », c'est-à-dire des 26 personnes ayant travaillé au laboratoire national de Los Alamos sur du plutonium et en ayant ingéré au point qu'il était suivi dans les urines, montrent par exemple une mortalité et un taux de cancers inférieurs à la moyenne68.
L'affirmation selon laquelle « Il suffirait de quelques centaines de grammes de plutonium répandue uniformément sur terre, pour y effacer toute forme de vie humaine »66 n'est pas non plus conforme aux données disponibles. On estime en effet que la dispersion d'une masse de l'ordre du kilogramme sur une surface de quelques centaines de kilomètres carrés (soit dans un rayon d'environ 10 km) conduit à une contamination inférieure au centième de microgramme par mètre carré65,69, de sorte quelques centaines de grammes répartis uniformément à la surface de la Terre seraient bien en deçà de toute quantité détectable.
Il convient également de distinguer la radiotoxicité du plutonium 238, qui est particulièrement élevée, de celle du plutonium 239 employé par l'armée et l'industrie nucléaire, dont la radioactivité spontanée est sensiblement moindre. Ces deux isotopes sont produits en quantités très différentes, par des circuits distincts et pour des usages qui n'ont aucun rapport : le plutonium 238 est produit à raison de quelques kilogrammes essentiellement comme source d'énergie embarquée pour générateur thermoélectrique à radioisotope, tandis que le plutonium 239 est produit à raison de plusieurs tonnes pour tirer profit de sa nature d'isotope fissile dans des réacteurs nucléaires ou des armes nucléaires70.
Toxicodynamique
Chez l'homme, le plutonium absorbé est transporté par des transferrines71,72,73,74 et est stocké dans le sang par la ferritine75,76,77,78 pour finir par s'accumuler essentiellement dans les os, également dans le foie, et, dans une moindre mesure, dans les poumons79. Il demeure dans le corps humain avec une demi-vie biologique d'environ 50 ans80. Un moyen courant d'en limiter les effets est d'injecter un complexe d'acide diéthylène-triamine penta-acétique81,82,83 (DTPA, parfois appelé « acide pentétique ») avec du calcium84 ou du zinc85 dans les 24 h suivant la contamination, ce qui limite la fixation du plutonium, ainsi que de l'américium et du curium. D'autres chélateurs peuvent également être utilisés, comme l'entérobactine86 et la déféroxamine, certains avec une meilleure efficacité que le DTPA, comme le 3,4,3-LIHOPO ou la DFO-HOPO87 (déféroxamine-hydroxypyridinone).
On estime que chez l'Homme, 10 % du plutonium qui a franchi la barrière intestinale ou pulmonaire quitte le corps (via l'urine, et les excréments). Le reste après passage dans le sang se fixe pour moitié dans le foie et pour moitié dans le squelette, où il demeure très longtemps et pour partie à vie (Le DOE américain estime que la demi-vie dans l'organe est respectivement de 20 et 50 ans pour le foie et l'os, selon des modèles simplifiés ne tenant pas compte de redistributions intermédiaires (en cas de fracture et/ou de ménopause (cf. décalcification) et lors du recyclage normal de l'os, etc). Le DOE précise que le taux accumulé dans le foie et le squelette dépend aussi de l'âge de l'individu (l'absorption dans le foie augmente avec l'âge), et qu'en fait, le plutonium se fixe d'abord sur la surface corticale et trabéculaire des os avant d'être lentement redistribué dans tout le volume minéral osseux.
Applications
Militaires
Le plutonium 239 est un isotope fissile clé pour la réalisation d'armes nucléaires en raison de sa relative facilité de mise en œuvre et de sa disponibilité assez élevée. Il est possible de réduire la masse critique nécessaire à l'explosion en entourant le cœur de plutonium par des réflecteurs de neutrons qui ont le double rôle d'augmenter le flux de neutrons thermiques dans le cœur et de retarder l'expansion thermique de ce dernier afin d'y prolonger la réaction en chaîne et d'accroître la puissance de l'explosion nucléaire.
Une masse de 10 kg de plutonium 239 sans réflecteur suffit généralement pour atteindre la criticité88 ; cette masse peut être divisée par deux par une conception optimisée. C'est environ le tiers de la masse critique de l'uranium 235.
La bombe Fat Man larguée sur Nagasaki par les États-Unis le 9 août 1945 utilisait une charge de 6,4 kg d'alliage plutonium-gallium 239Pu-240Pu-Ga 96:1:3 autour d'une source de neutrons d'amorçage Be-210Po le tout cerné de lentilles explosives comprimant le plutonium pour en accroître significativement la masse volumique et donc la puissance de l'explosion, qui atteignit l'équivalent de 20 000 t de TNT89. Il est en théorie possible de réduire la masse de plutonium nécessaire dans une arme nucléaire pour atteindre la criticité à moins de 4 kg moyennant une conception suffisamment élaborée.
Civiles
Le combustible nucléaire usagé provenant de réacteurs à eau légère conventionnels contient un mélange d'isotopes 238Pu, 239Pu, 240Pu et 242Pu. Ce mélange n'est pas suffisamment enrichi en plutonium 239 pour permettre la réalisation d'armes nucléaires mais peut être recyclé en combustible MOX. Les captures neutroniques accidentelles au cours de la réaction nucléaire accroissent la quantité de plutonium 240 et de plutonium 242 chaque fois que le plutonium est irradié dans un réacteur à neutrons thermiques de sorte que, à l'issue d'un premier cycle, le plutonium ne peut plus être utilisé que par des réacteurs à neutrons rapides. Si de tels réacteurs ne sont pas disponibles, ce qui est généralement le cas, le plutonium en excès est généralement éliminé en formant des déchets radioactifs à vie longue. La volonté de réduire la quantité de tels déchets et de les valoriser a poussé à réaliser davantage de réacteurs à neutrons rapides90.
Le procédé chimique le plus courant, dit PUREX, permet le retraitement du combustible nucléaire usé en extrayant le plutonium et l'uranium qu'il contient afin de former un mélange d'oxydes dit MOX, essentiellement du dioxyde d'uranium UO2 et du dioxyde de plutonium PuO2, pouvant être utilisé à nouveau dans des réacteurs nucléaires. Du plutonium de qualité militaire peut être ajouté à ce mélange pour en accroître les performances énergétiques. Le MOX peut être utilisé dans les réacteurs à eau légère et contient environ 60 kg par tonne de combustible ; après quatre années d'utilisation, les trois quarts du plutonium sont consommés. Les surgénérateurs sont conçus afin d'optimiser l'utilisation des neutrons produits au cours de la réaction nucléaire en les utilisant pour produire, à partir d'atomes fertiles, davantage de matériau fissile qu'ils en consomment90.
Le MOX est utilisé depuis les années 1980, notamment en Europe. Les États-Unis et la Russie ont signé, en , l'Accord de gestion et de traitement du plutonium (PMDA) par lequel ils entendent éliminer 34 tonnes de plutonium de qualité militaire ; le DOE américain prévoit d'avoir recyclé cette masse de plutonium en MOX avant la fin de l'année 201991.
Le MOX accroît le rendement énergétique total. Une barre de combustible nucléaire est retraitée après une utilisation de trois ans afin d'en extraire les déchets, qui représentent alors environ 3 % de la masse totale de ces barres40. Les isotopes d'uranium et de plutonium produits au cours de ces trois années d'exploitatione sont laissés dans la barre de combustible, qui retourne dans un réacteur pour y être utilisé. La présence de gallium jusqu'à hauteur de 1 % pondéral dans le plutonium de qualité militaire peut interférer avec l'utilisation à long terme de ce matériau dans un réacteur à eau légère92.
Les plus grandes installations déclarées de recyclage du plutonium sont les unités B205 (en) et THORP (en)f de Sellafield, au Royaume-Uni ; l'usine de retraitement de la Hague, en France ; l'usine nucléaire de Rokkasho, au Japon ; et le complexe nucléaire Maïak en Russie ; il existe d'autres sites déclarés plus modestes, par exemple en Inde et au Pakistan.
Spatiales
Le plutonium 238 a une demi-vie de 87,74 ans. Il émet une grande quantité d'énergie thermique accompagnée de faibles flux de neutrons et de photons d'énergie gamma. Un kilogramme de cet isotope peut dégager une puissance thermique d'environ 570 W. Il émet principalement des particules α d'énergie élevée mais qui sont faiblement pénétrantes, de sorte qu'il ne nécessite qu'un blindage léger. Une feuille de papier suffit pour arrêter des rayons α94.
Ces caractéristiques font de cet isotope du plutonium une source thermique particulièrement intéressante pour les applications embarquées devant fonctionner sans possibilité de maintenance directe pendant la durée d'une vie humaine. Il a par conséquent été utilisé comme source de chaleur dans les générateurs thermiques à radioisotope (RTG) et éléments chauffants à radioisotope (RHU) comme ceux des sondes Cassini-Huygens95, Voyager, Galileo et New Horizons, ainsi que le rover Curiosity de Mars Science Laboratory.
Les sondes jumelles Voyager ont été lancées en 1977, chacune avec une source en plutonium libérant une puissance de 500 W. Plus de 30 ans plus tard, ces sources d'énergie libéraient encore une puissance de 300 W permettant un fonctionnement limité des sondes96. Une version plus ancienne de cette technologie alimentait les cinq Apollo Lunar Surface Experiments Packages à partir d'Apollo 12 en 196940.
Le plutonium 238 a également été utilisé avec succès pour alimenter des stimulateurs cardiaques afin d'éviter les interventions chirurgicales répétées pour remplacer la source d'énergie97. Le plutonium 238 a depuis été largement remplacé dans cet usage par les piles au lithium, mais il restait encore en 2003 entre 50 et 100 patients aux États-Unis équipés de stimulateurs cardiaques alimentés au plutonium 23898.
Sécurité
Le plutonium étant susceptible d'être utilisé à des fins militaires ou terroristes, il fait l'objet de nombreux textes et conventions internationaux visant à en prévenir la prolifération. Le plutonium recyclé à partir de combustible nucléaire usé présente un risque de prolifération limité en raison de sa contamination élevée en isotopes non fissiles tels que le plutonium 240 et le plutonium 242, dont l'élimination n'est pas réalisable.
Un réacteur opérant avec un taux de combustion très faible produit peu de ces isotopes indésirables et laisse donc un matériau nucléaire potentiellement utilisable à des fins militaires. Le plutonium de qualité militaire est censé être constitué au moins de 92 % de plutonium 239, mais il est techniquement possible de faire exploser une bombe nucléaire de faible puissance à partir de plutonium ne contenant que 85 % de plutonium 239g. Le plutonium produit par un réacteur à eau légère avec un taux de combustion normal contient généralement moins de 60 % de plutonium 239, 10 % de plutonium 241 fissile et jusqu'à 30 % d'isotopes indésirables plutonium 240 et 242. On ignore s'il est possible de faire exploser un engin nucléaire constitué d'un tel matériau, cependant un tel engin pourrait probablement répandre de la matière radioactive sur une surface étendue.
L'Agence internationale de l'énergie atomique classifie ainsi tous les isotopes du plutonium, qu'ils soient fissiles ou non, comme matériau directement utilisable à des fins nucléaires, c'est-à-dire comme matériau nucléaire qui peut être utilisé pour la fabrication d'explosifs nucléaires sans transmutation ni enrichissement supplémentaire. En France, le plutonium est une matière nucléaire dont la détention est réglementée par le chapitre III du code de la Défense100.
Origine
Le plutonium est un élément chimique qui est des plus rares dans la nature et presque exclusivement produit par l'homme de 1940 à nos jours. Cependant, de 4 à 30 kg de plutonium 239 seraient produits chaque année sur Terre par radioactivité α de l'uranium sur des éléments plus légers ainsi que sous l'effet des rayons cosmiques101. C'est le deuxième des transuraniens à avoir été découvert.
L'isotope 238Pu a été produit en 1940 en bombardant une cible d'uranium par du deutérium au cyclotron de Berkeley102. Durant le projet Manhattan, le plutonium 239 avait le nom de code 49, le '4' étant le dernier chiffre de 94 (le numéro atomique) et le '9', le dernier chiffre de 239, la masse atomique de l'isotope utilisé pour la bombe, le 239Pu103.
Il n'y a plus de plutonium en quantités détectables remontant à une nucléosynthèse primordiale. Des publications anciennes font toutefois état d'observations de plutonium 244 naturel104. On trouve par ailleurs des traces de plutonium 239 dans les minerais d'uranium naturel (de même que du neptunium), où il résulte de l'irradiation de l'uranium par le très faible taux de neutrons créés par la désintégration spontanée de l'uranium.
Il a été produit plus massivement (et existe encore en quantités infimes) sous forme de 239Pu dans des structures géologiques particulières, où de l'uranium a été naturellement concentré par des processus géologiques il y a environ 2 milliards d'années, pour atteindre une criticité suffisante pour engendrer une réaction nucléaire naturelle. Son taux de formation dans le minerai d'uranium a ainsi été accéléré par des réactions nucléaires rendues possibles par un accident de criticité naturel. C'est le cas sur le site du réacteur nucléaire naturel d'Oklo.
Production
Plutonium 238
Dans les centrales nucléaires, du plutonium 238 est formé parallèlement au plutonium 239, par la chaîne de transformation commençant par l'uranium 235 fissible.
- L'uranium 235 qui capture un neutron thermique peut se stabiliser par émission d'un rayonnement γ dans 16 % des cas. Il forme alors un atome 236U, relativement stable (demi-vie de 23 millions d'années).
- Une deuxième capture neutronique le transforme en 237U (pour mémoire, des noyaux 238U peuvent également subir une réaction (n, 2n) qui les transforme en 237U par perte d'un neutron). L'uranium 237 est instable avec une demi-vie de 6,75 jours, et se transforme par émission β− en neptunium 237, relativement stable (demi-vie de 2,2 millions d'années).
- Une troisième capture neutronique transforme le noyau en neptunium 238, instable de demi-vie 2,1 jours, qui se transforme en plutonium 238 par émission β−.
Le plutonium 238, d'une demi-vie de 86,41 ans, est un émetteur très puissant de rayonnement α. En raison de son activité massique α et γ élevée, il est utilisé comme source de neutrons (par « réaction α » avec des éléments légers), comme source de chaleur et comme source d'énergie électrique (générateurs thermoélectriques à radiositopes). Les utilisations du 238Pu pour produire de l'électricité sont cantonnées aux utilisations spatiales, et, par le passé, à certains stimulateurs cardiaques.
On prépare le plutonium 238 à partir de l'irradiation neutronique du neptunium 237, un actinide mineur récupéré pendant le retraitement, ou à partir de l'irradiation de l'américium, en réacteur. Dans les deux cas, pour extraire le plutonium 238 des cibles, on les soumet à un traitement chimique, comportant une dissolution nitrique.
Il n'y a qu'environ 700 g/t de neptunium 237 dans le combustible des réacteurs à eau ordinaire irradié pendant 3 ans, et il faut l'extraire sélectivement.
Plutonium 239
L'irradiation de l'uranium 238 dans les réacteurs nucléaires génère du plutonium 239 par capture de neutrons. Dans un premier temps, un atome d'uranium 238 capture un neutron et se transforme transitoirement en uranium 239. Cette réaction de capture est plus facile avec des neutrons rapides qu'avec des neutrons thermiques, mais est présente dans les deux cas.
L'uranium 239 formé est fortement instable. Il se transforme rapidement (avec une demi-vie de 23,5 minutes) en neptunium par radioactivité β− :
Le neptunium 239 est également instable, et subit à son tour une décroissance β− (avec une demi-vie de 2,36 jours) qui le transforme en plutonium 239 relativement stable (demi-vie de 24 000 ans).
Le plutonium 239 est fissile, et il peut donc contribuer à la réaction en chaine du réacteur. De ce fait, pour le bilan énergétique d'un réacteur nucléaire, le potentiel énergétique de l'uranium présent dans le réacteur comprend non seulement celui de l'uranium 235 initialement présent, mais également celui de l'uranium 238 fertile qui aura été transmuté en plutonium.
Soumis à un flux neutronique en réacteur, le plutonium 239 peut également capturer un neutron sans subir de fission. Quand le combustible subit des périodes d'irradiation de plus en plus longues, les isotopes supérieurs s'accumulent de cette manière, en raison de l'absorption de neutrons par le plutonium 239 et ses produits. Il se forme ainsi des isotopes 240Pu, 241Pu, 242Pu, jusqu'au 243Pu instable qui se désintègre en américium 243.
L'isotope intéressant par son caractère fissile est le 239Pu, relativement stable à échelle humaine (24 000 ans).
Le rythme de production d'un isotope dépend de la disponibilité de son précurseur, qui doit avoir eu le temps de s'accumuler. Dans un combustible neuf, le 239Pu se forme donc linéairement en fonction du temps, la proportion de 240Pu augmente suivant une loi au carré du temps (en t2), celle de 241Pu suivant une loi au cube du temps (en t3), et ainsi de suite.
Ainsi, quand on utilise un réacteur spécifique pour la fabrication du « plutonium militaire », le combustible utilisé pour la production du plutonium aussi bien que les cibles et la couverture s'il y en a, sont extraits après un bref séjour (quelques semaines) dans le réacteur afin d'avoir l'assurance que le plutonium 239 est aussi pur que possible. En revanche, pour des usages civils, une brève irradiation n'extrait pas toute l'énergie que le combustible peut produire. On n'enlève donc le combustible des réacteurs électrogènes qu'après un séjour beaucoup plus long (3 ou 4 ans).
En première approximation, un réacteur produit typiquement 0,8 atome de 239Pu pour chaque fission de 235U, soit un gramme de plutonium par jour et par MW de puissance thermique (les réacteurs à eau légère produisant moins que les graphite-gaz). Ainsi, en France, les réacteurs nucléaires produisent chaque année environ 11 tonnes de plutonium105.
Plutonium 240
Le 240Pu est simplement fertile et présente une radioactivité « seulement » quatre fois plus élevée que le 239Pu (avec une demi-vie de 6 500 ans).
Plutonium 241
Le 241Pu est également fissile, mais extrêmement radioactif (demi-vie de 14,29 ans).
En outre il se désintègre en produisant de l'américium 241 neutrophage, qui réduit par son accumulation éventuelle l'efficacité des dispositifs nucléaires militaires ou civils.
Plutonium 242
Le 242Pu a une durée de vie beaucoup plus longue que les précédents (373 000 ans). Il n'est pas fissile en neutrons thermiques. Sa section efficace est beaucoup plus faible que celle des autres isotopes ; le recyclage successif du plutonium en réacteur tend donc à accumuler le plutonium sous cette forme très peu fertile.
Plutonium 243
Le 243Pu est instable (demi-vie de moins de 5 heures) et se désintègre en américium 243.
Plutonium 244
Le plutonium 244, l'isotope le plus stable d'une demi-vie de 80 millions d'années, ne se forme pas dans les réacteurs nucléaires. En effet, les captures neutroniques successives partant de l'uranium 239 conduisent au 243Pu, de très faible demi-vie (de l'ordre de cinq heures). Même dans des réacteurs « à haut flux », le 243Pu se transforme rapidement en 243Am, sans avoir le temps de capturer un neutron supplémentaire pour former le 244Pu.
En revanche, des flux neutroniques plus importants permettent cette formation. Il est synthétisé lors des explosions nucléaires ou par nucléosynthèse stellaire lors de l'explosion d'une supernova. Ainsi, en 1952, l'explosion de la première bombe thermonucléaire américaine (test Ivy Mike) a ainsi produit deux radioisotopes alors encore inconnus : le plutonium 244 (244Pu) et le plutonium 246 (246Pu). Les traces de 244Pu dans l'environnement sont généralement attribuées aux essais nucléaires atmosphériques ainsi qu'à des reliquats de 244Pu primordial.
Stocks mondiaux
Après près de 70 ans d'une production mondiale toujours croissante, les stocks déclarés de plutonium atteignent un total de 500 tonnes à la fin de l'année 2013, dont 52 % d'origine civile et 48 % militaire106. Les stocks déclarés sont essentiellement répartis entre 5 pays :
- Russie : 178 tonnes soit 35,6 %
- Royaume-Uni : 107,2 tonnes soit 21,4 %
- États-Unis : 88,3 tonnes soit 17,7 %
- France : 66,2 tonnes soit 13,2 %
- Japon : 47,1 tonnes soit 9,4 %
- Reste du monde : 13 tonnes soit 3 %
Notes
- À la température de transition de phase.
- Masse volumique correspondante donnée à 0 °C.
- L'ion PuO2+ est instable en solution et se dismute en Pu4+ et PuO22+ ; le Pu4+ oxyde alors le PuO2+ résiduel en PuO22+ en devenant lui-même du Pu3+. Une solution de PuO2+ devient donc au fil du temps un mélange de PuO22+ et de Pu3+. L'ion UO2+ est instable pour la même raison36.
- En anglais, UPPU se lit you pee Pu, c'est-à-dire « tu pisses du plutonium ».
- La composition isotopique du plutonium dans un combustible nucléaire usagé est de l'ordre de 58 % de 239Pu, 24 % de 240Pu, 11 % de 241Pu, 5 % de 242Pu et 2 % de 238Pu40.
- Une fuite importante de plutonium et d'uranium est survenue le 19 avril 2005 à l'usine THORP (en) à la suite d'une rupture de soudure dans une des cuves de retraitement. 200 kg de plutonium ont été perdus avec 83 000 L de matière radioactive provenant d'une cuve en béton armé conçue pour recueillir d'éventuelles pertes. Cette fuite a fait suite à une rupture de canalisation qui n'avait pas été détectée, les techniciens ayant ignoré, durant plusieurs mois, les indicateurs d'alerte à ce sujet, qui signalaient une perte de masse dans la cuve signifiant une fuite. Craignant un accident de criticité, l'autorité de sûreté a provisoirement fermé l'une des deux installations jumelles93.
- Les États-Unis ont ainsi fait exploser un engin nucléaire en 1962 à partir de combustible usé provenant d'un réacteur britannique Magnox, très probablement celui de la centrale nucléaire de Chapelcross, de type Calder Hall ; la composition isotopique de ce plutonium n'a pas été rendue publique mais n'excède certainement pas 85 % de plutonium 23999.
Notes et références
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », Dalton Transactions, , p. 2832 - 2838 (DOI 10.1039/b801115j)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC, , 89e éd., p. 10-203
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-420-09084-0)
- fiche IFA GESTIS
- (en) David L. Clark, Gordon Jarvinen, Cynthia Kowalczyk, Jim Rubin et Mary Ann Stroud, « Nitric Acid Processing » [archive] [PDF], Actinide Research Quarterly — 3rd Quarter 2008, sur Actinide Research Quarterly (ARQ) [archive] sur le site du Los Alamos National Laboratory, Seaborg Institute for Transactinium Science, (consulté le ), p. 10
- (en) David L. Clark, Gordon Jarvinen, Cynthia Kowalczyk, Jim Rubin et Mary Ann Stroud, « Nitric Acid Processing » [archive] [PDF], Actinide Research Quarterly — 3rd Quarter 2008, sur Actinide Research Quarterly (ARQ) [archive] sur le site du Los Alamos National Laboratory, Seaborg Institute for Transactinium Science, (consulté le ), p. 6 :
« While plutonium dioxide is normally olive green, samples can be various colors. It is generally believed that the color is a function of chemical purity, stoichiometry, particle size, and method of preparation, although the color resulting from a given preparation method is not always reproducible. »
- (en) A. Michael Boring et James L. Smith, « Plutonium Condensed-Matter Physics – A survey of theory and experiment », Los Alamos Science, no 26, , p. 90-127 (lire en ligne [archive])
- (en) Siegfried S. Hecker, « Plutonium and Its Alloys – From atoms to microstructure », Los Alamos Science, no 26, , p. 290-335 (lire en ligne [archive])
- (en) Siegfried S. Hecker et Michael F. Stevens, « Mechanical Behavior of Plutonium and Its Alloys », Los Alamos Science, no 26, , p. 336-355 (lire en ligne [archive])
- (en) William N. Miner et Fred W. Schonfeld, « Plutonium », The Encyclopedia of the Chemical Elements, 1968, Clifford A. Hampel, Reinhold Book Corporation, New York, pp. 540–546
- (en) Siegfried S. Hecker, « Plutonium, an element at odds with itself », Los Alamos Science, no 26, , p. 16-23 (lire en ligne [archive])
- (en) Siegfried S. Hecker et Joseph C. Martz, « Aging of Plutonium and Its Alloys », Los Alamos Science, no 26, , p. 238-243 (lire en ligne [archive])
- (en) Dana C. Christensen, « The Future Role of Plutonium Technology », Los Alamos Science, no 23, , p. 168-173 (lire en ligne [archive])
- (en) « Chart of Nuclides » [archive], sur National Nuclear Data Center (consulté le ).
- (en) David L. Heiserman, « Element 94: Plutonium », Exploring Chemical Elements and their Compounds, 1992, TAB Books, New York (NY), pp. 337–340. (ISBN 0-8306-3018-X).
- (en) Isaac Asimov, Nuclear Reactors, Understanding Physics, 1988, Barnes & Noble Publishing, New York. (ISBN 0-88029-251-2).
- (en) Samuel Glasstone et Leslie M. Redman, « An introduction to nuclear weapons » [PDF], sur web.archive.org, Atomic Energy Commission, (consulté le ).
- (en) F. G. Gosling, (1999). The Manhattan Project: Making the Atomic Bomb [archive] « Copie archivée » (version du 24 février 2009 sur l'Internet Archive) [PDF], 1999, United States Department of Energy, Oak Ridge. (ISBN 0-7881-7880-6)
- (en) « Plutonium: the 50 Years » [PDF], sur web.archive.org, U.S. Department of Energy, (consulté le ).
- (en) J. W. Kennedy, G. T. Seaborg, E. Segrè et A. C. Wahl, « Properties of 94(239) », Physical Review, vol. 70, nos 7-8, , p. 555-556 (DOI 10.1103/PhysRev.70.555, Bibcode 1946PhRv...70..555K, lire en ligne [archive])
- (en) Louis A. Turner, « Atomic Energy from U238 », Physical Review, vol. 69, nos 7-8, , p. 366-366 (DOI 10.1103/PhysRev.69.366, Bibcode 1946PhRv...69..366T, lire en ligne [archive])
- (en) David L. Heiserman, Exploring Chemical Elements and their Compounds, New York (NY), TAB Books, , 1re éd., 376 p. (ISBN 978-0-8306-3018-9, LCCN 91017687), « Element 94: Plutonium », p. 337–340
- (en) Richard Rhodes, The Making of the Atomic Bomb, New York, Simon & Schuster, , 1re éd., 886 p., poche (ISBN 978-0-671-65719-2, LCCN 86015445), p. 659–660 Leona Marshall : « Quand vous en prenez un lingot en main, on sent qu'il est chaud comme un lapin vivant ».
- K. Beaugelin-Seiller, D. Boust, P. Germain, S. Roussel-Debet et C. Colle, « Plutonium et environnement » [archive] [PDF], Fiche Radionucléide, sur http://www.irsn.fr/ [archive], Institut de radioprotection et de sûreté nucléaire, (consulté le ).
- (en) « Can Reactor Grade Plutonium Produce Nuclear Fission Weapons? » [archive], sur http://www.cnfc.or.jp/ [archive], Council for Nuclear Fuel Cycle Institute for Energy Economics Japan, (consulté le ).
- (en) « Plutonium, Radioactive » [archive] [html], National Institutes of Health (consulté le ).
- (en) « Plutonium Crystal Phase Transitions » [archive], GlobalSecurity.org
- (en) Kenton James Moody, Ian D. Hutcheon et Patrick M. Grant, Nuclear forensic analysis, 2005, CRC Press, p. 169. (ISBN 0-8493-1513-1)
- (en) David G. Kolman et Lisa P. Colletti, « Aqueous Corrosion Behavior of Plutonium Metal and Plutonium–Gallium Alloys Exposed to Aqueous Nitrate and Chloride Solutions », Journal of the Electrochemical Society, vol. 155, no 12, , C565-C570 (DOI 10.1149/1.2976352, lire en ligne [archive])
- (en) D. G. Hurst, A. G. Ward, Canadian Research Reactors [archive] [PDF], 1956, Atomic Energy of Canada Limited, Ottawa.
- (en) A. E. Kay, Plutonium 1965, 1965, Taylor & Francis.
- (en) Gerard L. Hofman, R. G. Pahl, C. E. Lahm et D. L. Porter, « Swelling behavior of U-Pu-Zr fuel », Metallurgical Transactions A, vol. 21, no 2, , p. 517-528 (DOI 10.1007/BF02671924, Bibcode 1990MTA....21..517H, lire en ligne [archive])
- (en) R. G. Pahl, D. L. Porter, C. E. Lahm et G. L. Hofman, « Experimental studies of U-Pu-Zr fast reactor fuel pins in the experimental breeder reactor-ll », Metallurgical Transactions A, vol. 21, no 7, , p. 1863–1870 (DOI 10.1007/BF02647233, Bibcode 1990MTA....21.1863P, lire en ligne [archive])
- (en) David L. Clark, « The Chemical Complexities of Plutonium », Los Alamos Science, no 26, , p. 364-381 (lire en ligne [archive])
- (en) David R. Lide, Handbook of Chemistry and Physics, 2006, CRC Press, Taylor & Francis Group 87e édition, Boca Raton. (ISBN 0-8493-0487-3)
- (en) William J. Crooks, « Nuclear Criticality Safety Engineering Training Module 10 – Criticality Safety in Material Processing Operations, Part 1 [archive] » [PDF], 2002.
- (en) Cory J. Windorff, Guo P. Chen, Justin N. Cross, William J. Evans, Filipp Furche, Andrew J. Gaunt, Michael T. Janicke, Stosh A. Kozimor et Brian L. Scott, « Identification of the Formal +2 Oxidation State of Plutonium: Synthesis and Characterization of {PuII[C5H3(SiMe3)2]3}− », Journal of the American Chemical Society, vol. 139, no 11, , p. 3970-3973 (PMID 28235179, DOI 10.1021/jacs.7b00706, lire en ligne [archive])
- (en) George Matlack, A Plutonium Primer: An Introduction to Plutonium Chemistry and Its Radioactivity [archive], Los Alamos national Laboratory, janvier 2003.
- (en) Mary Eagleson, Concise Encyclopedia Chemistry, 1994, Walter de Gruyter, Berlin, p. 840. (ISBN 978-3-11-011451-5).
- (en) John Emsley, (2001). « Plutonium », Nature's Building Blocks: An A–Z Guide to the Elements, 2001, Oxford University Press, Oxford (UK). (ISBN 0-19-850340-7).
- (en) John M. Haschke, Thomas H. Allen et Luis A. Morales, « Surface and Corrosion Chemistry of Plutonium », Los Alamos Science, no 26, , p. 252-273 (lire en ligne [archive])
- (en) « Plutonium », Primer on Spontaneous Heating and Pyrophoricity, sur web.archive.org, U.S. Department of Energy, Washington, D.C. 20585, (consulté le ).
- (en) Kevin N. Roark, « Criticality accidents report issued », laboratoire national de Los Alamos, 8 octobre 2008
- (en) Jon Hunner, Inventing Los Alamos, 2004 (ISBN 978-0-8061-3891-6).
- (en) « Raemer Schreiber », Staff Biographies, Los Alamos 16 novembre 2008.
- (en) William R. Stratton, « A Review of Criticality Accidents » [archive] [PDF], Laboratoire national de Los Alamos, (consulté le ).
- (en) John Peterson, Margaret MacDonell, Lynne Haroun et Fred Monette, « Radiological and Chemical Fact Sheets to Support Health Risk Analyses for Contaminated Areas » [archive] [PDF], sur Radiation Emergency Medical Management, Argonne National Laboratory Environmental Science Division, (consulté le ).
- Ch. O. Bacri, « La gestion des déchets nucléaires » [archive] [PDF], De la physique au détecteur, sur http://www.in2p3.fr [archive], IN2P3, (consulté le ), p. 17.
- (en) James Grellier, Will Atkinson, Philippe Bérard, Derek Bingham, Alan Birchall, Eric Blanchardon, Richard Bull, Irina Canu Guseva, Cécile Challeton-de Vathaire, Rupert Cockerill, Minh T. Do, Hilde Engels, Jordi Figuerola, Adrian Foster, Luc Holmstock, Christian Hurtgen, Dominique Laurier, Matthew Puncher, Anthony E. Riddell, Eric Samson, Isabelle Thierry-Chef, Margot Tirmarche, Martine Vrijheid et Elisabeth Cardis, « Risk of lung cancer mortality in nuclear workers from internal exposure to alpha particle-emitting radionuclides », Epidemiology, (DOI 10.1097/EDE.0000000000000684, lire en ligne [archive])
- FAS fact sheet [archive]
- (en) Reuben Rainisch, « Effect of Americium-241 Content on Plutonium Radiation Source Terms » [archive] [PDF], American Nuclear Society 1999 Annual Meeting and Embedded Topical at Boston, (consulté le ).
- (en) William Moss et Roger Eckhardt, « The Human Plutonium Injection Experiments », Los Alamos Science, vol. 23, , p. 177-233 (lire en ligne [archive])
- Guillaume Phan, François Rebière, Jean-Michel Deligne et Jean-René Jourdain, « Plutonium : Aspects sanitaires » [archive] [PDF], Fiche radionucléide, sur http://centredoc.ecole-eme.fr/opac/ [archive] de l'École des métiers de l'environnement (France), IRSN, (consulté le ), p. 5.
- Fiche radiotoxicologique Plutonium [archive], CEA, décembre 2005.
- (en) David Albright et Kevin O'Neill, « The Lessons of Nuclear Secrecy at Rocky Flats », sur https://web.archive.org/, Institute for Science and International Security, (consulté le ).
- (en) Bernard L. Cohen, « Hazards from Plutonium Toxicity », Health Physics, vol. 32, no 5, , p. 359-379 (PMID 881333, DOI 10.1097/00004032-197705000-00003, lire en ligne [archive])
- (en) Bernard L. Cohen, « The Myth of Plutonium Toxicity », sur web.archive.org, (consulté le ).
- (en) « Toxicological Profile for Plutonium » [archive], sur ATSDR [archive] Toxic Substances Portal, Agency for Toxic Substances & Disease Registry, (consulté le ).
- (en) G. L. Voelz, « What We Have Learned about Plutonium from Human Data », Health Physics, vol. 29, no 4, , p. 551-561 (PMID 1205858, DOI 10.1097/00004032-197510000-00011, lire en ligne [archive])
- radioactivité naturelle et artificielle [archive], l'électron libre, 12/2002
- Nucléaire : comment en sortir ? [archive], Réseau "Sortir du nucléaire", 2007.
- La lettre d'information avril 2011 [archive], EELV Midi-Pyrénées.
- Fleur Australe [archive], Géraldine Danon, Flammarion -Arthaud, 2012.
- L’exploration spatiale, "nouvelle frontière" du nucléaire ? [archive], Sortir du nucléaire no 56 - Hiver 2012-2013
- Y'a quéqu' chose qui cloche là-d'dans... [archive], Le blog de Gdalia Roulin, Mediapart, 4 juillet 2015.
- (en) « Toxicological Profile for Plutonium » [archive] [PDF], Toxic Substances Portal, sur ATSDR [archive] - Plutonium, Agency for Toxic Substances and Disease Registry (ATSDR) et U.S. Environmental Protection Agency (EPA), (consulté le ).
- (en) Jeremy Bernstein, Plutonium : a history of the world's most dangerous element, 2007, Joseph Henry Press, Washington, D.C. (ISBN 978-0-309-10296-4)
- The Curiosity Mission: Nukes in Space [archive], Karl Grossman.
- Plutonium Watch: Tracking Plutonium Inventories [archive], ISIS Reports, June 2004.
- (en) G. A. Turner et D. M. Taylor, « The Binding of Plutonium to Serum Proteins in Vitro », Radiation Research, vol. 36, no 1, , p. 22-30 (PMID 17387923, DOI 10.2307/3572534, JSTOR 3572534, lire en ligne [archive])
- (en) A. R. Chipperfield et D. M. Taylor, « Binding of Plutonium to Glycoproteins in Vitro », Radiation Research, vol. 43, no 2, , p. 393-402 (PMID 5465552, DOI 10.2307/3573043, JSTOR 3573043, lire en ligne [archive])
- (en) Mark P. Jensen, Drew Gorman-Lewis, Baikuntha Aryal, Tatjana Paunesku, Stefan Vogt, Paul G. Rickert, Soenke Seifert, Barry Lai, Gayle E. Woloschak et L. Soderholm, « An iron-dependent and transferrin-mediated cellular uptake pathway for plutonium », Nature Chemical Biology, vol. 7, no 8, , p. 560-565 (PMID 21706034, PMCID 3462652, DOI 10.1038/nchembio.594, lire en ligne [archive])
- (en) John R. Cooper et Helen S. Gowing, « The Binding of Americium and Curium to Human Serum Proteins », International Journal of Radiation Biology and Related Studies in Physics, Chemistry and Medicine, vol. 40, no 5, , p. 569-572 (PMID 6975262, DOI 10.1080/09553008114551541, lire en ligne [archive])
- (en) David M. Taylor et George J. Kontoghiorghes, « Mobilisation of plutonium and iron from transferrin and ferritin by hydroxypyridone chelators », Inorganica Chimica Acta, vol. 125, no 3, , L35-L38 (DOI 10.1016/S0020-1693(00)84710-6, lire en ligne [archive])
- (en) David M. Taylor, Arnulf Seidel, Felicitas Planas-Bohne, Ute Schuppler, Margarethe Neu-Müller et Rainer E. Wirth, « Biochemical studies of the interactions of plutonium, neptunium and protactinium with blood and liver cell proteins », Inorganica Chimica Acta, vol. 140, , p. 361-363 (DOI 10.1016/S0020-1693(00)81124-X)
- (en) F. W. Bruenger, B. J. Stover et W. Stevens, « 239Pu(IV): its subcellular distribution and association with ferritin in the canine liver », Health Physics, vol. 21, no 5, , p. 679-687 (PMID 5112182, DOI 10.1097/00004032-197111000-00009, lire en ligne [archive])
- (en) G. Boocock, C. J. Danpure, D. S. Popplewell et D. M. Taylor, « The Subcellular Distribution of Plutonium in Rat Liver », Radiation Research, vol. 42, no 2, , p. 381-396 (PMID 4315168, DOI 10.2307/3572805, JSTOR 3572805, lire en ligne [archive])
- (en) N. P. Singh, M. D. E. Wrenn et S. A. Ibrahim, « Plutonium concentration in human tissues: comparison to thorium », Health Physics, vol. 44, no Suppl. 1, , p. 469-476 (PMID 6862922, DOI 10.1097/00004032-198306001-00045, lire en ligne [archive])
- (en) « Appendix D. Overview of basic radiation physics, chemistry, and biology » [archive] [PDF], Toxic Substances Portal, sur ATSDR [archive] - Plutonium, Agency for Toxic Substances and Disease Registry (ATSDR) et U.S. Environmental Protection Agency (EPA), (consulté le ), p. D-4.
- (en) K. Konzen et R. Brey, « Development of the Plutonium-DTPA Biokinetic Model », Health Physics, vol. 108, no 6, , p. 565-573 (PMID 25905517, DOI 10.1097/HP.0000000000000283, lire en ligne [archive])
- (en) M. Alex Brown, Alena Paulenova et Artem V. Gelis, « Aqueous Complexation of Thorium(IV), Uranium(IV), Neptunium(IV), Plutonium(III/IV), and Cerium(III/IV) with DTPA », Inorganic Chemistry, vol. 51, no 14, , p. 7741-7748 (PMID 22738207, DOI 10.1021/ic300757k, lire en ligne [archive])
- (en) F.Ménétrier, L.Grappin, P.Raynaud, C.Courtay, R.Wood, S.Joussineau, V.List, G. N. Stradling, D. M. Taylor, Ph. Bérard, M. A. Morcillo et J.Rencova, « Treatment of accidental intakes of plutonium and americium: Guidance notes », Applied Radiation and Isotopes, vol. 62, no 6, , p. 829-846 (PMID 15799861, DOI 10.1016/j.apradiso.2005.01.005, lire en ligne [archive])
- (en) A. L. Sérandour, N. Tsapis, C. Gervelas, G. Grillon, M. Fréchou, J. R. Deverre, H. Bénech, E. Fattal, P. Fritsch et J. L. Poncy, « Decorporation of plutonium by pulmonary administration of Ca-DTPA dry powder: a study in rat after lung contamination with different plutonium forms », Radiation Protection Dosimetry, vol. 127, nos 1-4, , p. 472-476 (PMID 17562654, DOI 10.1093/rpd/ncm300, lire en ligne [archive])
- (en) David M. Taylor, Susan A. Hodgson et Neil Stradling, « Treatment of human contamination with plutonium and americium: would orally administered Ca- or Zn-DTPA be effective? », Radiation Protection Dosimetry, vol. 127, nos 1-4, , p. 469-471 (PMID 17556346, DOI 10.1093/rpd/ncm299, lire en ligne [archive])
- (en) Pihong Zhao, Vadim V. Romanovski, Donald W. Whisenhunt Jr, Darleane C. Hoffman, Thomas R. Mohs, Jide Xu et Kenneth N. Raymond, « Extraction of plutonium by chelating hydroxypyridinone and catecholamide resins », Solvent Extraction and Ion Exchange, vol. 17, no 5, , p. 1327-1353 (DOI 10.1080/07366299908934651, lire en ligne [archive])
- (en) V. Volf, R. Burgada, K. N. Raymond et P. W. Durbin, « Early Chelation Therapy for Injected Pu-238 and Am-241 in the Rat: Comparison of 3,4,3-LIHOPO, DFO-HOPO, DTPA-DX, DTPA and DFOA », International Journal of Radiation Biology, vol. 63, no 6, , p. 785-793 (PMID 8100266, DOI 10.1080/09553009314552191, lire en ligne [archive])
- (en) A. Blanchard, K. R. Yates, J. F. Zino, D. Biswas, D. E. Carlson, H. Hoang et D. Heemstra, « Updated Critical Mass Estimates for Plutonium-238 » [archive], sur https://www.osti.gov/ [archive], U.S. Department of Energy: Office of Scientific & Technical Information (consulté le ).
- (en) John Malik, « The Yields of the Hiroshima and Nagasaki Nuclear Explosions » [archive] [PDF], sur https://fas.org/ [archive], Laboratoire national de Los Alamos, (consulté le ).
- (en) C. E. Till, Y. I. Chang, Plentiful Energy: The Story of the Integral Fast Reactor, the Complex History of a Simple Reactor Technology, with Emphasis on Its Scientific Basis for Non-specialists, 2011, Charles E. Till and Yoon Il Chang, pp. 254-256. (ISBN 978-1-4663-8460-6)
- (en) (en) « Plutonium Storage at the Department of Energy's Savannah River Site: First Annual Report to Congress » [archive] [PDF], sur https://www.dnfsb.gov [archive], Defense Nuclear Facilities Safety Board, (consulté le ), A-1.
- (en) Theodore M. Besmann, « Thermochemical Behavior of Gallium in Weapons-Material-Derived Mixed-Oxide Light Water Reactor (LWR) Fuel », Journal of the American Ceramic Society, vol. 81, no 12, , p. 3071–3076 (DOI 10.1111/j.1151-2916.1998.tb02740.x, lire en ligne [archive])
- (en) « Huge radioactive leak closes Thorp nuclear plant » [archive], sur https://www.theguardian.com [archive], The Guardian, (consulté le ).
- (en) « From heat sources to heart sources: Los Alamos made material for plutonium-powered pumper » [archive], sur http://www.lanl.gov [archive], Laboratoire national de Los Alamos (consulté le ).
- (en) « Why the Cassini Mission Cannot Use Solar Arrays », sur https://web.archive.org, Jet Propulsion Laboratory, (consulté le ).
- (en) « Voyager Spacecraft » [archive], sur https://www.jpl.nasa.gov [archive], Jet Propulsion Laboratory (consulté le ).
- (en) Venkateswara Sarma Mallela, V. Ilankumaran et N.Srinivasa Rao, « Trends in Cardiac Pacemaker Batteries », Indian Pacing and Electrophysiology Journal, vol. 4, no 4, , p. 201-212 (PMID 16943934, PMCID 1502062, lire en ligne [archive])
- (en) « Plutonium Powered Pacemaker (1974) » [archive], sur http://www.orau.org [archive], Oak Ridge Associated Universities (en), (consulté le ).
- (en) « Plutonium » [archive], sur http://www.world-nuclear.org/ [archive], Association nucléaire mondiale (consulté le ).
- « Code de la défense » [archive], sur https://www.legifrance.gouv.fr [archive] (consulté le ).
- Henri Métivier, « Plutonium - Mythes et réalités » [archive] (consulté le )
- Plutonium production [archive], Federation of American Scientists.
- (en) E.F. Hammel, « The taming of "49" — Big Science in little time. Recollections of Edward F. Hammel » [archive], Los Alamos Science, Vol 26, Iss. 1, 2000 (consulté le ). Cette convention a été étendue pour tous les actinides, dans les équations décrivant la dynamique de leur population dans des réacteurs. Ainsi, l'isotope 235 de l'uranium (92) reçoit dans les équations l'indice 25 et ainsi de suite.
- (en) D. C. Hoffman, F. O. Lawrence, J. L. Mewherter et F. M. Rourke, « Detection of Plutonium-244 in Nature », Nature, vol. 234, no 5325, , p. 132-134 (DOI 10.1038/234132a0, Bibcode 1971Natur.234..132H, lire en ligne [archive])
- Rapport Bataille [archive] 1997/1998 au Sénat.
- (en) « Alternatives to MOX - Direct-disposal options for stockpiles of separated plutonium » [archive], sur http://fissilematerials.org [archive], (consulté le )
Voir aussi
Bibliographie
- (en) David R. Lide et al., Handbook of Chemistry and Physics, Boca Raton (FL), CRC Press, Taylor & Francis Group, , 87e éd., 2608 p. (ISBN 0-8493-0487-3)
- Sandrine Matton ; Mesures in vitro et in vivo des paramètres de dissolution des oxydes mixtes d'uranium et de plutonium en milieu biologique (In vitro and in vivo measurements of dissolution parameters of mixed uranium and plutonium oxides in biological medium) ; Thèse de Sandrine Matton (sous la direction de Michel Genet), soutenue à l'université de Paris 11 Orsay (Inist CNRS [archive])
- IEER, Énergie & Sécurité no 3 [archive] Sommaire : L'utilisation du plutonium militaire comme combustible de réacteur ; Les effets du plutonium sur la santé ; Le MOX en France et en Belgique ; Situation et perspective pour la production du combustible MOX en Russie ; La transmutation n'est pas une alternative à l'enfouissement ; La transformation du plutonium avec le temps], Énergie & Sécurité no 3, 1997 (scan PDF)
Articles connexes
Liens externes
- (en) « Technical data for Plutonium » [archive] (consulté le ), avec en sous-pages les données connues pour chaque isotope
- (en) Les expérimentations humaines sur le plutonium aux États-Unis [archive] (Los Alamos Science, 23, 1995)
- (en) Plutonium [archive], par le "World Nuclear Association"
- « Les isotopes du plutonium et leurs descendants dans le nucléaire civil » [archive] (consulté le ), rapport à l'Académie des sciences par Robert Dautray - Paris - - Éditions Tec & Doc Lavoisier.
- Plutonium, Mythes et Réalités - Janvier 2010 - EDP Sciences. [archive]
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
| Métaux Alcalins |
Alcalino- terreux |
Lanthanides | Métaux de transition |
Métaux pauvres |
Métal- loïdes |
Non- métaux |
Halo- gènes |
Gaz nobles |
Éléments non classés |
| Actinides | |||||||||
| Superactinides | |||||||||
Modèle de Bohr
Pour les articles homonymes, voir Bohr.
Le modèle de Bohr est une théorie obsolète dans le domaine de la physique/chimie, cherchant à comprendre la constitution d'un atome, et plus particulièrement celui de l'hydrogène et des ions hydrogénoïdes (ions ne possédant qu'un seul électron). Élaborée par Niels Bohr en 1913, cette théorie établie sur le modèle planétaire de Rutherford rencontra un succès immédiat car elle expliquait de manière simple les raies spectrales des éléments hydrogénés tout en effectuant un rapprochement entre les premiers modèles de l'atome et la théorie des quanta. Ce modèle sera généralisé au cas des électrons relativistes par Arnold Sommerfeld afin d'écrire de façon quantitative la structure fine des lignes spectrales de l'hydrogène. Cependant, cette théorie ne peut expliquer le spectre d'éléments à plusieurs électrons (comme celui de l'hélium), ni la nature des liaisons chimiques, et elle est totalement abandonnée au profit de la mécanique quantique à partir de 1925.
Histoire
Développement de la spectroscopie
Durant les XVIIIe et XIXe siècles, la spectroscopie se développe, et on mesure des spectres de différentes sources lumineuses comme le soleil ou la lampe à hydrogène. Depuis Thomas Melvill (1726-1753) en 1750, on comprend que les spectres des éléments chimiques sont discrets et formés de raies spectrales. La spectroscopie théorique naît avec la loi du rayonnement de Gustav Kirchhoff (1824-1887), publiée en 1859, qui explique l'équivalence entre le spectre d'émission et le spectre d'absorption des substances chimiques. En collaboration avec Robert Bunsen (1811-1899), ils expliquent les raies de Fraunhofer du soleil comme étant la signature de trente éléments chimiques présents dans les couches supérieures du soleil. Ainsi chaque élément chimique possède un spectre unique et caractéristique. Toutefois, pour chaque élément, le nombre et la position des raies restaient inexpliqués. Le plus simple d'entre eux, le spectre de l'hydrogène, fut alors intensivement étudié et on trouva bientôt des « séries » de raies comme celles de Lyman, Balmer, Paschen, etc., du nom de leur découvreurs. Johann Balmer (1825-1898) trouve en 1855 une expression empirique simple qui explique sa série en accord avec les raies trouvées dans le visible par Ångström et dans l'ultraviolet par Huggins : la longueur d'onde λ {\displaystyle \lambda } des raies est liée à la différence entre deux termes d'énergie — appelés « termes spectraux » — par
où n et p sont des nombres entiers associés à deux raies différentes de la série. En 1888, Johannes Rydberg et Walther Ritz généralisent ce résultat avec la formule de Rydberg, formule qui reste empirique mais qui introduit la constante de Rydberg et qui s’avérera valide pour les autres séries. Toutefois, il faudra attendre les travaux de Max Planck en 1900 et ceux d'Albert Einstein en 1905 pour comprendre que le rayonnement électromagnétique peut être émis (rayonnement du corps noir) ou absorbé (effet photoélectrique) avec une certaine quantité d'énergie discrète ou quantifiée ; c'est le concept du photon qui transporte l'énergie :
où h désigne la constante de Planck et c la vitesse de la lumière dans le vide.
Concept de l'atome
Un autre apport fondamental viendra du concept encore controversé d'atome et de son étude : la notion de grain élémentaire de matière fera d'abord son chemin chez les chimistes (John Dalton) puis chez les physiciens (Ludwig Boltzmann). De plus, le tableau périodique des éléments, établi par Dimitri Mendeleïev en 1869, indique que les éléments purs peuvent être regroupés en lignes et en colonnes dans un tableau suivant leurs propriétés chimiques. Si atomes il y a, ces derniers semblent alors présenter des sous-structures. En 1897, Joseph John Thomson identifie l'électron comme étant une particule élémentaire chargée négativement. Il propose alors le modèle de Thomson où l'atome est composé d'électrons plongés dans une « soupe » ou nuage de charge positive pour équilibrer la charge négative des électrons. Ces derniers sont considérés comme dispersés au sein de l'atome, mais avec de multiples structures possibles pour leurs positionnements (des anneaux tournants d'électrons par exemple). Ce modèle fut réfuté en 1909 par des expériences de bombardement de feuilles d'or d'Ernest Rutherford et en 1911, ce dernier montra l'existence d'un très petit noyau chargé positivement, ce qui le conduisit par la suite à proposer le modèle atomique de Rutherford : un atome est constitué d'électrons négatifs qui orbitent sur des trajectoires circulaires autour d'un noyau dense positif, à la manière des planètes du système solaire qui orbitent de manière quasi circulaire autour du Soleil, la force électromagnétique remplaçant alors la force de gravitation comme force de cohésion du système. Toutefois, la théorie planétaire de Rutherford se heurtait à la théorie du rayonnement de l'électron accéléré. En effet, d'après les observations expérimentales et les lois de Maxwell, un électron soumis à une accélération émet de l'énergie sous forme de champ électromagnétique (c'est la formule de Larmor, établie par Joseph Larmor en 1897). Ramené au niveau de l'atome de Rutherford, l'électron devrait décrire une spirale concentrique, et non un cercle, pour finir par s'écraser sur le noyau au bout de quelques millions de révolutions, ce qui correspond à une nanoseconde. Les orbites ne sont donc pas stables.
L'article de Bohr
En 1913, le physicien danois Niels Bohr (1885-1962) introduit alors trois postulats pour rendre ce modèle compatible avec les observations du spectre de l'hydrogène : le premier postulat suppose qu'il existe des orbites circulaires stables pour les électrons, c'est-à-dire qu'une fois sur une de ces orbites, l'électron ne rayonne aucune énergie électromagnétique. Il ne décroit donc pas en spirale et peut rester indéfiniment sur cette orbite. De telles orbites sont dites stationnaires et sont donc similaires à des orbites kepleriennes sur lesquelles l'orbiteur ne ressent aucune accélération. En outre, chacune d'elles correspond à une énergie bien définie de l'électron (on parle alors de niveau d'énergie de l'électron, qui sont ici de valeur négative pour signifier que le système noyau-électron est lié). Selon le deuxième postulat, l'électron peut passer d'une orbite stable à une autre, c'est-à-dire d'un niveau d'énergie à un autre, par absorption ou émission d'un quantum d'énergie h ν {\textstyle h\nu } encore appelé photon. L'absorption d'un photon fait ainsi passer l'électron d'une orbite basse (proche du noyau) d'énergie faible à une orbite haute (loin du noyau) d'énergie plus élevée. L'émission d'un photon correspond à l'opération inverse : l'électron passe d'une orbite éloignée de haute énergie à une orbite proche du noyau de plus basse énergie, le surplus d'énergie étant expulsé sous forme d'un photon. Ceci explique pourquoi on observe un spectre d'absorption et un spectre d'émission et pourquoi ils ont les mêmes raies c'est-à-dire les mêmes longueurs d'onde. Il manque toutefois une règle de sélection ou de quantification pour identifier les orbites stables parmi une infinité d'orbites possibles. Bohr introduit alors un troisième postulat aussi simple qu'étrange : pour le noyau d'hydrogène, la quantification des niveaux d'énergie découle de la quantification du moment cinétique L → {\textstyle {\vec {L}}} :
où ℏ {\textstyle \hbar } désigne la constante de Planck réduite et n {\textstyle n} un entier positif. Niels Bohr publie alors en son article : On the constitution of atoms and molecules1. Dans celui-ci, il explique pourquoi, après les expériences de Hans Geiger (1913), il opte pour l'atome planétaire de Rutherford (1911) contre l'atome de Thomson (1904). Il indique qu'il est redevable à Max Planck de la notion de quanta et de la constante de Planck. Il reconnaît enfin à l'astronome Seth Barnes Nicholson (1912) l'idée de considérer le moment cinétique. Avec ces postulats, le spectre expérimental de l'hydrogène ainsi que la constante de Rydberg sont prédits théoriquement, et le problème d'instabilité du modèle de Rutherford disparait. Néanmoins, ce succès se fait au prix d'introduction d'hypothèses dites ad hoc, c'est-à-dire qu'elles sont émises et retenues pour le seul fait de coller aux résultats expérimentaux sans que Bohr n'en avance lui-même des idées physiques plus profondes pour les justifier. Ceci le mènera à proposer une théorie radicale et controversée, la théorie BKS (en), théorie qui inspirera Heisenberg pour sa théorie quantique.
Remarques et conséquences
- La formule de Balmer présentée plus haut ne satisfait pas Bohr dans la mesure où cette longueur d'onde est monochromatique, et ne correspond à aucune oscillation de l'électron (il n'y a pas de résonance).
- D'autre part, il n'y a pas de référence à la masse réduite dans cet article, alors qu'elle est souvent présentée comme un succès pour expliquer le passage de la constante de Rydberg théorique R∞ à la constante de Rydberg pour l'atome d'hydrogène RH.
- Toutefois, l'énigme de l'hydrogène de Pickering, moins citée, a pu être résolue : l'astronome Pickering publie des séries de raies qui s'accordent avec la théorie de Rydberg, mais en prenant des valeurs de n et p demi-entiers (1895). Alfred Fowler le confirme en dans une expérience terrestre avec un tube contenant de l'hydrogène et de l'hélium. Bohr a alors l'idée de la réaction suivante H + He → H− + He+, et déclare que l'on voit le spectre de l'ion hydrogénoïde He+ (avec une constante de Rydberg quadruple) donc que l'hydrogène de Pickering n'existe pas. De plus, il interprète alors les raies des métaux alcalins avec des modifications légères des termes de Ritz par des entiers effectifs. Néanmoins, sa théorie ne permet d'interpréter ni le spectre des autres atomes ni celui des molécules.
- Pour la théorie de l'état s de l'hydrogène, il faudra attendre 1926 et l'apparition du principe d'incertitude.
Postulats et théorie
Ce modèle est un complément du modèle planétaire d'Ernest Rutherford qui décrit l'atome d'hydrogène comme un noyau massif et chargé positivement, autour duquel se déplace un électron de masse m {\displaystyle m} et chargé négativement. L'interaction entre ces deux particules est électrostatique, la force intervenant étant la force de Coulomb. Ceci nous permet donc d'écrire l'énergie potentielle de l'électron à une distance r {\displaystyle r} du noyau comme
où ε 0 {\displaystyle \varepsilon _{0}} désigne la permittivité du vide, q e {\displaystyle q_{e}} la charge de l'électron, et e {\displaystyle e} la charge réduite telle que e 2 = q e 2 4 π ε 0 {\displaystyle e^{2}={\frac {q_{e}^{2}}{4\pi \varepsilon _{0}}}} par souci de simplification d'écriture (cf. système d'unités atomiques).
Orbites circulaires stables
Selon le premier postulat de la théorie de Bohr, l'électron ne rayonne aucune énergie lorsqu'il se trouve sur une orbite stable dite encore stationnaire. Cette orbite étant supposée circulaire, l'accélération de cet électron vaut alors a → = − v 2 r u r → {\displaystyle {\vec {a}}=-{v^{2} \over r}{\vec {u_{r}}}} où v {\displaystyle v} est la vitesse de l'électron, et u r → {\displaystyle {\vec {u_{r}}}} est le vecteur unitaire centrifuge. On peut alors invoquer le principe fondamental de la dynamique et écrire :
On en déduit l'énergie cinétique comme étant E c = 1 2 m v 2 = e 2 2 r = − 1 2 E p {\displaystyle E_{c}={\frac {1}{2}}mv^{2}={\frac {e^{2}}{2r}}=-{\frac {1}{2}}E_{p}} et finalement l'énergie mécanique
Quantification du moment cinétique
Le postulat de quantification du moment cinétique L → {\displaystyle {\vec {L}}} veut que L = n ℏ {\displaystyle \ L=n\hbar } où L {\displaystyle L} désigne la norme du moment cinétique, n {\displaystyle n} est un entier positif non nul représentant la couche où se situe l'électron, et ℏ {\displaystyle \hbar } est la constante de Planck « réduite » d'un facteur 2 π {\displaystyle \pi } . Seules les orbites ayant ce moment cinétique ne rayonnent pas : les orbites sont donc « quantifiées » par le nombre entier n positif. En développant le moment cinétique d'une orbite circulaire, cette relation s'écrit :
Cette quantification a été confirmée par l'expérience de Franck et Hertz, dont l'intérêt a été de montrer que la quantification n'est pas seulement due à celle de la lumière, mais résulte bien de la quantification de l'orbite des électrons de l'atome.
On obtient alors un système des deux équations, m v 2 r = e 2 r 2 ⇒ v = e m r {\textstyle {\frac {mv^{2}}{r}}={\frac {e^{2}}{r^{2}}}\Rightarrow v={\frac {e}{\sqrt {mr}}}} et m v r = n ℏ ⇒ r = n ℏ m v {\textstyle mvr=n\hbar \Rightarrow r={\frac {n\hbar }{mv}}} , à deux inconnues qui sont la distance noyau-électron r {\displaystyle r} et la vitesse de l'électron v {\displaystyle v} . On peut résoudre ce système en remplaçant r {\displaystyle r} par n ℏ m v {\textstyle {\frac {n\hbar }{mv}}} dans v = e m r {\textstyle v={\frac {e}{\sqrt {mr}}}} , on obtient alors simplement l'expression explicite de v {\displaystyle v}
qui ne dépend que de constantes physiques et d'un nombre entier qui caractérise les orbitales. On voit d'emblée que plus n est grand, moindre est la vitesse. La vitesse maximale (correspondant à n = 1) est appelée vitesse de Bohr e 2 ℏ = q e 2 ℏ 4 π ε 0 = c α {\textstyle {\frac {e^{2}}{\hbar }}={\frac {q_{e}^{2}}{\hbar 4\pi \varepsilon _{0}}}=c\alpha } où c désigne la vitesse de la lumière dans le vide et α {\textstyle \alpha } la constante de structure fine, elle vaut à peu près 2,19 × 106 m s−1 dans le cas de l'hydrogène, ce qui est très faiblement relativiste2. En remplaçant v {\displaystyle v} par sa solution e 2 n ℏ {\textstyle {\frac {e^{2}}{n\hbar }}} dans r = n ℏ m v {\textstyle r={\frac {n\hbar }{mv}}} , on obtient l'expression explicite de r {\displaystyle r}
où a 0 = ℏ 2 m e 2 = ℏ 2 k m q e 2 {\textstyle a_{0}={\frac {\hbar ^{2}}{me^{2}}}={\frac {\hbar ^{2}}{kmq_{e}^{2}}}} est appelé le rayon de Bohr, le plus petit rayon possible (correspond à n = 1), soit environ 53 pm = 5,3 × 10−11 m. Et k {\displaystyle k} est la constante de Coulomb k = 1 4 π ε 0 ≅ 9 × 10 9 N ⋅ m 2 ⋅ C − 2 {\displaystyle k={\frac {1}{4\pi \varepsilon _{0}}}\cong 9\times 10^{9}\;{\rm {N\cdot m^{2}\cdot C^{-2}}}}
En conséquence, l'énergie totale de l'électron est aussi quantifiée :
où E 1 = − k 2 m q e 4 2 ℏ 2 {\textstyle E_{1}=-{k^{2}mq_{e}^{4} \over 2\hbar ^{2}}} est appelée l'énergie de Rydberg (voir constante de Rydberg). Toutefois, elle est plus communément appelée énergie du niveau fondamental car elle correspond au niveau d'énergie le plus bas possible (correspond à n = 1), et vaut environ −13,6 eV pour l'hydrogène.
Dans le modèle quantique qui a remplacé le modèle de Bohr, il n'existe en fait pas de position ni de vitesse précise d'un électron, et il ne peut donc parcourir un « cercle » ; son orbitale peut en revanche être parfois à symétrie sphérique.
Quantification du rayonnement
Selon le dernier postulat, l'électron ne rayonne ou n'absorbe de l'énergie que lors d'un changement d'orbite.
On retrouve la formule de Rydberg.
Notes et références
- (en) Niels Bohr, « On the constitution of Atoms and Molecules. Part I - Binding of Electrons by Positive Nuclei », Philos. Mag. series 6, vol. 26, , p. 1-24 (lire en ligne [archive]).
- Le rapport vitesse de Bohr sur vitesse de la lumière est égale à la constante de structure fine soit 1/137 ce qui n'est pas négligeable. Ceci poussera Sommerfeld à réécrire le modèle de Bohr dans le cadre de la relativité restreinte où les orbites circulaires sont remplacées par des orbites elliptiques, et où un deuxième nombre quantique apparaît.
Voir aussi
Articles connexes
- Spectre de l'hydrogène
- Expérience de Franck et Hertz
- Constante de Rydberg, formule de Rydberg pour l'explication en mécanique quantique
- Atome d'hydrogène
- Rayon de Bohr
- Saturation des inégalités d'Heisenberg
- Système d'unités atomiques
- Quantification semi-classique
- Régime semi-classique
Liens externes
- Ressource relative à la santé
- :
- (cs + sk) WikiSkripta
-
Notice dans un dictionnaire ou une encyclopédie généraliste
- « De la constitution des atomes et des molécules » [archive], bibnum, article de 1913, commenté, .
- « Atome : bienvenue à Bohr » [archive], La Méthode scientifique, France Culture, .
Antimatière
En physique des particules, l'antimatière est l'ensemble des antiparticules qui ont la même masse et le même spin, mais des charges, nombres baryoniques et nombres leptoniques opposés aux particules ordinaires.
L'antimatière n'existe qu'en quantités infimes dans l'univers local, soit dans les rayons cosmiques, soit produite en laboratoire. Les travaux sur l'antimatière consistent en grande partie à expliquer la rareté de l'antimatière par rapport à la matière. Selon la théorie du Big Bang, la matière et l'antimatière devraient avoir été présentes en quantités égales.
Principes et histoire
La différence entre matière et antimatière se fait au niveau des charges (dont la charge électrique) : les particules composant l'antimatière ont des charges opposées à celles des particules jouant le même rôle dans la matière. Par exemple, la matière comprend les protons, positifs, et les électrons, négatifs. L'antimatière comprend donc les antiprotons, négatifs, et les antiélectrons (ou positonsnote 1), positifs.
Pour une particule élémentaire de charge nulle, il est possible d'être sa propre antiparticule : c'est le cas du photon.
L'antimatière a été imaginée quand Paul Dirac a écrit l'équation portant son nom en 19281, et remarqué qu'elle s'appliquait encore pour des particules de charge opposée2. Il en déduit que pour chaque particule, il existe une antiparticule correspondante, ayant les mêmes caractéristiques, mais de charge opposée3.
La première particule d'antimatière découverte est un antiélectron (ou positon), détectée par Carl David Anderson qui étudiait les traces des rayons cosmiques4.
En 1936, Fritz Zwicky étudie à l'observatoire du Mont Palomar de la matière et l'antimatière dans les étoiles et les galaxies5.
L'antiproton est découvert en 1955 par Emilio Segrè, l'antineutron en 1956 par Bruce Cork6.
En 1965 a lieu la création du premier « antinoyau » avec un antideutéron, noyau de l'antideutérium, dans le Proton Synchrotron du CERN7 et au Alternating Gradient Synchrotron (en) du Laboratoire national de Brookhaven8.
En 1995 le premier atome d’antimatière est créé, l’antihydrogène, dans un laboratoire du CERN à Genève9
En 2010 sont créés les premiers antihypernoyaux10.
Le , des chercheurs du CERN ont annoncé qu’ils ont réussi à piéger pour la première fois des atomes d’antihydrogène dans un champ magnétique11.
En 2011 est observé le plus lourd antinoyau : un noyau d'4He (antihélium-4)12
En 2019, on connaît les antiparticules des quarks étrange, bottom et charmé4.
La réaction matière-antimatière
L'antimatière et la matière, quand elles entrent en contact, peuvent s'annihiler mutuellement. Elles sont alors transformées en énergie, suivant l'équation E=mc2. En fait, il s'agit de la seule situation connue dans laquelle la masse est intégralement convertie en énergie. Par comparaison, une réaction nucléaire classique ne dégage qu'une très petite partie de l'énergie "de masse" contenue dans les combustibles nucléaires utilisés (~1 millième), cette dernière dégageant pourtant bien plus d'énergie encore qu'une combustion (~1 million de fois plus).
Ce phénomène est réversible : de l'énergie peut être transformée en couple matière/antimatière. Mais il faut une concentration d'énergie énorme pour y parvenirnote 2.
Ce phénomène ne peut être utilisé comme source d'énergie puisque la seule antimatière dont on dispose est fabriquée en laboratoire précisément par cette réaction. Les lois de conservation des phénomènes physiques rendent impossible un gain d'énergie conséquent à la création puis la destruction d'antimatière.
L'antimatière pourrait en revanche être théoriquement employée comme moyen de stockage de l'énergie, mais pour l'instant l'énergie à employer pour créer de l'antimatière est égale à 108 fois l'énergie récupérée13.
La symétrie CPT
C, P et T sont des opérations de symétrie respectivement par inversion de la charge électrique, de la parité (c'est-à-dire des coordonnées dans l'espace à 3 dimensions) et du temps. On s'intéressera alors à considérer que l'évolution d'un système lui conserve ou non l'une, 2 ou ces 3 symétries.
Selon le modèle standard, la matière et l'antimatière devraient se trouver en quantités égales dans l'univers, ce qui n'est pas le cas. Avec l'amélioration des techniques d'observation, l'absence d'antimatière a été établie dans notre galaxie, puis dans les galaxies voisines, et enfin dans tout l'univers visible14. Une hypothèse avancée par les scientifiques est l’existence d’une asymétrie entre la matière et l’antimatière. Cette asymétrie serait à l’origine de l’absence apparente d’antimatière dans l’Univers. En effet, supposons que la matière et l’antimatière soient parfaitement symétriques, étant en quantités égales après le Big-bang, toute la matière et l’antimatière se seraient statistiquement annihilées. Notre existence montre qu’il reste pourtant encore de la matière. Il ne semble donc pas y avoir de symétrie complètenote 3. Cette asymétrie est révélée par une légère différence entre les interactions d’une particule de matière et d’une antiparticule. Cette dissymétrie a été expliquée en 1965 par Andreï Sakharov à l’aide de la « brisure de symétrie CP » (découverte expérimentalement en 1964). Cependant, cette brisure fut longtemps contestée, et il semble que Sakharov n’était pas au courant de ces expériences lorsqu’il publia son modèle.[réf. nécessaire]
Sakharov a déterminé trois conditions pouvant expliquer le passage d'un univers constitué à égalité de matière et d'antimatière à un univers constitué exclusivement de matière :
- qu'il y ait des différences entre les lois régissant l'évolution de la matière et celles de l'antimatière.
- qu'il existe un processus violant la conservation du nombre baryonique.
- qu'il y ait rupture de l'équilibre thermique.
La première violation de la symétrie charge parité (abrégée en symétrie CP) est constatée en 1964 sur les quarks étranges. En 2001, la violation de la symétrie CP est trouvée sur les quarks bottom, et en mars 2019 le LHC la détecte pour les quarks charmés4.
« Victoire » de la matière par violation de CP
Les kaons neutres sont des particules qui se transforment spontanément en leurs propres antiparticules, et ceci dans les deux sens. Mais il existe une asymétrie dans cette transformation, y compris vis-à-vis de la symétrie CP : la transformation d'un kaon en antikaon est légèrement plus lente que l'inverse. Le nombre de kaons présents tend donc à être supérieur à celui d'antikaons à un instant donné15.
Cette asymétrie peut expliquer que l'antimatière se soit retrouvée en très légère minorité (un milliardième de moins) face à la matière (1 000 000 000 particules d'antimatière pour 1 000 000 001 particules de matière classique). L'annihilation mutuelle a alors conduit à ne laisser que de la matière, en quantité infime par rapport à la quantité présente avant l'annihilation.
L'antimatière serait au-delà de notre champ de vision
Une toute petite partie de l'Univers serait visible parce que les plus grands télescopes possèdent une limite et que l'antimatière peut très bien se trouver au-delà de ce champ de vision.[pas clair]
De surcroît, plus on regarde loin, plus on voit dans le passé, la lumière prenant un certain temps à voyager. Or, l'Univers a environ 13,7 milliards d'années. Par conséquent, il n'est possible de voir que les objets dont la lumière aura voyagé pendant moins de 13,7 milliards d'années (ce qui situe la limite de l'univers observable à une distance spatiale, non pas de 13,7 milliards d'années-lumière, mais de 43 milliards d'années-lumière, à cause de l'expansion de l'Univers). L'antimatière peut se trouver au-delà de cet « horizon » visible.
On observe actuellement aux frontières de l'univers observable des éléments de la taille d'une galaxie, mais illuminant l'espace avec l'intensité de milliards de galaxies. Selon certaines hypothèses, ces objets célestes pourraient être des régions où matière et antimatière se rencontreraient et se concentreraient, sous l'attraction gravitationnelle, en une sorte de galaxie mixte où les rencontres entre matière et antimatière seraient très nombreuses, d'où leur forte luminosité.[réf. nécessaire]
Cependant, comme dit plus haut, le photon étant sa propre antiparticule, rien ne permet de distinguer facilement une lointaine galaxie (ou un amas) d'antimatière d'une galaxie (ou d'un amas) de matière. Enfin, on peut faire remarquer que, pour faire coexister dans un seul univers matière et antimatière, il suffit d'admettre que cet Univers est fortement structuré et que, pour une raison encore non établie, il n'y a pas "mélange immédiat" de ces deux parties.
Hypothèse antigravitaire
Une hypothèse avancée16 est cependant qu'il pourrait y avoir dissymétrie gravitationnelle entre particules et antiparticules au niveau de leur masse pesante (mais pas forcément de leur masse inerte), avec dans le cas extrême un phénomène d'antigravité pour ces dernières : diverses expériences au CERN (GBar17, AlphaG18, ou encore Aegis) visent d'ailleurs sur 2019-2021 à mesurer une telle éventuelle dissymétrie de l'antimatière.
Dans le cas extrême (modélisé par un Univers dit de Dirac-Milne promu par le physicien français Gabriel Chardin), la répulsion entre matière et anti-matière, et entre les particules d'anti-matière elles-mêmes, aurait conduit ces dernières non pas à se concentrer en astres comme pour la matière, mais au contraire à se diluer au maximum dans l'espace (un peu comme un gaz dans un ballon prend tout le volume disponible), à l'écart des zones de concentration de matière, dans les régions actuellement désignées comme vides spatiaux.
Ainsi dans cette hypothèse encore minoritaire, les antiparticules n'auraient aucunement mystérieusement disparu lors du Big-Bang, mais se retrouveraient simplement diluées dans ces régions au point d'être indétectables.
Un anti-univers
Une hypothèse propose que l'antimatière ait été projetée, lors de la formation de l'Univers, dans un univers « parallèle », composé alors uniquement d'antimatière (ou, du moins, où la matière serait aussi rare que l'antimatière dans le nôtre). Cet univers parallèle serait alors appelé « anti-univers ». L'hypothèse est assez minoritaire19.
Elle ne doit pas être confondue avec l'hypothèse de Sakharov, pour qui il existe un univers constitué d'antimatière avant l'instant zéro, et de matière après20.
Dans la pratique
État de la recherche
Production naturelle d'antimatière
Grâce au télescope spatial Fermi, Michael Briggs, astrophysicien à l’université d’Alabama, a découvert que la foudre produisait des antiparticules (des positons)21. L’annihilation réciproque de ces positons et des électrons correspondants (leurs antiparticules) se manifeste sous la forme de rayonnements gamma dont le pic à 511 keV est typique d’un tel phénomène. L’énergie due à cette rencontre entre matière et antimatière monte vers la haute atmosphère pendant ces orages22.
Par ailleurs, une ceinture naturelle d'antiprotons a été découverte autour de la Terre23.
Production et conservation
La recherche sur la production et le stockage de l'antimatière s'améliore rapidement au cours du temps: ainsi aujourd'hui on est capable de créer de l'antimatière, en utilisant notamment les accélérateurs de particules. Les accélérateurs de particules, en projetant des particules l'une contre l'autre, entraînent la formation d'antiprotons et de positons (des antiélectrons). Il est désormais possible de les isoler des autres particules via une méthode complexe, puis de les piéger dans un champ magnétique sous vide.
Des chercheurs ont déjà stocké ainsi des millions d'antiparticules dans des réservoirs pendant une semaine. La difficulté du stockage semble a priori réglée, les temps de stockage s'améliorant rapidement, ainsi que le savoir-faire permettant de produire les quantités suffisantes requises par le besoin des expériences, (mais en aucun cas en tant que stockage d'énergie). Cependant, ces antiparticules étant à grande vitesse après leur création, il faut les ralentir très fortement pour obtenir des antiatomes faciles à étudier : ce processus n'est pas encore résolu. L'expérience Aegis24, qui est menée au CERN, a pour but de tester l'effet de la gravité sur l'antimatière25.
Perspectives
Production
Avec une « usine à antimatière » utilisant les techniques actuelles, construite exclusivement afin d'en produire (contrairement aux accélérateurs de particules, dont ce n'est pas le but premier), la quantité d'antimatière produite pourrait augmenter considérablement.
Les quantités produites, accumulées pendant plusieurs mois ou années, pourraient peut-être contribuer aux voyages spatiaux. En effet, une énorme quantité de carburant n'est déterminante qu'au décollage, pour échapper à l'attraction terrestre; que l'on se rappelle par exemple le rapport de volume entre une capsule spatiale et la fusée qui l'envoie hors de l'atmosphère : l'essentiel du carburant est consacré à accélérer le carburant encore non consommé.
Dans le domaine spatial
Les recherches de la NASA prédisent qu'il serait possible de disposer de 10 mg d'antimatièrenote 4, suffisante pour un voyage Terre-Mars, pour 250 millions de dollars « seulement »26.
Dans le domaine militaire
Une bombe utilisant un gramme d'antimatière libérerait une énergie de 43 kilotonnes, soit trois fois la bombe d'Hiroshima. Cependant, le coût de production empêche en pratique l'utilisation d'une telle bombe27.
L'antimatière pourrait servir de détonateur à une réaction de fusion thermonucléaire. Cela permettrait de se débarrasser du détonateur de la bombe H, qui est une bombe A (réaction de fission, très polluante, de matériaux lourds de type uranium ou plutonium).
Ainsi, les 5 kg de plutonium nécessaires à une réaction en chaine de fission ne seraient plus indispensables et seraient remplacés par quelques microgrammes d'antimatière. La taille des bombes H serait ainsi facilement réduite, ce qui permettrait leur utilisation dans les guerres conventionnelles. De plus, les retombées radioactives (sans la bombe A) seraient considérablement réduites par la non-utilisation d'éléments radioactifs à longue période.
En médecine
L'antimatière pourrait servir lors de certaines radiothérapies28,29,30. L'antimatière permettrait d'irradier quatre fois plus de cellules cancéreuses avec moins de séquelles sur les tissus sains, parfois abîmés par les rayonnements utilisés.
Le PET-Scan (Positron Emission Tomography) ou tomographie par émission de positons utilise d'ores et déjà les propriétés d'interaction positon-électron à des fins de diagnostic. On injecte du glucose contenant des noyaux radioactifs dans le corps de la personne qui subit le PET-Scan. La désintégration de ces noyaux radioactifs émet des positons, qui vont réagir avec les électrons présents dans le corps humain selon la réaction matière-antimatière. Cela produit des photons à une énergie particulière, permettant de les identifier. In fine, on peut savoir où se sont fixées les molécules de glucose dans le corps4.
Dans la science-fiction
Plusieurs œuvres de science-fiction traitent de l'antimatière14. C'est notamment le cas d'Anges et Démons de Dan Brown, où le vol d'un gramme d'antimatière est une clé de l'intrigue, ou bien le mode de propulsion du vaisseau spatial Enterprise de Star Trek6. L'antimatière est aussi utilisée comme arme et comme moyen de propulsion dans L'Aube de la nuit de Peter F. Hamilton, ainsi que comme arme de destruction dans La Spirale du temps de Roger Leloup.
Notes et références
Notes
- positon ou positron en anglais
- Par l'équation E=mc2, l'énergie contenue dans 1 g de matière et 1 g d'antimatière est de l'ordre de 50 GWh.
- D'autres hypothèses avaient été quelque temps envisagées, comme celle qu'il reste un nombre important d'étoiles, voire de galaxies, entièrement composées d'antimatière, en raison des hétérogénéités de départ; elles n'ont cependant pas eu de suite.
- Une masse de 10 mg d'antimatière s'annihilant avec autant de matière représente une énergie de 1,8 TJ, soit l'équivalent de 430 tonnes de TNT, soit ~1/35e de la bombe d'Hiroshima (15 kt TNT équivalent = 6,276 1013 J = 62,76 TJ ; avec 1 t TNT = 4,184 GJ)
Références
- Futura-Sciences, « Antimatière » [archive], sur Futura-Sciences (consulté le )
- Erwan Cario, « L'antimatière Mais qu'est-il donc arrivé au Némésis de la matière? » [archive], sur Libération, (consulté le )
- « L'antimatière » [archive], sur Organisation européenne pour la recherche nucléaire (consulté le )
- Sébastien Gavois, « Première nuit de l'antimatière : retour sur ces énigmatiques particules » [archive], sur nextinpact.com, (consulté le ).
- Histoire de l'astronomie de Charles-Albert Reichen, 1964 (Le cercle du Bibliophile et ENI) coll. Erik Nitsche
- Patrick Nedelec, « Les secrets de l'antimatière » [archive], sur pourlascience.fr, (consulté le ).
- (en) Massam, T., et al., « Experimental observation of antideuteron production », Il Nuovo Cimento, vol. 39, , p. 10–14
- (en) Dorfan, D. E., et al., « Observation of Antideuterons », Phys. Rev. Lett., vol. 14, no 24, , p. 1003-1006 (DOI 10.1103/PhysRevLett.14.1003, lire en ligne [archive])
- Paul Indelicato, « Des pommes, des poires et de l’antigravité? » [archive], sur lejournal.cnrs.fr, (consulté le ).
- (en) Collaboration STAR, « Observation of an Antimatter Hypernucleus », Science, (lire en ligne [archive])
- (en) « Scientists capture antimatter atoms in particle breakthrough » [archive], sur CNN.com, (consulté le )
- STAR Collaboration, « Observation of the antimatter helium-4 nucleus », Nature, vol. 473, , p. 353–356 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/nature10079, lire en ligne [archive], consulté le )
- « CERN - À la une : Anges et démons » [archive], sur public.web.cern.ch (consulté le )
- ROMÀN IKONICOFF, « Antimatière : son absence reste un mystère » [archive], sur science-et-vie.com, (consulté le ).
- Gabriel Chardin, « L'antimatière » [archive], sur cosmosaf.iap.fr (consulté le )
- Yaroslav Pigenet, « Un Univers sans matière noire » [archive], sur lejournal.cnrs.fr, (consulté le )
- (en) « GBAR - The Gravitational Behaviour of Antihydrogen » [archive], sur home.cern/
- « Le Cern sur la piste de l'antigravité avec GBAR et Alpha-g » [archive], sur www.futura-sciences.com, (consulté le )
- « Science: An Anti-Matter Universe? », Time, (ISSN 0040-781X, lire en ligne [archive], consulté le )
- « sakharov » [archive], sur ysagnier.free.fr (consulté le )
- (en) « Signature of antimatter detected in lightning » [archive], sur Science News
- Science et Vie, janvier 2010, p. 12, Les éclairs créent de l’antimatière !
- « New Particle Found Among the Anti Matter Circling Earth's Magnetic Field » [archive], sur International Business Times TV (consulté le )
- Antimatter Experiment: Gravity, Interferometry, Spectroscopy.
- Antimatière : est-elle la clé de l'Univers ? Science et vie, octobre 2009, no 1105, p. 67.
- (en) « NASA - New and Improved Antimatter Spaceship for Mars Missions » [archive], sur www.nasa.gov (consulté le )
- « Science et guerre : 1 gramme d'antimatière = 3 Hiroshima » [archive], sur sicencesetavenir.fr, (consulté le ).
- (en) Paul Gilster, « A Practical Use for Antimatter » [archive], sur centauri-dreams.org, (consulté le ).
- (en) « Antiproton portable traps and medical applications » (version du 22 août 2011 sur l'Internet Archive)
- Julie Crédou, « L'antimatière contre le cancer » [archive], sur linternaute.com, (consulté le ).
Voir aussi
Bibliographie
- Maurice Duquesne, Matière et antimatière, Paris, Presses universitaires de France, coll. « Que sais-je? » (no 767), , 6e éd., 125 p. (ISBN 978-2-13-037229-5, BNF 34687402)
- Robert L. Forward et Joel Davis (trad. Nicolas Prantzos), Les Mystères de l'antimatière [« Mirror matter »], Monaco, Le Rocher, coll. « L'esprit et la matière », (ISBN 978-2-268-01225-4, OCLC 26819301)
- Gabriel Chardin, L'antimatière, la matière qui remonte le temps, Paris, Éditions Le Pommier, coll. « Poche » (no 6), (ISBN 978-2-7465-0288-8, BNF 40183134)
- Bernard PIRE et Jean-Marc RICHARD, Antimatière, Encyclopedia Universalis (lire en ligne [archive])
- (en) Gordon Fraser, Antimatter : The Ultimate Mirror, Cambridge University Press, , 224 p. (ISBN 978-0-521-89309-1, présentation en ligne [archive])
- Richard Schaeffer, « L’anti-matière» (pp. 103-115), In Marie-Odile Monchicourt (sous la direction de), Chaos et Cosmos, Paris, Éditions Le Mail, 1986, (ISBN 2-226-15564-3)
Articles connexes
- Antiparticule, équation de Majorana
- Symétrie CP
- Principe anthropique
- Interaction gravitationnelle de l'antimatière
Liens externes
- « Antimatière, cet obscur objet de la physique » [archive], La Méthode scientifique, France Culture, 1 avril 2019.
- « Où est donc passée l'anti-matière ? » [archive], La Méthode scientifique, France Culture, 20 décembre 2016.
- Pour la Science, dossier Les Symétries de la nature, no 20, : Traite de l'asymétrie cosmique entre la matière et l'antimatière, Site de Pour la science [archive]
- Dossier Antimatière [archive], futura-sciences.com
- L'antimatière selon Hubert Reeves [archive] (suite de 5 textes)
- Article simplifié [archive]
- Portail de la physique
- Portail de la cosmologie
- Portail de la science-fiction
- Portail de l’astronautique
gamma-Butyrolactone
Pour les articles homonymes, voir GBL.
| γ-butyrolactone | ||
 |
||
 |
||
| Structure de la γ-butyrolactone. | ||
| Identification | ||
|---|---|---|
| Nom UICPA | gamma-Butyrolactone | |
| Synonymes |
Tétrahydro-2-furanone |
|
| No CAS | ||
| No ECHA | 100.002.282 | |
| No CE | 202-509-5 | |
| FEMA | 3291 | |
| Apparence | liquide hygroscopique, incolore, huileux1. | |
| Propriétés chimiques | ||
| Formule | C4H6O2 [Isomères] | |
| Masse molaire4 | 86,089 2 ± 0,004 2 g/mol C 55,81 %, H 7,02 %, O 37,17 %, |
|
| Moment dipolaire | 4,27 ± 0,03 D2 | |
| Diamètre moléculaire | 0,527 nm3 | |
| Propriétés physiques | ||
| T° fusion | −44 °C1 | |
| T° ébullition | 204 °C1 | |
| Solubilité | dans l'eau : miscible | |
| Paramètre de solubilité δ | 25,8 MPa1/2 (25 °C)5 | |
| Masse volumique | 1,1 g cm−31 | |
| T° d'auto-inflammation | 455 °C1 | |
| Point d’éclair | 98 °C (coupelle fermée)1 | |
| Limites d’explosivité dans l’air | 0,3–16,0 %vol1 | |
| Pression de vapeur saturante | à 20 °C : 0,15 kPa1 | |
| Thermochimie | ||
| Cp | ||
| Propriétés optiques | ||
| Indice de réfraction | n D 25 {\displaystyle {\textit {n}}_{D}^{25}} 1,4343 | |
| Précautions | ||
| NFPA 704 | ||
| Classification du CIRC | ||
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme7 | ||
| Écotoxicologie | ||
| LogP | −0,571 | |
| Caractère psychotrope | ||
| Catégorie | Dépresseur | |
| Mode de consommation |
Ingestion |
|
| Autres dénominations |
GBL |
|
| Risque de dépendance | Modéré | |
| Composés apparentés | ||
| Isomère(s) | Diacétyle | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
La γ-butyrolactone (GBL) est un composé organique volatil, précurseur de l'acide γ-hydroxybutyrique (GHB). Elle est utilisée dans l'industrie comme solvant de peinture, époxyde ou vernis à ongles où ses caractéristiques de solvant dissout le plastique et les vernis.
Cette lactone possède une faible odeur caractéristique de beurre rance (l'acide butyrique tirant son nom du beurre, les lactones faisant primordialement référence aux compositions et décompositions acides-alcools du lait où elles ont été découvertes par distillation). Son odeur est encore décrite comme celle d'une eau vaseuse ou de plastique brûlé. On la retrouve à l'état naturel à la concentration de 3 à 10 et même 20 μg/mL (0,02 mL/L) dans différents vins8, plus particulièrement rouges. C'est du point de vue chimique la plus simple des lactones.
Elle est souvent improprement employée au masculin pour évoquer le psychotrope en confusion avec le genre masculin du GHB.
Usages
Elle est très utilisée industriellement pour diluer les peintures ou encore pour effacer les tags et s'utilise pour lessiver les métaux exposés à de fortes pollutions comme les jantes chromées de voiture, ou a même pu s'utiliser pour lustrer les boules et pistes de bowling à un niveau de jeu professionnel. Très corrosive pour les peintures et les plastiques, il est important de tester les produits sur une surface non visible avant de l'utiliser.
Depuis les évènements tragiques survenus en 2009 qui ont concerné Loana[réf. nécessaire], elle n'est plus disponible à l'état pur (sans dilution avec d'autres produits comme les agents tensioactifs non ioniques ou autres détergents, qui empêchent rigoureusement son ingestion) dans plusieurs pays d'Europe, notamment en France, mais reste permise dans les échanges européens. Elle a en outre été remplacée par d'autres produits dans la plupart des formules accessibles au grand public, comme les vernis à ongles, qui ne contiennent plus de GBL.
Effet sur l'organisme
Dans le corps humain, la gamma-butyrolactone se transforme en gamma-hydroxybutyrate (GHB)9 ; c'est pour cela qu'elle produit les mêmes effets que le GHB : euphorie, production d'hormone de croissance, relaxation, augmentation de la libido ; coma potentiellement mortel en cas d'overdose.
Ce solvant peut être détourné en drogue10. Ses dosages sont très faibles, entre 0,25 et 2,0 ml le plus souvent et strictement selon la sensibilité individuelle (dose très inférieure à celle de l'alcool pur, de vingt à quarante fois plus fortes plus les doses de GBL sont élevées). Au-delà, une sédation lourde amenant à un profond sommeil et une incapacité à rester éveillé peut se faire ressentir, et ce typiquement entre 1,2 et 2,5 ml maximum. La prise à jeun augmente la vitesse d'absorption et donc les effets, qui se font ressentir en moins de 20 min au lieu de 45 à 60 min. Les effets durent d'une à quelques heures (quatre à cinq) et sont soumis à une accoutumance qui a été mesurée en laboratoire chez les rats après des prises répétées et quotidiennes. Au bout de la 5e heure, la totalité du produit à l'exception de traces, est métabolisée en eau et dioxyde de carbone.
Comme pour le GHB, les faibles doses peuvent produire une euphorie, une sensation vertigineuse et une exacerbation de la sensibilité (libido, érotisme tactile…) de type alcool, sans pour autant perturber la vigilance ni distordre les perceptions au degré de ce dernier. Une envie de dormir succombante peut se faire ressentir et peut s'avérer très dangereuse selon les circonstances. Des doses plus fortes bloquent l'effet euphorique et tout le système de récompense (même des opiacés), notamment dopaminergique, et provoquent un puissant effet hypnotique. Le dosage est ainsi délicat et peut s'avérer problématique ou traitre en cas de prise répétée ou rapprochées ; l'accumulation peut amener à une concentration provoquant ce pressant sommeil. L'espace entre les doses induisant une pseudo-ébriété et celles hypnotiques est faible. Chaque utilisateur utilise une dose ou un rang de dosage qui lui est propre et pratique des « réajustements » (prise d'une fraction précise de dose à des moments donnés pour prolonger les effets ou les rehausser).
Son caractère hautement acide, tout autant que sa saveur écœurante, impose une haute dilution préalable à toute consommation et c'est pourquoi le GHB (également appelé drogue du violeur) lui est préféré car il est nettement moins dangereux. Le GBL est aussi beaucoup moins stable quand il est dilué (il se dégrade vite en milieu aqueux et au contact d'acides ou de bases). Ses pics plasmatiques se montrent plus aigus (plus concentrés et provoquant plus de somnolence), imprévisibles (absorption aléatoire) et nauséeux. Pour ces raisons, le GBL n'est pas souvent recherché comme psychotrope, il n'est considéré que comme un succédané parfois redouté et mal perçu du GHB.
Relation chimique entre GBL et GHB
L'ouverture du cycle de la GBL s'effectue généralement en milieu basique par exemple en présence de soude caustique.
La réaction se produit par attaque nucléophile de l'ion hydroxyde (HO−) sur le carbone portant la fonction ester interne (lactone), celui-ci étant déficitaire en électrons par l'effet inductif attracteur de l'oxygène. Le cycle s'ouvre (lactonolyse) par retour d'un doublet d'électrons sur l'oxygène. On obtient ainsi le gamma-hydroxybutyrate. Une réaction de saponification peut en découler et conduire à la formation de gamma-hydroxybutyrate de sodium (sel sodique de l'acide gamma-hydroxybutyrique).
À noter : en milieu basique ou fortement anhydre, le GHB peut être reconverti dans sa forme lactone, donc en GBL.
Cadre légal
En France, le ministère chargé de la Santé a décidé d’interdire par arrêté du la vente et la cession au public de la GBL et du butane-1,4-diol (1,4-BD)11, deux produits qui entrent notamment dans la synthèse du GHB.
Le texte concerne la GBL en tant que matière première, ainsi que des produits manufacturés en contenant une concentration supérieure à 10 % et/ou d'un volume de plus de 100 ml.
Les sanctions pénales prévues en cas de vente ou de cession au public de la GBL et du 1,4-BD sont de trois ans d'emprisonnement et de 45 000 euros d'amende.
L’article L 3421-4 du code de la santé publique prévoit d’ailleurs une peine de cinq ans d’emprisonnement et 75 000 euros d’amende pour celui qui inciterait à l’usage de la GBL en la présentant comme ayant des propriétés stupéfiantes12.
Enfin, le fait de faire absorber, par violence ou par ruse, de la GBL à quelqu’un est susceptible d’être qualifié pénalement sur la base de l’administration de substance nuisible (article 222-15 du code pénal) et est passible à ce titre de peines pouvant aller jusqu’à quinze ans de réclusion criminelle13.
Voir aussi
Articles connexes
Notes et références
- gamma - BUTYROLACTONE [archive], Fiches internationales de sécurité chimique .
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1 et 1-4200-6679-X), p. 9-50.
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, Angleterre, John Wiley & Sons, , 239 p. (ISBN 0-471-98369-1).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 » [archive], sur www.chem.qmul.ac.uk.
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, lire en ligne [archive]), p. 294.
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub. Co., (ISBN 0-88415-857-8).
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Évaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » [archive], sur http://monographs.iarc.fr [archive], CIRC, (consulté le ).
- The presence of gamma-hydroxybutyric acid (GHB) and gamma-butyrolactone (GBL) in alcoholic and non-alcoholic beverages [archive].
- « gamma-Butyrolactone - Fiche toxicologique no 247 » [archive], INRS, mars 2018.
- Les syndromes d'addiction et de manque sous GHB (et GBL) [archive], sur projectghb.org.
- Arrêté du 2 septembre 2011 portant application d'une partie de la réglementation des stupéfiants à la gamma-butyrolactone (GBL), au 1,4-butanediol (1,4 BD) et aux produits qui en contiennent [archive].
- « Article L 3421-4 du code de la santé publique » [archive], sur legifrance.gouv.fr (consulté le ).
- « Code pénal - Article 222-15 » [archive], sur legifrance.gouv.fr (consulté le ).
Nucléosynthèse explosive
La nucléosynthèse explosive est la création de nouveaux éléments chimiques par une supernova, un collapsar1 ou une fusion d'étoiles à neutrons2 au cours de la fusion explosive de l'oxygène et du silicium3. Parmi les éléments synthétisés, on trouve par exemple, le soufre, le chlore, l'argon, le sodium, le potassium, le scandium ainsi que des éléments du pic du fer : chrome, manganèse, fer, cobalt et nickel. Leur abondance augmente dans le milieu interstellaire environnant après leur éjection4.
Les éléments plus lourds que le nickel sont créés principalement par une capture rapide des neutrons dans un processus appelé le processus r. Cependant, il y a aussi d'autres processus qui pourraient être responsables de la création d'éléments lourds à partir d'éléments légers, notamment le processus de capture de proton, connu sous le nom de processus rp, et un processus de photodésintégration qui se nomme le processus gamma (ou p). Celui-ci synthétise les plus légers, la plupart pauvres en neutrons.
Nucléosynthèse stellaire
Dans les processus de fusion nucléaire se produisant lors d'une nucléosynthèse stellaire, la masse maximale d'un élément fusionné est celle du fer, atteignant un isotope ayant une masse atomique de 56. Avant une supernova, les éléments de fusion entre le silicium et le fer peuvent être produits seulement dans les plus grosses étoiles, dans le processus de combustion du silicium.
Un procédé de capture de neutrons lents, connu sous le nom de processus s qui se produit également lors de la nucléosynthèse stellaire normale, peut créer des éléments jusqu'au bismuth, avec une masse atomique d'environ 209. Toutefois, le processus s survient principalement chez les étoiles de faible masse qui évoluent plus lentement.
Supernova
Une supernova est l'explosion marquant la fin de la vie d'une étoile massive.
On distingue essentiellement deux types de supernova, les supernovas thermonucléaires (Ia) et les supernovas à effondrement de cœur (II). Les Ia se produisent dans un système qui contient au moins une naine blanche, lorsque celle-ci est suffisamment proche d'une géante rouge : un transfert de matière peut survenir, ce qui entraine une augmentation de la masse de la naine. Lorsque celle-ci atteint 1,4 de masse solaire, un processus s'enclenche, menant surtout à des réactions thermonucléaires de fusion de carbone et d'oxygène décrites par les lois de la mécanique quantique. Une explosion violente survient alors, soufflant complètement l'étoile5.
Le deuxième type de supernova survient lorsque des étoiles massives de plus de 10 masses solaires ont totalement consommé leur « combustible nucléaire ». À ce moment, il y a un effondrement des couches externes de l'étoile engendré par l'absence soudaine de compensation de la force de gravité par la pression des radiations engendrée par les réactions thermonucléaires6.
Une fois que le noyau ne parvient pas à produire suffisamment d'énergie pour soutenir l'enveloppe externe des gaz, l'étoile explose en supernova produisant la majeure partie des éléments au-delà du fer. La production des éléments du fer à l'uranium se produit en quelques secondes dans une explosion de supernova. En raison de la grande quantité d'énergie libérée, les températures et densités beaucoup plus élevées que les températures normales stellaires sont atteintes. Ces conditions permettent un environnement où les éléments transuraniens pourraient être formés7.
Processus r
Durant la nucléosynthèse de supernova, le processus r (r pour rapide) crée des isotopes lourds très riches en neutrons, qui se désintègrent après l'événement au premier isotope stable, ainsi créant les isotopes stables riches en neutrons de tous les éléments lourds. Ce processus de capture de neutron se produit dans des conditions de température élevée et de haute densité en neutrons.
Notes et références
- (en) Daniel M. Siegel, Jennifer Barnes et Brian D. Metzger, « Collapsars as a major source of r-process elements », Nature, vol. 569, (lire en ligne [archive]).
- (en) Imre Bartos et Szabolcs Marka, « A nearby neutron-star merger explains the actinide abundances in the early Solar System », Nature, vol. 569, (lire en ligne [archive]).
- (en) S. E. Woosley, W. D. Arnett et D. D. Clayton, « Explosive burning of oxygen and silicon », The Astrophysical Journal Supplement, vol. 26, , p. 231–312 (DOI 10.1086/190282, Bibcode 1973ApJS...26..231W, résumé [archive], lire en ligne [archive])
- Astrophysique Sur Mesure, « La nucléosynthèse dans les étoiles massives » [archive], L'Observatoire de Paris
- « Dictionnaire : Supernova » [archive], sur http://www.futura-sciences.com [archive]
- Serge Jodra, « Les supernovae » [archive], sur http://www.cosmovisions.com [archive],
- Collectif d'auteurs [archive], « Premier volet de la trilogie : Comment se forment les éléments, Comment se forment les minéraux, Comment se forment les cristaux. » [archive], 18 décembre 2010 (dernière mise à jour)
Articles connexes
- Portail de l’astronomie
-
Hydrogène
Cet article concerne l'élément chimique. Pour le corps simple H2, voir Dihydrogène. Pour la théorie quantique de l'atome d'hydrogène, voir Atome d'hydrogène.
Hydrogène 
Hydrogène liquide dans une chambre à bulles.← Hydrogène → Hélium 
1H ↑ H ↓ Li Tableau complet • Tableau étendu Position dans le tableau périodique Symbole H Nom Hydrogène Numéro atomique 1 Groupe 1 Période 1e période Bloc Bloc s Famille d'éléments Non-métal Configuration électronique 1s1 Électrons par niveau d’énergie 1 Propriétés atomiques de l'élément Masse atomique 1,007 94 ± 0,000 07 u1,2 Rayon atomique (calc) 25 pm (53 pm) Rayon de covalence 31 ± 5 pm3 Rayon de van der Waals 120 pm4 État d’oxydation -1, +1 Électronégativité (Pauling) 2,2 Oxyde amphotère Énergies d’ionisation5 1re : 13,598 443 eV Isotopes les plus stables Iso AN Période MD Ed PD MeV 1H 99,9885 % stable avec 0 neutron 2D 0,0115 % stable avec 1 neutron 3T traces (syn.) 12,32 a β– 0,019 3He Propriétés physiques du corps simple Masse volumique 0,089 88 g L−1 (gaz, CNTP),
0,070 8 kg L−1 (liquide, −253 °C),
0,070 6 kg L−1 (solide, −262 °C)1Système cristallin Hexagonal Divers No CAS Précautions NFPA 7046 Transport -Unités du SI & CNTP, sauf indication contraire. modifier 
L'hydrogène est l'élément chimique de numéro atomique 1, de symbole H. L'hydrogène présent sur Terre est presque entièrement constitué de l'isotope 1H (un proton, zéro neutron) ; il comporte environ 0,01 % de 2H (un proton, un neutron). Ces deux isotopes sont stables. Un troisième isotope 3H (un proton, deux neutrons), instable, est produit dans les explosions nucléaires. Ces trois isotopes sont respectivement appelés « protium », « deutérium » et « tritium ».
L'hydrogène peut avoir les nombres d'oxydation 0 (dihydrogène H2 ou hydrogène métallique), +I (dans la plupart de ses composés chimiques) et –I (dans les hydrures métalliques). L'hydrogène est un élément électropositif, fréquemment ionisé à l'état H+ ou H3O+. Il forme aussi des liaisons covalentes (notamment dans le dihydrogène et les hydrocarbures) et des liaisons de nature intermédiaire appelées liaisons hydrogène (notamment dans la molécule d'eau et la matière organique).
L'hydrogène est le principal constituant du Soleil et de la plupart des étoiles (dont l'énergie provient de la fusion thermonucléaire de cet hydrogène), et de la matière interstellaire ou intergalactique. C'est un composant majeur des planètes géantes, sous forme métallique au cœur de Jupiter et de Saturne, et sous la forme de dihydrogène solide, liquide ou gazeux dans leurs couches plus externes et dans les autres planètes géantes. Sur Terre, il est surtout présent à l'état d'eau liquide, solide (glace) ou gazeuse (vapeur d'eau), mais on le trouve aussi dans les émanations de certains volcans sous la forme de H2 et de CH4 (méthane).
Le corps simple H2 est mis en évidence à l'état gazeux par Cavendish en 1766, qui l'appelle « air inflammable » parce qu'il brûle ou explose en présence d'oxygène, produisant de la vapeur d'eau. Lavoisier désigne ce gaz sous le nom d'hydrogène, composé du préfixe hydro-, du grec ὕδωρ (hudôr) signifiant « eau », et du suffixe -gène, du grec γεννάω (gennaô), « engendrer »7. Son nom scientifique est désormais « dihydrogène », mais dans la langue courante on continue à l'appeler « hydrogène ».
Abondance
L'hydrogène est l'élément le plus abondant de l'Univers : 75 % en masse et 92 % en nombre d'atomes. Il est présent en grande quantité dans les étoiles et les planètes gazeuses ; il est également le composant principal des nébuleuses et du gaz interstellaire.
Dans la croûte terrestre, l'hydrogène ne représente que 0,22 % des atomes, loin derrière l'oxygène (47 %) et le silicium (27 %)8. Il est rare également dans l'atmosphère terrestre, puisqu'il ne représente en volume que 0,55 ppm des gaz atmosphériques. Sur Terre, la source la plus commune d'hydrogène est l'eau, dont la molécule est constituée de deux atomes d'hydrogène et d'un atome d'oxygène ; l'hydrogène est surtout le principal constituant (en nombre d'atomes) de toute matière vivante, associé au carbone dans tous les composés organiques. Par exemple, l'hydrogène représente 63 % des atomes et 10 % de la masse du corps humain8. Des accumulations d'hydrogène existent dans la croûte terrestre, l'une d'elles au Mali est quasiment pure (à 96%) et est utilisée pour produire de l'électricité9. D'autres sont actuellement recherchées10.
Sous de très faibles pressions, comme celles qui existent dans l'espace, l'hydrogène a tendance à exister sous forme d'atomes individuels car il n'entre pas en collision avec d'autres atomes pour se combiner. Les nuages d'hydrogène sont à la base du processus de la formation des étoiles.
L'atome d'hydrogène
L'hydrogène est l'élément chimique le plus simple ; son isotope le plus commun est constitué seulement d'un proton et d'un électron. L'hydrogène est l'atome le plus léger. Comme il ne possède qu'un électron, il ne peut former qu'une liaison covalente : c'est un atome univalent.
Cependant, l'hydrogène solide peut être métallique lorsqu'il se trouve sous très haute pression. Il cristallise alors avec une liaison métallique (voir hydrogène métallique). Dans le tableau périodique des éléments, il se trouve dans la colonne des métaux alcalins. N'étant toutefois pas présent dans cet état sur Terre, il n'est pas considéré comme un métal en chimie.
La section efficace de capture de l'hydrogène (200 mb aux neutrons thermiques et 0,04 mb aux neutrons rapides)11 est suffisamment faible pour permettre l'utilisation de l'eau comme modérateur et réfrigérant des réacteurs nucléaires.
Mécanique quantique
L'atome d'hydrogène est l'atome le plus simple qui existe. C'est donc celui pour lequel la résolution de l'équation de Schrödinger, en mécanique quantique, est la plus simple. L'étude de ce cas est fondamentale, puisqu'elle a permis d'expliquer les orbitales atomiques, et ensuite les différentes liaisons chimiques avec la théorie des orbitales moléculaires.
Isotopes et propriétés nucléaires
Isotopes
L’hydrogène est le seul élément dont chaque isotope porte un nom spécifique, car leur différence de masse (comparativement à celle de l'atome d'hydrogène) est significative : du simple au double ou au triple, ce qui explique que, contrairement à ce qui vaut pour les isotopes en général, ces différences peuvent influencer les propriétés chimiques du deutérium ou du tritium par rapport au protium (effet isotopique). L'eau lourde (D2O), qui contient des isotopes d'hydrogène lourds, est par exemple toxique (à forte dose) pour de nombreuses espèces. En effet, en raison de la grande différence de masse entre les isotopes la cinétique des réactions en solution aqueuse est considérablement ralentie.
Les isotopes les plus notables de l'hydrogène sont :
- l’hydrogène léger ou protium 1H, le plus abondant (~99,98 % de l'hydrogène naturel). Le noyau est simplement constitué d'un proton et ne possède donc pas de neutron. C'est un isotope stable ;
- le deutérium 2H (ou D), beaucoup moins abondant (de 0,0082 à 0,0184 % de l'hydrogène naturel, ~0,015 % en moyenne). Le noyau est constitué d'un proton et d'un neutron, c'est aussi un isotope stable. Sur Terre, il est essentiellement présent sous forme d'eau deutérée HDO (eau semi-lourde) ;
- le tritium 3H (ou T), présent seulement en quantité infime dans l'hydrogène naturel (un atome de tritium pour 1018 atomes d’hydrogène). Le noyau est constitué d’un proton et de deux neutrons, il est radioactif et se transforme en 3He par émission d'un électron (radioactivité β−). 2H et 3H peuvent participer à des réactions de fusion nucléaire. La radiotoxicité du tritium est réputée très faible lorsqu'il est présent sous forme HTO (eau tritiée), elle est moins connue et moins bien comprise lorsqu'il est présent sous forme organique (les études présentent des résultats contradictoires ou très variables selon leurs protocoles expérimentaux12). Dans l’environnement naturel, le tritium peut prendre la place du protium dans les molécules comprenant de l'hydrogène, y compris dans les molécules biologiques et jusque dans l'ADN où il peut être cause de cassures de l'information génétique, de mutations ou d'apoptoses cellulaires. Le tritium étant un isotope rare, sa concentration dans l'eau et les tissus est généralement très faible (hors contaminations accidentelles d’origine humaine) ;
- le quadrium ou tétradium 4H (ou Q), l'isotope le plus instable de l'hydrogène (sa demi-vie est ultracourte : 1,39 × 10−22 seconde13). Il se décompose par émission de neutron14 ;
- l'hydrogène 7 (7H), l'isotope le plus riche en neutrons jamais observé. Sa demi-vie est de l'ordre de 10−21 seconde15.
Fusion nucléaire
L'hydrogène, présent en grandes quantités dans le cœur des étoiles, est une source d'énergie par les réactions de fusion nucléaire, qui combinent deux noyaux d'atomes d'hydrogène (deux protons) pour former un noyau d'atome d'hélium. Les deux voies de cette fusion nucléaire naturelle sont la chaîne proton-proton, de Eddington, et le cycle carbone-azote-oxygène catalytique, de Bethe et von Weizsäcker.
La fusion nucléaire réalisée dans les bombes à hydrogène ou bombes H concerne des isotopes intermédiaires de la fusion (l'hydrogène se transforme en hélium), comme celle qui se déroule dans les étoiles : isotopes lourds de l'hydrogène, hélium 3, tritium, etc. Mais, dans une bombe H, les réactions nucléaires ne durent que quelques dizaines de nanosecondes, ce qui permet uniquement des réactions en une unique étape. Or, pour aboutir à la transformation de l'hydrogène en hélium, il faut plusieurs étapes dont la première, la réaction d'un proton, est très lente.
Depuis 2006, le projet ITER vise à vérifier la « faisabilité scientifique et technique de la fusion nucléaire comme nouvelle source d’énergie16 ».
Le corps simple hydrogène
Sauf aux pressions extrêmement basses (comme dans l'espace intergalactique) ou extrêmement hautes (comme dans les parties centrales de Jupiter et Saturne), le corps simple hydrogène est formé de molécules H2 (dihydrogène).
Aux pressions extrêmement hautes, l'hydrogène est dans un état dit « sombre », intermédiaire entre un gaz et un métal. Il ne reflète pas la lumière et ne la transmet pas. Il devient aussi très faiblement conducteur d'électricité17. Il s'apparente aux métaux alcalins qui le suivent dans le groupe 1 du tableau de Mendeleïev.
Aux pressions les plus basses, l'hydrogène est un gaz monoatomique.
Isomérie
La molécule de dihydrogène existe sous deux isomères de spin nucléaire: l'hydrogène ortho (spins parallèles) et l'hydrogène para (spins antiparallèles)18.
Hydrogène gazeux
Dans les conditions normales de température et de pression, comme dans la plupart des conditions qui intéressent la chimie et les sciences de la Terre, l'hydrogène est un gaz moléculaire de formule H2, le dihydrogène. Le dihydrogène forme aussi de vastes « nuages moléculaires » dans les galaxies, qui sont à l'origine de la formation des étoiles.
À très basse pression et très haute température l'hydrogène est un gaz monoatomique (donc de formule H), c'est notamment le cas du gaz interstellaire ou intergalactique. En raison de l'immensité de ces espaces et malgré la très faible densité du gaz, l'hydrogène monoatomique constitue près de 75 % de la masse baryonique de l'univers19.
Hydrogène liquide
Hydrogène solide
L'hydrogène solide est obtenu en abaissant la température en dessous du point de fusion du dihydrogène, situé à 14,01 K (−259,14 °C)20. L'état solide fut obtenu pour la première fois en 1899 par James Dewar21,22.
Hydrogène métallique
L'hydrogène métallique est une phase de l'hydrogène survenant lorsqu'il est soumis à une très forte pression et à de très basses températures. C'est un exemple de matière dégénérée. D'aucuns estiment qu'il y a un intervalle de pressions (autour de 400 GPa) dans lequel l'hydrogène métallique est liquide, même à de très basses températures23,24.
Hydrogène triatomique
L'hydrogène triatomique est une forme allotropique très instable du corps simple hydrogène, de formule H325.
Propriétés chimiques et composés
Ions hydron H+, hydronium H3O+ et hydrure H−
L'atome d'hydrogène peut perdre son unique électron pour donner l'ion H+, désigné couramment par le nom de proton. En effet l'atome qui a perdu son seul électron est réduit à son noyau, et dans le cas de l'isotope le plus abondant 1H, ce noyau n'est constitué que d'un proton. Cette appellation n'est pas rigoureusement correcte si l'on tient compte de la présence, certes discrète (inférieure à 0,02 %), des autres isotopes. L'appellation hydron est plus générale (on dit aussi ion hydrogène, malgré la confusion possible avec l'anion H−). Son rayon est très petit : environ 1,5 × 10−15 m contre 5 × 10−11 m pour l'atome.
En solution, le proton n'existe pas à l'état libre mais est toujours lié au nuage électronique d'une molécule. En solution aqueuse il est solvaté par des molécules d'eau ; on peut en simplifiant considérer qu'il est capté par une molécule d'eau H2O, formant un ion « hydronium » H3O+, aussi appelé « oxonium » ou « hydroxonium ».
L'atome d'hydrogène peut aussi acquérir un second électron pour donner l'ion « hydrure » H−, ce qui lui confère le même cortège électronique stable que l'atome d'hélium.
Réactions acido-basiques
L'hydrogène joue un rôle primordial dans une réaction acido-basique (au sens de la théorie de Brønsted-Lowry) puisque cette dernière correspond formellement à l'échange d'un ion hydrogène H+ entre deux espèces, la première (l'acide) libérant H+ par rupture d'une liaison covalente, et la deuxième (la base) captant cet H+ par formation d'une nouvelle liaison covalente :
- AH + B = A − + BH + acide1 base2 base1 acide2 {\displaystyle {\begin{matrix}{\mbox{AH}}&+&{\mbox{B}}&=&{\mbox{A}}^{-}&+&{\mbox{BH}}^{+}\\{\mbox{acide1}}&&{\mbox{base2}}&&{\mbox{base1}}&&{\mbox{acide2}}\end{matrix}}}
Liaison hydrogène
La liaison hydrogène est une interaction électrostatique entre un atome d'hydrogène, lié chimiquement à un atome électronégatif A, et un autre atome électronégatif B (A et B étant typiquement O, N ou F en chimie organique).
Cette liaison joue un rôle important en chimie organique, puisque les atomes d'oxygène O, d'azote N ou de fluor F sont susceptibles de créer des liaisons hydrogène, mais aussi en chimie inorganique, entre les alcools et les alcoolates métalliques.
Composés covalents
L'atome d'hydrogène peut engager son unique électron pour former une liaison covalente avec de nombreux atomes non-métalliques.
Les composés les plus connus sont :
- la molécule de dihydrogène H2 ;
- la molécule d'eau H2O ;
- les molécules d'hydrocarbures CxHy.
L'hydrogène est également présent dans toutes les molécules organiques, où il est lié principalement à des atomes de carbone, d'oxygène et d'azote.
Hydrures
L'hydrogène se combine avec la plupart des autres éléments car il possède une électronégativité moyenne (2,2) et peut ainsi former des composés avec des éléments métalliques ou non-métalliques. Les composés qu'il forme avec les métaux sont appelés « hydrures », dans lesquels il se trouve sous forme d'ions H− trouvés généralement en solution. Dans les composés avec les éléments non-métalliques, l'hydrogène forme des liaisons covalentes, car l'ion H+ a une forte tendance à s'associer avec les électrons. Dans les acides en solution aqueuse, il se forme des ions H3O+ appelés ions « hydronium » ou « oxonium », association du proton et d'une molécule d'eau.
Agressivité à l'égard des matériaux
L'hydrogène corrode de nombreux systèmes d'alliages en les fragilisant26. Ceci peut conduire à des défaillances catastrophiques, par exemple de piles à combustible ou de certains processus catalytiques. C'est un problème grave pour les industries qui produisent ou utilisent de l'hydrogène. C'est encore un frein à la production, au transport, au stockage et à un large usage de ce produit26.
La science des matériaux recherche des matériaux plus résistants à la fragilisation par l'hydrogène, mais ce travail est rendu difficile par la difficulté de mesurer ou d'observer l'hydrogène de manière expérimentale et à l'échelle atomique26. Chen et al. ont observé en 2017 la répartition tridimensionnelle précise des atomes d'hydrogène dans un acier ferritique au moyen d'une sonde atomique tomographique fondée sur le deutérium[C'est-à-dire ?], le transfert cryogénique[Quoi ?] et des algorithmes d'analyse de données27,26,28,29.
Toxicité, écotoxicité
Très peu d'études semblent avoir été menées à ces sujets, probablement parce que les organismes vivants ne sont pas supposés être dans la nature exposés à de l'hydrogène gazeux. En effet, ce gaz étant très léger, il se disperse rapidement vers les très hautes couches de l'atmosphère.
En matière de toxicité pour l'homme, l'hydrogène peut être absorbé dans l’organisme par inhalation. En milieu industriel ou en présence d'une fuite importante, une concentration nocive de ce gaz (sans odeur) dans l'air peut être rapidement atteinte (et former aussi un mélange explosif avec l'air, l'oxygène, les halogènes et tout oxydant puissant, surtout en présence d'un catalyseur métallique comme le nickel ou le platine)30. À concentration élevée, l'hydrogène expose à une aggravation de problèmes pulmonaires préexistant et à une anoxie, avec alors des « symptômes tels que maux de tête, bourdonnements dans les oreilles, vertiges, somnolence, perte de conscience, nausée, vomissements et dépression de tous les sens » et une peau pouvant prendre une teinte bleutée, avant asphyxie si l'exposition se prolonge30.
L'hydrogène n'est pas à ce jour (2019) connu comme étant source de mutagénicité, d'embryotoxicité, de tératogénicité ni de toxicité pour la reproduction30.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Hydrogen » (voir la liste des auteurs).
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-420-09084-0)
- IUPAC Commission on Isotopic Abundances and Atomic Weights donne : min : 1,00784 max : 1,00811 moy : 1,007975 ± 0,000135.
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », Dalton Transactions, , p. 2832 - 2838 (DOI 10.1039/b801115j)
- Paul Arnaud, Brigitte Jamart, Jacques Bodiguel, Nicolas Brosse, Chimie Organique 1er cycle/Licence, PCEM, Pharmacie, Cours, QCM et applications, Dunod, , 710 p., Broché (ISBN 2100070355)
- (en) Ionization Energies of Atoms and Atomic Ions, in CRC Handbook of Chemistry and Physics, 91e éd. (version Internet 2011), W. M. Haynes, éd., CRC Press/Taylor & Francis, Boca Raton, FL., p. 10-203
- (en) « HYDROGEN » [archive], sur https://cameochemicals.noaa.gov [archive]
- Paul Depovere, La classification périodique des éléments. La merveille fondamentale de l'Univers, De Boeck Supérieur, , p. 103.
- p. 6 Reginald H. Garrett, Charles M. Grisham et B. Lubochinsky (trad. Bernard Lubochinsky), Biochimie, Paris, De Boeck Université, , 1292 p. (ISBN 978-2-7445-0020-6, OCLC 44434958, BNF 37106164)
- Alain Prinzhofer, Cheick Sidy Tahara Cissé et Aliou Boubacar Diallo, « Discovery of a large accumulation of natural hydrogen in Bourakebougou (Mali) », International Journal of Hydrogen Energy, vol. 43, no 42, , p. 19315–19326 (ISSN 0360-3199, DOI 10.1016/j.ijhydene.2018.08.193, lire en ligne [archive], consulté le )
- (en) Isabelle Moretti, Emyrose Brouilly, Keanu Loiseau et Alain Prinzhofer, « Hydrogen Emanations in Intracratonic Areas: New Guide Lines for Early Exploration Basin Screening », Geosciences, vol. 11, no 3, , p. 145 (ISSN 2076-3263, DOI 10.3390/geosciences11030145, lire en ligne [archive], consulté le )
- On trouve aussi 332 mb aux neutrons thermiques.
- Annabelle Comte, Fiche radiotoxicologique « tritium » du CEA, version 12-2005.
- G. Audi, O. Bersillon, J. Blachot et A. H. Wapstra, The NUBASE evaluation of nuclear and decay properties [archive], Nuclear Physics A, 729, 2003, p. 3, 27, 128.
- G. M. Ter-Akopian et al., Hydrogen-4 and Hydrogen-5 from t+t and t+d transfer reactions studied with a 57.5-MeV triton beam, Nuclear Physics in the 21st Century: International Nuclear Physics Conference INPC 2001, American Institute of Physics Conference Proceedings, 610, p. 920-924, DOI:10.1063/1.1470062.
- CNRS, « Découverte de l'hydrogène 7, le système nucléaire le plus exotique jamais observé » [archive] [PDF], communiqué de presse, 19 novembre 2007
- (en) ITER Objectives [archive], sur le site iter.org.
- « Optical Properties of Fluid Hydrogen at the Transition to a Conducting State » [archive]
- « Hydrogène » [archive], sur savoirs.essonne.fr
- (en) D. Palmer, « Hydrogen in the Universe », sur NASA, .
- (en) Caractéristiques de la fusion et propriétés thermophysiques globales de l'hydrogène solide (1972) [archive]
- (en) Correspondance, cahiers de notes et articles généralistes de James Dewar [archive].
- James Dewar, « Sur la solidification de l'hydrogène », Annales de chimie et de physique, 7e série, vol. 18, , p. 145-150 (lire en ligne [archive])
- (en) Ashcroft N.W., The hydrogen liquids [archive], J. Phys. A, 12, A129-137, 2000.
- (en) Bonev, S.A., Schwegler, E., Ogitsu, T. et Galli, G., A quantum fluid of metallic hydrogen suggested by first principles calculations [archive], Nature, 431, 669, 2004.
- (en) C. Bordas, P. C. Cosby et H. Helm, « Measurement of the lifetime of metastable triatomic hydrogen », The Journal of Chemical Physics, vol. 93, no 9, , p. 6303–6309 (ISSN 0021-9606 et 1089-7690, DOI 10.1063/1.458999, lire en ligne [archive], consulté le ).
- Julie Cairney, « Atoms on the move—finding the hydrogen »', Science, 17 mars 2017, vol. 355, no 6330, p. 1128-1129, DOI:10.1126/science.aam8616 (résumé [archive]).
- (en) Y.-S. Chen, D. Haley, S. S. A. Gerstl, A. J. London, F. Sweeney, R. A. Wepf, W. M. Rainforth, P. A. J. Bagot et M. P. Moody, « Direct observation of individual hydrogen atoms at trapping sites in a ferritic steel », Science, vol. 355, no 6330, , p. 1196–1199 (ISSN 0036-8075, PMID 28302855, DOI 10.1126/science.aal2418).
- Yi-Sheng Chen, Paul A.J. Bagot, Michael P. Moody et Daniel Haley, « Observing hydrogen in steel using cryogenic atom probe tomography: A simplified approach », International Journal of Hydrogen Energy, vol. 44, no 60, , p. 32280–32291 (ISSN 0360-3199, DOI 10.1016/j.ijhydene.2019.09.232).
- Yi-Sheng Chen, Matthew J. Griffith et Julie M. Cairney, « Cryo Atom Probe: Freezing atoms in place for 3D mapping », Nano Today, vol. 37, , p. 101107 (ISSN 1748-0132, DOI 10.1016/j.nantod.2021.101107).
- « Hydrogen - H ; Chemical properties of hydrogen - Health effects of hydrogen - Environmental effects of hydrogen » [archive], Lenntech (consulté le 11 janvier 2019)
Voir aussi
Articles connexes
- Antihydrogène
- Dihydrogène (H2)
- Hydrogène kaonique
- Hydrogène liquide
- Hydrogène métallique
- Hydrogénoduc
- Hydrure
- Macro-élément
- Hydrogénation en chimie organique
- Technologie de l'hydrogène
- Chronologie des technologies de l'hydrogène
- Production d'hydrogène
- Stockage de l'hydrogène
- Pile à combustible
- Véhicule à hydrogène
- Économie hydrogène
Liens externes
- (en) « Technical data for Hydrogen » [archive] (consulté le ), avec en sous-pages les données connues pour chaque isotope.
- (en) Images de l'hydrogène et de ses isotopes sous différentes formes [archive].
- (en) 2001 - Properties of solid hydrogen at very low temperatures [archive].
- (en) Solid hydrogen experiments for atomic propellants [archive].
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7 Fr Ra Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Nh Fl Mc Lv Ts Og 8 119 120 * * 121 122 123 124 125 126 127 128 129 130 131 132 133 134 135 136 137 138 139 140 141 142 Métaux
AlcalinsAlcalino-
terreuxLanthanides Métaux de
transitionMétaux
pauvresMétal-
loïdesNon-
métauxHalo-
gènesGaz
noblesÉléments
non classésActinides Superactinides







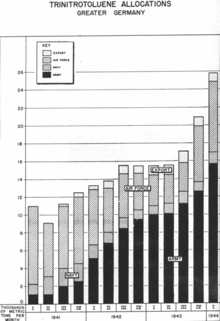


























![Plutonium vu par la tranche sur le salt cake issu du procédé multicycle de réduction directe d'oxyde (MCDOR) : le dioxyde de plutonium PuO2 est dissous dans le chlorure de calcium CaCl2 fondu de 820 à 875 °C dans un creuset en oxyde de magnésium MgO pour y être réduit en plutonium métallique[5].](https://upload.wikimedia.org/wikipedia/commons/a/a4/Pu%2C94.jpg)



![{\displaystyle \mathrm {\xrightarrow[{23.5\ min}]{\beta ^{-}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/f7a91aa1a6ff0b2763a640151dce5797a76165f7)
![{\displaystyle \mathrm {\xrightarrow[{2.3565\ d}]{\beta ^{-}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/7a21e2d7d99345c4b8953cd85639c4bb6c936aeb)
![{\displaystyle \mathrm {\xrightarrow[{2{,}117\;\mathrm {j} }]{\beta ^{-}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/1f755a5bcc4681f2724bfd8940088cf77a9669f3)